
|
HISTORIA TECHNOLOGII, TECHNOLOGII, OBIEKTÓW WOKÓŁ NAS
Dynamit. Historia wynalazku i produkcji
Katalog / Historia technologii, technologii, przedmiotów wokół nas Dynamit to mieszanka wybuchowa, absorbent (na przykład ziemia okrzemkowa) nasycony nitrogliceryną. Może również zawierać inne składniki (saletra itp.). Całość jest zwykle prasowana w cylindryczny kształt i umieszczana w papierowych lub plastikowych opakowaniach. Podważanie ładunku odbywa się za pomocą kapsuły detonatora. Dynamit został opatentowany przez Alfreda Nobla 25 listopada 1867 roku.
Przez kilka stuleci znany był ludziom tylko jeden materiał wybuchowy - czarny proch, który był szeroko stosowany zarówno w wojnie, jak i w pokojowym strzelaniu. Ale druga połowa XIX wieku była naznaczona wynalezieniem całej rodziny nowych materiałów wybuchowych, których niszcząca moc była setki i tysiące razy większa niż prochu strzelniczego. Ich powstanie poprzedziło kilka odkryć. Już w 1838 roku Peluz przeprowadził pierwsze eksperymenty z nitrowaniem substancji organicznych. Istota tej reakcji polega na tym, że wiele substancji zawierających węgiel, potraktowanych mieszaniną stężonych kwasów azotowego i siarkowego, oddaje swój wodór, przyjmując w zamian grupę nitrową NO2 i zamień się w potężne materiały wybuchowe. Inni chemicy badali to interesujące zjawisko. W szczególności Shenbein, azotujący bawełnę, otrzymał piroksylinę w 1846 roku. W 1847 r., działając w podobny sposób na glicerynę, Sobrero odkrył nitroglicerynę, materiał wybuchowy o kolosalnej sile niszczącej. Początkowo nitrogliceryna nikogo nie interesowała. Sam Sobrero powrócił do swoich eksperymentów dopiero 13 lat później i opisał dokładną metodę nitrowania glicerolu. Następnie nowa substancja znalazła zastosowanie w górnictwie. Początkowo wlewano ją do studni, zatykano gliną i wysadzano za pomocą zanurzonego w niej naboju. Jednak najlepszy efekt osiągnięto zapalając kapiszon z piorunianem rtęci. Co tłumaczy wyjątkową wybuchową moc nitrogliceryny? Stwierdzono, że podczas wybuchu ulega on rozkładowi, w wyniku czego najpierw powstają gazy CO2,CO,H2CH4, N2 i NO, które ponownie oddziałują ze sobą, uwalniając ogromną ilość ciepła. Ostateczną reakcję można wyrazić wzorem: 2C3H5 (NIE3)3 = 6 CO2 + 5H2O+3N+0,5O2. Podgrzane do ogromnej temperatury gazy te gwałtownie rozszerzają się, wywierając ogromny nacisk na środowisko. Produkty końcowe wybuchu są całkowicie nieszkodliwe. Wszystko to sprawiało, że nitrogliceryna była nieodzowna do podziemnego strzelania, ale szybko okazało się, że produkcja, przechowywanie i transport tego płynnego materiału wybuchowego wiązały się z wieloma niebezpieczeństwami. Ogólnie rzecz biorąc, czysta nitrogliceryna jest dość trudna do zapalenia z otwartego płomienia. Zapalona zapałka zgniła w nim bez żadnych konsekwencji. Ale z drugiej strony jego wrażliwość na wstrząsy i wstrząsy (detonacja) była wielokrotnie wyższa niż czarnego prochu. Po uderzeniu, często dość nieznacznym, w warstwach poddanych drganiom następował gwałtowny wzrost temperatury, aż do rozpoczęcia reakcji wybuchowej. Minieksplozja pierwszych warstw wywarła nowy wpływ na głębsze warstwy i trwało to aż do wybuchu całej masy materii. Czasami, bez żadnego zewnętrznego wpływu, nitrogliceryna nagle zaczynała się rozkładać na kwasy organiczne, szybko ciemniała, a wtedy wystarczyło najmniejsze potrząsanie butelką, aby spowodować straszną eksplozję. Po wielu wypadkach stosowanie nitrogliceryny zostało niemal powszechnie zakazane. Przemysłowcy, którzy rozpoczęli produkcję tego materiału wybuchowego, mieli dwie możliwości – albo znaleźć stan, w którym nitrogliceryna będzie mniej wrażliwa na detonację, albo ograniczyć produkcję. Jednym z pierwszych, który zainteresował się nitrogliceryną był szwedzki inżynier Alfred Nobel, który założył fabrykę do jej produkcji. W 1864 r. wraz z robotnikami wystartowała jego fabryka. Zginęło pięć osób, w tym brat Alfreda Emil, który miał zaledwie 20 lat. Po tej katastrofie Noblowi groziły znaczne straty – nie było łatwo przekonać ludzi do zainwestowania w tak niebezpieczne przedsięwzięcie. Przez kilka lat badał właściwości nitrogliceryny i ostatecznie udało mu się stworzyć całkowicie bezpieczną jej produkcję. Ale problem transportu pozostał. Po wielu eksperymentach Nobel stwierdził, że nitrogliceryna rozpuszczona w alkoholu jest mniej wrażliwa na detonację. Jednak ta metoda nie zapewniała pełnej niezawodności. Poszukiwania trwały dalej, a wtedy niespodziewany incydent pomógł genialnie rozwiązać problem. Podczas transportu butelek z nitrogliceryną, w celu złagodzenia wstrząsów, umieszczano je w ziemi okrzemkowej, specjalnej ziemi okrzemkowej wydobywanej w Hanowerze. Ziemia okrzemkowa składała się z krzemiennych muszli alg z licznymi zagłębieniami i kanalikami. I raz, podczas transportu, pękła jedna butelka nitrogliceryny i jej zawartość wysypała się na ziemię. Nobel wpadł na pomysł przeprowadzenia kilku eksperymentów z tą ziemią okrzemkową zaimpregnowaną nitrogliceryną. Okazało się, że właściwości wybuchowe nitrogliceryny wcale się nie zmniejszyły z powodu jej wchłonięcia przez porowatą ziemię, ale jej wrażliwość na detonację spadła kilkakrotnie. W tym stanie nie eksplodował ani od tarcia, ani od słabego ciosu, ani od spalenia. Ale z drugiej strony, gdy w metalowej kapsule zapaliła się niewielka ilość piorunu rtęci, nastąpiła eksplozja o tej samej sile, która dała czystą nitroglicerynę w tej samej objętości. Innymi słowy, było to dokładnie to, co było potrzebne, a nawet znacznie więcej niż to, co Nobel miał nadzieję uzyskać. W 1867 roku wykupił patent na odkryty przez siebie związek, który nazwał dynamitem. Siła wybuchu dynamitu jest równie ogromna jak nitrogliceryny: 1 kg dynamitu w ciągu 1/50000 1000000 s wytwarza siłę 1000000 1 1 kgm, czyli wystarczającą do podniesienia 0 01 1 kg na 0 m. Co więcej, jeśli 00002 kg czarnego prochu obraca się w gaz przez 25 sekundy, a następnie XNUMX kg dynamitu w XNUMX sekundy. Ale przy tym wszystkim dobrze wykonany dynamit eksplodował dopiero od bardzo silnego uderzenia. Rozpalony dotykiem ognia, płonął stopniowo bez eksplozji, z niebieskawym płomieniem. Eksplozja nastąpiła dopiero po zapaleniu dużej masy dynamitu (ponad XNUMX kg). Podkopywanie dynamitu, takiego jak nitrogliceryna, najlepiej przeprowadzać za pomocą detonacji. W tym celu Nobel w tym samym roku 1867 wynalazł detonator grzechoczących spłonek. Dynamit natychmiast znalazł najszersze zastosowanie przy budowie autostrad, tuneli, kanałów, linii kolejowych i innych obiektów, co w dużej mierze przesądziło o szybkim wzroście fortuny jego wynalazcy. Nobel założył pierwszą fabrykę do produkcji dynamitu we Francji, następnie uruchomił jego produkcję w Niemczech i Anglii. Przez trzydzieści lat handel dynamitem przyniósł Noblowi ogromne bogactwo – około 35 milionów koron.
Proces wytwarzania dynamitu został zredukowany do kilku operacji. Przede wszystkim konieczne było uzyskanie nitrogliceryny. To był najtrudniejszy i najniebezpieczniejszy moment w całej produkcji. Reakcja nitrowania zachodziła, gdy 1 część glicerolu została potraktowana 6 częściami stężonego kwasu azotowego w obecności XNUMX części stężonego kwasu siarkowego. Równanie wyglądało tak: C3H5(O)3 +3HNO3 = C3H5(NO3)3 + 3H2O. Kwas siarkowy nie brał udziału w związku, ale jego obecność była konieczna, po pierwsze, do wchłonięcia wody uwolnionej w wyniku reakcji, co w przeciwnym razie, rozcieńczając kwas azotowy, uniemożliwiłoby tym samym zakończenie reakcji, a po drugie, aby wyizolować powstałą nitroglicerynę z roztworu w kwasie azotowym, ponieważ będąc dobrze rozpuszczalną w tym kwasie, nie rozpuszczała się w swojej mieszaninie z kwasem siarkowym. Nitracjom towarzyszyło silne wydzielanie ciepła. Co więcej, jeśli na skutek ogrzewania temperatura mieszaniny wzrosłaby powyżej 50 stopni, to przebieg reakcji potoczyłby się w przeciwnym kierunku – rozpoczęłoby się utlenianie nitrogliceryny, któremu towarzyszyłoby gwałtowne uwalnianie tlenków azotu i jeszcze większe ogrzewanie , co doprowadziłoby do wybuchu. Dlatego nitrowanie musiało odbywać się przy ciągłym chłodzeniu mieszaniny kwasów i glicerolu, dodając tę ostatnią stopniowo i stale mieszając każdą porcję. Powstająca bezpośrednio w kontakcie z kwasami nitrogliceryna, posiadająca mniejszą gęstość w porównaniu z mieszaniną kwasów, wypłynęła na powierzchnię i po zakończeniu reakcji mogła być łatwo zebrana. Przygotowanie mieszaniny kwasowej w fabrykach Nobla odbywało się w dużych cylindrycznych naczyniach żeliwnych, skąd mieszanina wchodziła do tzw. aparatu nitracyjnego.
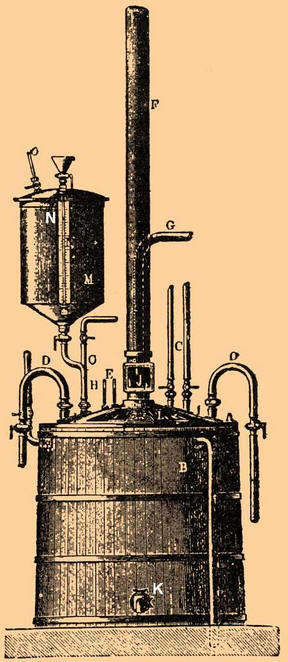
Aparatura składała się z ołowianego naczynia A, które umieszczono w drewnianej wannie B i zamknięto ołowianą pokrywą L, którą podczas pracy posmarowano cementem. Końce dwóch cewek ołowianych D, znajdujących się wewnątrz aparatu, przeszły przez pokrywę (przez nie była stale dostarczana zimna woda). Do aparatu doprowadzono również zimne powietrze przez rurkę C w celu wymieszania mieszaniny. Rurka F usuwała opary kwasu azotowego z aparatu; probówka G służyła do wlania odmierzonej ilości kwaśnej mieszaniny; glicerol wlano przez probówkę H. W naczyniu M mierzono wymaganą ilość tej substancji, którą następnie wstrzykiwano do mieszaniny azotu za pomocą sprężonego powietrza doprowadzonego przez rurkę O. W takiej instalacji jednorazowo można było przetwarzać około 150 kg glicerolu. Po wpuszczeniu wymaganej ilości mieszaniny kwasów i schłodzeniu jej (przepuszczając przez wężownice zimne sprężone powietrze i zimną wodę) do temperatury 15-20 stopni, rozpoczęli rozpylanie ochłodzonej gliceryny. Jednocześnie upewnili się, że temperatura w aparacie nie wzrosła powyżej 30 stopni. Gdyby temperatura mieszaniny zaczęła gwałtownie rosnąć i zbliżać się do krytycznej, zawartość kadzi można było szybko wylać do dużego naczynia z zimną wodą. Operacja tworzenia nitrogliceryny trwała około półtorej godziny. Następnie mieszanina weszła do separatora - ołowianego prostokątnego pudełka ze stożkowym dnem i dwoma kranami, z których jeden znajdował się na dole, a drugi z boku. Gdy mieszanina osiadła i rozdzieliła się, nitrogliceryna została uwolniona przez górny kran, a kwasowa mieszanina przez dolny. Powstała nitrogliceryna została kilkakrotnie przemyta w celu usunięcia nadmiaru kwasów, ponieważ kwas mógł z nią wchodzić w reakcję i spowodować jej rozkład, co nieuchronnie doprowadziło do wybuchu. Aby tego uniknąć, do hermetycznej kadzi doprowadzano wodę z nitrogliceryną i mieszaninę mieszano sprężonym powietrzem. Kwas rozpuścił się w wodzie, a ponieważ gęstość wody i nitrogliceryny znacznie się różniła, oddzielenie ich od siebie nie było trudne. W celu usunięcia resztek wody nitrogliceryna została przepuszczona przez kilka warstw filcu i soli kuchennej. W wyniku tych wszystkich działań uzyskano oleistą żółtawą ciecz, bezwonną i bardzo trującą (zatrucie mogło nastąpić zarówno przez wdychanie oparów, jak i kontakt kropli nitrogliceryny na skórze). Po podgrzaniu powyżej 180 stopni eksplodował ze straszliwą niszczycielską siłą. Przygotowaną nitroglicerynę zmieszano z ziemią okrzemkową. Wcześniej ziemia okrzemkowa została obmyta i dokładnie zmielona. Impregnacja nitrogliceryną odbywała się w drewnianych skrzynkach wyłożonych wewnątrz ołowiem. Po zmieszaniu z nitrogliceryną dynamit przetarto przez sito i wepchnięto do wkładów pergaminowych. W dynamicie z ziemi okrzemkowej w reakcji wybuchowej brała udział tylko nitrogliceryna. Później Nobel wpadł na pomysł impregnacji różnych gatunków prochu nitrogliceryną. W tym przypadku proch również uczestniczył w reakcji i znacznie zwiększył siłę wybuchu. Autor: Ryzhov K.V.
▪ Kompas
Nowy sposób kontrolowania i manipulowania sygnałami optycznymi
05.05.2024 Klawiatura Primium Seneca
05.05.2024 Otwarto najwyższe obserwatorium astronomiczne na świecie
04.05.2024
▪ Lamy pomagają w walce z grypą ▪ Nowe akcelerometry o wysokiej precyzji i małej mocy ▪ Ekologiczne akumulatory do użytku domowego
▪ sekcja serwisu Zegary, timery, przekaźniki, przełączniki obciążenia. Wybór artykułu ▪ artykuł Johanna Gottfrieda Herdera. Słynne aforyzmy ▪ artykuł Jaki jest najgłębszy ocean? Szczegółowa odpowiedź ▪ artykuł Inżynier kosztorysowy działu projektowo-kosztorysowego. Opis pracy ▪ artykuł Wielofunkcyjny miernik częstotliwości. Encyklopedia elektroniki radiowej i elektrotechniki ▪ artykuł Ośmiornica, szkolna guma i mucha. eksperyment fizyczny
Strona główna | biblioteka | Artykuły | Mapa stony | Recenzje witryn www.diagram.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese



 Zobacz inne artykuły Sekcja
Zobacz inne artykuły Sekcja 