
|
ENCYKLOPEDIA RADIOELEKTRONIKI I INŻYNIERII ELEKTRYCZNEJ Charakterystyka porównawcza elementów galwanicznych w rozmiarze AA. Encyklopedia elektroniki radiowej i elektrotechniki
Encyklopedia radioelektroniki i elektrotechniki / Ładowarki, akumulatory, ogniwa galwaniczne Dziś w sklepach i na rynkach można znaleźć wiele różnych ogniw galwanicznych. Które wybrać? Ten artykuł pomoże Ci podjąć właściwą decyzję. Ogniwa i baterie galwaniczne są szeroko stosowane do zasilania różnych urządzeń elektronicznych. Najczęściej stosowane są elementy w rozmiarze AA. Na półkach można znaleźć podobne produkty różnych firm, głównie dwa systemy elektrochemiczne: solankowy i alkaliczny. Niedawno firma Energizer wprowadziła na rynek baterie litowe 1,5 V AA. Najważniejsza cecha ogniwa galwanicznego – pojemność (ilość energii elektrycznej, jaką jest ono w stanie oddać do obciążenia) – prawie nigdy nie jest podana na etykiecie. Kupujący może skupić się na telewizyjnych reklamach ogniw, które „pracują nawet dziesięciokrotnie dłużej niż konwencjonalna sól” lub zaufać firmie Energizer, która twierdzi, że nowe ogniwa litowe AA e2 wytrzymują pięć razy dłużej niż konwencjonalne baterie alkaliczne [1 ] Co więcej, nie jest do końca jasne, które elementy nazywa się „zwykłymi”. Aby ilościowo porównać parametry elementów różnych układów elektrochemicznych, konieczne jest ich badanie w tych samych warunkach. Takie testy przeprowadzono z trzema rodzajami ogniw: solnym Philips Long Life (emf „świeżego” ogniwa – 1,65 V), alkalicznym Duracell Ultra M1,62 (2 V) i litowym Energizer e1,8 (15 V). Każdy z nich został obciążony rezystorem 100 omów, co odpowiada początkowemu prądowi rozładowania wynoszącemu około 1 mA. Dla elementów o rozmiarze AA taki prąd obciążenia jest typowy. Rozładunek odbywał się w cyklach kilkugodzinnych na dobę, co odpowiada rzeczywistym warunkom pracy. Wyjaśnia to skoki napięcia na krzywych rozładowania pokazanych na ryc. XNUMX. Niebieska krzywa odpowiada pierwiastkowi soli, czerwona – zasadowemu, a zielona – litowi. Podczas „spoczynku” napięcie na elemencie dowolnego typu nieznacznie wzrosło, ale po podłączeniu obciążenia szybko spadło do minimum w poprzednim cyklu. Kropki oznaczają wartości pola elektromagnetycznego elementów - napięcia na nich bez obciążenia.
Jeżeli za kryterium całkowitego rozładowania ogniwa przyjmiemy spadek napięcia przy jego obciążeniu do 0,9 V, wyznaczona doświadczalnie pojemność ogniwa solnego wyniosła 1 Ah, ogniwa alkalicznego – 2,9 Ah, a ogniwa litowego – 3,5. Ach. W związku z tym nie ma potrzeby mówić o jakichkolwiek pięcio- czy dziesięciokrotnych różnicach w pojemności elementów różnych układów elektrochemicznych. Na ryc. 2 pokazuje kolejną serię krzywych.
Pokazują, jak zmieniał się opór wewnętrzny elementów podczas procesu rozładowania. Zależność między typem elementu a kolorem krzywej jest taka sama jak na ryc. 1. Wartości oporu wewnętrznego R obliczono ze wzoru
gdzie E jest polem elektromagnetycznym elementu; U - napięcie pod obciążeniem; RH to rezystancja obciążenia. Opór wewnętrzny soli i pierwiastków alkalicznych wzrasta monotonicznie w miarę ich rozładowywania. A opór litu, który gwałtownie spadł na początku wyładowania, pozostaje praktycznie niezmieniony aż do samego końca, a następnie równie gwałtownie wzrasta. Oczywiście przeprowadzonych eksperymentów nie można nazwać wyczerpującymi. Pojemność elementu nie jest wartością ściśle stałą, zależy od wielu czynników zewnętrznych. Dla różnych elementów jego maksimum można osiągnąć w znacznie odmiennych warunkach rozładowania. Aby to wszystko uwzględnić, należałoby przeprowadzić bardzo dużą serię eksperymentów, nierealnych w warunkach amatorskich. Spróbujmy jednak sprawdzić uzyskane wyniki za pomocą obliczeń. Aby teoretycznie oszacować maksymalną możliwą pojemność elementów różnych układów elektrochemicznych, należy znać skład chemiczny ich elektrod, elektrolitu oraz reakcję chemiczną zachodzącą w elemencie. W ogniwach solnych i alkalicznych katodą jest cynk, a anodą dwutlenek manganu. Z tego powodu pierwiastki takie nazywane są zbiorczo manganem-cynkiem. Ale elektrolit w nich jest inny: sól (zwykle chlorek amonu) lub zasada (wodorotlenek potasu). Według [2] reakcja zachodzi w solach manganu i cynku
i alkaliczne
Nie ma wiarygodnych informacji na temat materiału elektrod i reakcji chemicznej zachodzącej w ogniwie litowym. Możemy jedynie założyć, że elektrodami są lit i dwutlenek manganu, a elektrolitem jest roztwór nadchloranu litu w węglanie propylenu. Jeśli to przypuszczenie jest słuszne, zgodnie z [2] reakcji ulega ogniwo litowe
Korzystając z prawa Faradaya, otrzymujemy wyrażenie określające pojemność ogniwa galwanicznego C, Ah:
gdzie m to masa reagujących substancji. F = 96,5-103 C/g-eq to liczba Faradaya; n - wartościowość (dla ogniw galwanicznych solnych i alkalicznych - 2, dla litu - 1); M jest całkowitą masą cząsteczkową reagentów. Ważymy ogniwa galwaniczne o rozmiarze AA: sól – 17 g, alkalia – 24 g, lit – 15 g. ) jest pomijalna i można ją pominąć. Całkowitą masę cząsteczkową reagujących substancji obliczamy z powyższych równań reakcji chemicznych: dla soli - 346 g, dla zasad - 257 g, dla litu - 94 g. Podstawiając wartości liczbowe do wzoru otrzymujemy maksymalna możliwa pojemność elementu solnego – 2,6 Ah, alkalicznego – 5 Ah, litowego – 4,3 Ah. Różnice między obliczonymi wartościami pojemności a zmierzonymi można wyjaśnić raczej przybliżonymi założeniami przyjętymi w obliczeniach. Nie stwierdzono więc różnic pięcio- i dziesięciokrotnych. Teoretyczna pojemność ogniwa alkalicznego jest około dwukrotnie większa niż ogniwa solnego, a lit nie ma pod tym względem przewagi nad ogniwem alkalicznym. Jest to zgodne z wynikami eksperymentów. Na podstawie wyników wszystkich wykonanych prac możemy stwierdzić, co następuje: 1. Ogniwa litowo-galwaniczne charakteryzują się najbardziej stabilnym napięciem, najniższą rezystancją wewnętrzną, która praktycznie nie zależy od stopnia rozładowania i największą, choć niewielką, pojemnością. Najlepiej stosować je do zasilania urządzeń o dużym poborze prądu, a także w urządzeniach, które automatycznie wyłączają się w przypadku spadku napięcia zasilania (np. aparatów cyfrowych). 2. Ogniwa alkaliczne mają pojemność porównywalną z litem i są również w stanie dostarczyć do obciążenia duży prąd, ale przy niższym napięciu. Najlepiej sprawdzają się w urządzeniach o średnim poborze prądu bez automatycznej regulacji napięcia. W wielu przypadkach ogniwa alkaliczne są preferowane zamiast litowych, ponieważ są trzy do czterech razy tańsze. 3. Ogniwa solne mają najmniejszą pojemność i najwyższy opór wewnętrzny. Wskazane jest stosowanie ich w urządzeniach o niskim poborze prądu. literatura
Autor: I.Podushkin, Moskwa
Sztuczna skóra do emulacji dotyku
15.04.2024 Żwirek dla kota Petgugu Global
15.04.2024 Atrakcyjność troskliwych mężczyzn
14.04.2024
▪ Turbina wiatrowa Challenergy odporna na silne wiatry ▪ Elektronika pomoże kierowcy samochodu uniknąć wypadku ▪ Kształt ucha wpływa na słuch
▪ część witryny Zasilanie. Wybór artykułów ▪ artykuł Korespondencja modeli i obudów magnetowidów GRUNDIG. Informator ▪ artykuł Jak działają banki krwi? Szczegółowa odpowiedź ▪ artykuł Zastępca Dyrektora Generalnego. Opis pracy
Komentarze do artykułu: gość Artykuł wyjaśniający, dziękuję.
Strona główna | biblioteka | Artykuły | Mapa stony | Recenzje witryn www.diagram.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese






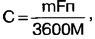
 Zostaw swój komentarz do tego artykułu:
Zostaw swój komentarz do tego artykułu: