
|
Notatki z wykładów, ściągawki
Terapia szpitalna. Notatki z wykładu: krótko, najważniejsze
Katalog / Notatki z wykładów, ściągawki Spis treści
WYKŁAD nr 1. Choroby układu sercowo-naczyniowego. Reumatyzm Reumatyzm (choroba Sokolskiego-Buyo) to ogólnoustrojowa choroba zapalna tkanki łącznej z dominującą lokalizacją procesu w układzie sercowo-naczyniowym, która rozwija się u osób do niej predysponowanych (z reguły są to młodzi ludzie) z powodu ostrej infekcji paciorkowce β-hemolizujące grupy A . Tę definicję choroby podał w 1989 roku V. A. Nasonov. Odzwierciedla wszystkie charakterystyczne cechy choroby: 1) dominujące uszkodzenie układu sercowo-naczyniowego; 2) rola dziedziczności patologicznej; 3) znaczenie infekcji paciorkowcami. Istota choroby polega na pokonaniu wszystkich błon serca, ale głównie mięśnia sercowego i wsierdzia z występowaniem deformacji aparatu zastawkowego - choroby serca i późniejszego rozwoju niewydolności serca. Klęska innych narządów i układów w reumatyzmie ma drugorzędne znaczenie i nie determinuje jej nasilenia i późniejszego rokowania. Etiologia. Paciorkowce beta-hemolizujące grupy A powodują uszkodzenie górnych dróg oddechowych. Dlatego początek reumatyzmu z reguły poprzedza ból gardła, zaostrzenie przewlekłego zapalenia migdałków oraz zwiększona ilość antygenu paciorkowcowego i przeciwciał przeciw paciorkowcom (ASL-O, ASG, ASA, antydeoksyrybonukleaza B (anty-DNaza B)) są wykrywane we krwi chorych. Taki związek z wcześniejszą infekcją paciorkowcami jest szczególnie wyraźny w ostrym przebiegu reumatyzmu, któremu towarzyszy zapalenie wielostawowe. W rozwoju reumatyzmu rolę odgrywają czynniki wiekowe i społeczne (niekorzystne warunki życia, niedożywienie), ważna jest również predyspozycja genetyczna (reumatyzm jest chorobą dziedziczoną poligenicznie, dobrze wiadomo o istnieniu rodzin „reumatycznych”), która polega na odpowiedź hiperimmunologiczna na antygeny paciorkowców, skłonność pacjentów do procesów autoimmunologicznych i immunokompleksowych. Patogeneza. W przypadku reumatyzmu występuje złożona i zróżnicowana odpowiedź immunologiczna (natychmiastowe i opóźnione reakcje nadwrażliwości) na liczne antygeny paciorkowcowe. Kiedy infekcja dostanie się do organizmu, powstają przeciwciała przeciw paciorkowcom i kompleksy immunologiczne (antygeny paciorkowcowe + przeciwciała przeciwko nim + dopełniacz), które krążą we krwi i osadzają się w łożysku mikrokrążenia. Toksyny i enzymy paciorkowcowe mają również szkodliwy wpływ na mięsień sercowy i tkankę łączną. Ze względu na genetycznie uwarunkowany defekt układu odpornościowego, antygeny paciorkowców i kompleksy immunologiczne nie są całkowicie i szybko eliminowane z organizmu pacjentów. Tkanki takich pacjentów mają zwiększoną tendencję do utrwalania tych kompleksów immunologicznych. Nie bez znaczenia są tu również przeciwciała reagujące krzyżowo, które powstając na antygenach paciorkowcowych są w stanie reagować z antygenami tkankowymi, w tym sercowymi organizmu. W odpowiedzi zapalenie rozwija się na podłożu immunologicznym (w zależności od rodzaju nadwrażliwości natychmiastowej), natomiast czynnikami realizującymi proces zapalny są lizosomalne enzymy neutrofili, które fagocytują kompleksy immunologiczne i jednocześnie ulegają zniszczeniu. Ten proces zapalny jest zlokalizowany w tkance łącznej, głównie w układzie sercowo-naczyniowym, i zmienia jego właściwości antygenowe oraz mięsień sercowy. W rezultacie procesy autoimmunologiczne rozwijają się w zależności od rodzaju nadwrażliwości typu opóźnionego, a we krwi pacjentów znajdują się limfocyty reagujące z tkanką serca. Komórki te mają duże znaczenie w powstawaniu zmian narządowych (głównie serca). W tkance łącznej przy reumatyzmie zachodzą zmiany fazowe: obrzęk śluzowy – zmiany włóknikowate – martwica włóknikowata. Morfologiczną ekspresją zaburzeń immunologicznych są reakcje komórkowe - naciek limfocytów i plazmocytów, tworzenie się ziarniniaka reumatycznego lub ziarniniaka Ashoffa-Talalayevsky'ego. Proces patologiczny kończy się stwardnieniem. Innym morfologicznym podłożem uszkodzenia serca w chorobie reumatycznej serca jest nieswoista reakcja zapalna podobna do tej w stawach i błonach surowiczych: obrzęk tkanki łącznej międzymięśniowej, pocenie się fibryny, nacieki neutrofilami i limfocytami. Choroba przebiega falami, pogarsza się pod wpływem infekcji lub czynników niespecyficznych (hipotermia, stres fizyczny, stres itp.), Co jest związane z autoimmunologicznym charakterem procesu patologicznego. Kiedy serce jest uszkodzone, proces zapalny może rozprzestrzenić się na wszystkie błony serca (pancarditis) lub osobno na każdą z błon. Zmiany morfologiczne w reumatyzmie dotyczą przede wszystkim mięśnia sercowego, więc to zapalenie mięśnia sercowego we wczesnym stadium determinuje obraz kliniczny. Zmiany zapalne wsierdzia (zapalenie zastawek, brodawkowate zapalenie wsierdzia), uszkodzenie włókien ścięgien i pierścienia włóknistego są wykrywane klinicznie po 6-8 tygodniach od ataku reumatyzmu. Najczęściej dotyczy to zastawki mitralnej, a następnie zastawki aortalnej i trójdzielnej. Zastawka płucna w reumatyzmie prawie nigdy nie jest naruszona. Klasyfikacja reumatyczna. Obecnie przyjęto klasyfikację i nazewnictwo reumatyzmu, zatwierdzoną w 1990 r. przez Ogólnounijne Towarzystwo Naukowe Reumatologii, odzwierciedlającą fazę procesu, cechy kliniczne i anatomiczne uszkodzeń narządów i układów, charakter przebiegu oraz stan funkcjonalny układu sercowo-naczyniowego (patrz tabela 1). Obraz kliniczny. Wszystkie objawy choroby można podzielić na kardiologiczne i pozasercowe. Z tych pozycji można opisać obraz kliniczny choroby. Etap I: ujawnia się związek choroby z przeniesioną infekcją. W typowych przypadkach po 1-2 tygodniach od bólu gardła lub ostrej choroby układu oddechowego temperatura ciała wzrasta, czasem do 38-40 °C, z wahaniami w ciągu dnia w granicach 1-2 °C i silnym poceniem się (zwykle bez dreszczy). Przy powtarzających się napadach reumatyzmu często dochodzi do nawrotu choroby pod wpływem czynników niespecyficznych (takich jak hipotermia, przeciążenie fizyczne, zabieg chirurgiczny). Tabela 1 Klasyfikacja reumatyczna
Najczęstszym objawem reumatyzmu jest uszkodzenie serca - choroba reumatyczna serca: jednoczesne uszkodzenie mięśnia sercowego i wsierdzia. U dorosłych choroba reumatyczna serca nie jest ciężka. Pacjenci skarżą się na łagodny ból lub dyskomfort w okolicy serca, znacznie rzadziej występują lekkie duszności podczas ćwiczeń, przerwy lub kołatanie serca. Objawy te nie są specyficzne dla choroby reumatycznej serca i mogą być obserwowane w innych chorobach serca. Charakter takich skarg określany jest na kolejnych etapach poszukiwań diagnostycznych. Reumocarditis u młodych pacjentów z reguły jest ciężkie: od samego początku choroby obserwuje się ciężką duszność podczas ćwiczeń iw spoczynku, ciągły ból w sercu i kołatanie serca. Mogą wystąpić objawy niewydolności krążenia w dużym kręgu w postaci obrzęku i ciężkości w prawym podżebrzu (z powodu wzrostu wątroby). Wszystkie te objawy wskazują na ciężkie rozlane zapalenie mięśnia sercowego. Rzadko występuje zapalenie osierdzia, a także pozasercowe objawy reumatyzmu. Wraz z rozwojem suchego zapalenia osierdzia pacjenci odnotowują tylko stały ból w okolicy serca. W przypadku wysiękowego zapalenia osierdzia, charakteryzującego się nagromadzeniem surowiczo-włóknistego wysięku w worku sercowym, ból znika, ponieważ arkusze osierdzia w stanie zapalnym są oddzielone gromadzącym się wysiękiem. Pojawia się duszność, która nasila się wraz z pozycją poziomą pacjenta. Ze względu na trudności w dopływie krwi do prawego serca, przekrwienie pojawia się w dużym okręgu (obrzęk, ociężałość w prawym podżebrzu z powodu wzrostu wątroby). Najbardziej charakterystyczną cechą reumatyzmu jest porażka układu mięśniowo-szkieletowego w postaci reumatycznego zapalenia wielostawowego. Pacjenci zauważają szybko narastający ból w dużych stawach (kolano, łokieć, bark, kostka, nadgarstek), niemożność aktywnych ruchów, zwiększenie objętości stawów. Po zastosowaniu kwasu acetylosalicylowego i innych niesteroidowych leków przeciwzapalnych następuje szybki efekt z ulgą przez kilka dni, często kilka godzin wszystkich objawów stawowych. Zmiany reumatyczne nerek są również niezwykle rzadkie, wykrywane tylko w badaniu moczu. Zmiany układu nerwowego w reumatyzmie są rzadkie, głównie u dzieci. Skargi są podobne jak w przypadku zapalenia mózgu, zapalenia opon mózgowo-rdzeniowych, zapalenia naczyń mózgowych o innej etiologii. Na uwagę zasługuje jedynie „mała pląsawica”, która występuje u dzieci (częściej dziewczynek) i objawia się połączeniem chwiejności emocjonalnej i gwałtownej hiperkinezy tułowia, kończyn i mięśni mimicznych. Zespół brzuszny (zapalenie otrzewnej) występuje prawie wyłącznie u dzieci i młodzieży z ostrym reumatyzmem pierwotnym. Charakteryzuje się nagłym początkiem, gorączką i objawami dysfagii (występują rozlane lub miejscowe skurcze, nudności, wymioty, zatrzymanie lub częste stolce). W II etapie poszukiwań diagnostycznych wykrycie oznak uszkodzenia serca ma niewielkie znaczenie. W pierwotnej reumatycznej chorobie serca serce zwykle nie jest powiększone. Osłuchiwanie ujawnia stłumiony ton I, czasami pojawienie się tonu III, cichy szmer skurczowy na wierzchołku. Ta symptomatologia wynika ze zmian w mięśniu sercowym. Jednak wzrost natężenia, czasu trwania i utrzymywania się hałasu może wskazywać na powstawanie niewydolności zastawki mitralnej. Można śmiało ocenić powstawanie wady 6 miesięcy po rozpoczęciu ataku, zachowując powyższy obraz osłuchowy. W przypadku uszkodzenia zastawki aortalnej może być słyszalny szmer protorozkurczowy w punkcie Botkina, a dźwięczność tonu II może zostać zachowana. Dopiero wiele lat później, po powstaniu ciężkiej niewydolności zastawki aortalnej, do tego znaku osłuchowego dołącza osłabienie (lub brak) tonu II w II przestrzeni międzyżebrowej po prawej stronie. U pacjentów z zapaleniem wielostawowym obserwuje się deformację stawów z powodu zapalenia błony maziowej i tkanek okołostawowych, bólu przy palpacji stawu. W okolicy zajętych stawów mogą pojawić się guzki reumatyczne, które znajdują się na przedramionach i goleniach, powyżej wyniosłości kostnych. Są to niewielkie, gęste, bezbolesne nacieki, które znikają pod wpływem leczenia. Rumień pierścieniowy (znak prawie patognomoniczny dla reumatyzmu) to różowe elementy w kształcie pierścienia, nie swędzące, zlokalizowane na skórze wewnętrznej powierzchni rąk i nóg, brzucha, szyi i tułowia. Ten objaw jest niezwykle rzadki (u 1-2% pacjentów). Reumatyczne zapalenie płuc i zapalenie opłucnej mają te same objawy fizyczne, co podobne choroby o banalnej etiologii. Ogólnie zmiany pozasercowe są obecnie obserwowane niezwykle rzadko, u młodych osób z ostrym przebiegiem reumatyzmu (w obecności wysokiej aktywności - III stopień). Są nieostro wyrażone, szybko ulegają odwróceniu rozwoju podczas terapii przeciwreumatycznej. Na III etapie poszukiwań diagnostycznych dane z badań laboratoryjnych i instrumentalnych pozwalają nam ustalić aktywność procesu patologicznego i wyjaśnić uszkodzenie serca i innych narządów. Przy aktywnym procesie reumatycznym testy laboratoryjne ujawniają niespecyficzną fazę ostrą i zmienione parametry immunologiczne. Wskaźniki ostrej fazy: neutrofilia z przesunięciem formuły krwi leukocytów w lewo; wzrost zawartości 2-globulin, a następnie wzrost poziomu - globulin; wzrost zawartości fibrynogenu; pojawienie się białka C-reaktywnego; ESR wzrasta. W odniesieniu do parametrów immunologicznych wzrastają miana przeciwciał przeciwko paciorkowcom (anty-hialuronidaza i antystreptokinaza ponad 1:300, anty-O-streptolizyna ponad 1:250). EKG czasami ujawnia zaburzenia rytmu i przewodzenia: przejściowa blokada przedsionkowo-komorowa (częściej I stopień - wydłużenie odstępu P-Q, rzadziej - II stopień), dodatkowy skurcz, rytm przedsionkowo-komorowy. U wielu pacjentów rejestruje się spadek amplitudy załamka T aż do pojawienia się zębów ujemnych. Te zaburzenia rytmu i przewodzenia są niestabilne i szybko ustępują w trakcie terapii przeciwreumatycznej. Jeśli zmiany w EKG są trwałe i utrzymują się po wyeliminowaniu napadu reumatycznego, należy pomyśleć o organicznym uszkodzeniu mięśnia sercowego. Podczas badania fonokardiograficznego określa się dane osłuchowe: osłabienie I tonu, pojawienie się III tonu, szmer skurczowy. W przypadku powstania choroby serca na PCG pojawiają się zmiany, które odpowiadają naturze zmiany zastawkowej. Prześwietlenie przy pierwszym ataku reumatyzmu, nie wykryto żadnych zmian. Tylko w przypadku ciężkiej choroby reumatycznej serca u dzieci i młodzieży można wykryć wzrost serca z powodu poszerzenia lewej komory. Wraz z rozwojem choroby reumatycznej serca na tle istniejącej choroby serca, zdjęcie rentgenowskie będzie odpowiadać konkretnej wadzie. Badanie echokardiograficzne w pierwotnej chorobie reumatycznej serca nie ujawnia żadnych charakterystycznych zmian. Tylko w ciężkiej reumatycznej chorobie serca z objawami niewydolności serca na echokardiogramie widoczne są oznaki wskazujące na zmniejszenie kurczliwości mięśnia sercowego i rozszerzenie jam serca. diagnostyka. Rozpoznanie reumatyzmu pierwotnego jest bardzo trudne, gdyż jego najczęstsze objawy, takie jak zapalenie wielostawowe i uszkodzenie serca, są niespecyficzne. Obecnie najczęściej stosowane są główne i mniejsze kryteria reumatyzmu Amerykańskiego Towarzystwa Kardiologicznego. Kombinacja dwóch głównych lub jednego większego i dwóch mniejszych kryteriów wskazuje na większe prawdopodobieństwo wystąpienia reumatyzmu tylko w przypadku przebytej infekcji paciorkowcami. Wraz ze stopniowym początkiem reumatyzmu, diagnoza syndromiczna zaproponowana przez AI Niestierowa w 1973 r. (patrz Tabela 2) ma znaczenie: zespół kliniczny i epidemiologiczny (związek z zakażeniem paciorkowcami); zespół kliniczny i immunologiczny (objawy niepełnej rekonwalescencji, bóle stawów, podwyższone miana przeciwciał przeciwpaciorkowcowych, a także wykrycie dysproteinemii i wskaźników ostrej fazy); zespół sercowo-naczyniowy (wykrywanie zapalenia serca, a także zmian pozasercowych) (patrz Tabela 3). Tabela 2 Kryteria dla reumatyzmu
Tabela 3 Stopnie reumatyzmu
Diagnostyka różnicowa. Reumatyczne zapalenie wielostawowe należy odróżnić od niereumatycznego (patrz tabela 4). Tabela 4 Reumatyczne i niereumatyczne zapalenie wielostawowe
W związku z reumatyzmem podejrzewa się następujące choroby i objawy: 1) zapalenie wsierdzia; 2) zapalenie mięśnia sercowego; 3) zapalenie osierdzia; 4) wady serca; 5) zaburzenia rytmu i przewodzenia; 6) ostra i przewlekła niewydolność serca; 7) przedłużający się stan podgorączkowy; 8) rumień guzowaty; 9) rumień pierścieniowy; 10) guzki podskórne; 11) ostre alergiczne zapalenie wielostawowe; 12) pląsawica. Żaden z wymienionych powyżej zespołów klinicznych nie jest specyficzny dla tej choroby. Dopiero połączenie patologii serca z co najmniej jednym pozasercowym objawem głównym reumatyzmu daje podstawy do podejrzeń o reumatyzm. Samo rozpoznanie choroby reumatycznej serca odbywa się na podstawie objawów takich jak duszność i kołatanie serca, zmęczenie, ból serca i zaburzenia rytmu serca, odgłosy, czasami rytm galopu i osłabienie tonu I. Ogromne znaczenie w diagnostyce choroby reumatycznej serca ma identyfikacja patologii na EKG. W reumatyzmie powoduje zapalenie mięśnia sercowego, zapalenie osierdzia i wady serca. Obserwacja dynamiczna pozwala odróżnić nieodwracalne zmiany charakterystyczne dla przerostu różnych części serca w przypadku wad, od przejściowych, wskazujących na aktualny proces zapalny. Leczenie. Pozytywny efekt w leczeniu, a także zapobieganiu rozwojowi chorób serca, ułatwia wczesna diagnoza i indywidualne leczenie, które opiera się na ocenie rodzaju przebiegu, aktywności procesu patologicznego, ciężkości zapalenia serca, oraz wariant zastawkowej choroby serca. Ważny jest stan mięśnia sercowego, innych tkanek i narządów, zawód pacjenta itp. Tak więc cały kompleks leczenia reumatyzmu składa się z terapii przeciwdrobnoustrojowej i przeciwzapalnej, środków mających na celu przywrócenie homeostazy immunologicznej. Zaleca się stosowanie racjonalnej, zbilansowanej diety, skupienie się na adaptacji do aktywności fizycznej, przygotowanie do pracy, terminowe leczenie chirurgiczne pacjentów ze złożonymi wadami serca. Wszystkim pacjentom w aktywnej fazie reumatyzmu pokazano penicylinę (1 200 000-1 500 000 jm na 6 dawek dziennie, co 4 godziny), która ma działanie bakteriobójcze na wszystkie rodzaje paciorkowców A. Przebieg leczenia wynosi 2 tygodnie w aktywnej fazie reumatyzmu, w przyszłości wymagane jest przejście na przedłużoną bicylinę-5 (1 500 000 jednostek). W przypadku nietolerancji penicyliny można przepisać erytromycynę 250 mg 4 razy dziennie. Leki o działaniu przeciwzapalnym, które są stosowane w nowoczesnym leczeniu aktywnej fazy reumatyzmu, to glikokortykosteroidy, pochodne salicylowe, indolowe, pochodne kwasu fenylooctowego itp. Prednizolon stosuje się w dawce 20-30 mg dziennie (przez 2 tygodnie, następnie dawkę zmniejsza się o 2,5-5 mg co 5-7 dni, w sumie przez 1,5-2 miesiące) w przypadku pierwotnego i nawrotowego z III i II stopień aktywności procesu reumatycznej choroby serca, z zapaleniem błon surowiczych i pląsawicy, z rozwojem niewydolności serca w wyniku czynnego zapalenia serca. W tym ostatnim przypadku preferowany jest triamcynolon w dawce 12-16 mg dziennie, ponieważ ma on niewielką zdolność do zaburzenia równowagi elektrolitowej. Kortykoidy wpływają na metabolizm wodno-solny, dlatego w leczeniu należy stosować chlorek potasu 3-4 g/dobę, pananginę i inne, z zatrzymaniem płynów - antagoniści aldosteronu (weroszpiron do 6-8 tabletek dziennie), leki moczopędne (lasix). 40 -80 mg / dzień, furosemid 40-80 mg / dzień itp.), z euforią - środki uspokajające itp. Niesteroidowe leki przeciwzapalne są również szeroko stosowane w reumatyzmie: średnie dawki kwasu acetylosalicylowego wynoszą 3-4 g dziennie, rzadziej 5 g dziennie lub więcej. Wskazania do stosowania salicylanów: 1) minimalny stopień aktywności, niewielkie nasilenie zapalenia serca, głównie mięśnia sercowego; 2) długotrwałe leczenie reumatyzmu, podejrzenie utajonego przebiegu; 3) przedłużone leczenie ze spadkiem aktywności przebiegu procesu i zaprzestaniem stosowania kortykosteroidów, a także po zakończeniu leczenia w szpitalu; 4) nawracająca choroba reumatyczna serca występująca na tle ciężkich wad serca i niewydolności krążenia, ponieważ salicylany nie są w stanie zatrzymać płynów, zapobiegają tworzeniu się skrzepów krwi i są stymulantami ośrodka oddechowego; 5) zmniejszenie prawdopodobieństwa zaostrzenia reumatyzmu w okresie wiosennym i jesiennym, a także po przebytych współistniejących infekcjach (wraz z antybiotykami). Kwas acetylosalicylowy stosuje się 1 g 3-4 razy dziennie po posiłkach przez 1-3 miesiące lub dłużej z prawidłową tolerancją i pod warunkiem kontroli skutków ubocznych. Skuteczne stosowanie pochodnej kwasu indoloctowego - indometacyny w reumatyzmie od ponad 20 lat. Ma wyraźny efekt terapeutyczny: subiektywne objawy zapalenia serca (ból serca, kołatanie serca, duszność) znikają do 8-10 dnia terapii, a obiektywne objawy - do 14-16 dnia. Znikanie zapalenia wielostawowego i zapalenia błon surowiczych następuje jeszcze szybciej. W leczeniu reumatyzmu ważne jest połączenie trzech głównych etapów: szpital – klinika – uzdrowisko. W szpitalu leczenie odbywa się za pomocą leków wymienionych powyżej. Po zmniejszeniu aktywności reumatyzmu i normalizacji stanu chorego przechodzą do II etapu - leczenia w sanatorium reumatologicznym. Głównym celem tego etapu jest kontynuacja leczenia niesteroidowymi lekami przeciwzapalnymi, które są indywidualnie dobierane w szpitalu, pochodnymi aminochinoliny, bicyliną-5, rehabilitacją. Etap III obejmuje obserwację ambulatoryjną i leczenie profilaktyczne. Jest to wdrożenie środków terapeutycznych mających na celu ostateczną eliminację aktywnego przebiegu procesu reumatycznego; prowadzenie objawowego leczenia zaburzeń krążenia u pacjentów z chorobami serca; rozwiązywanie kwestii rehabilitacji, zdolności do pracy i zatrudnienia; wdrożenie profilaktyki pierwotnej reumatyzmu i wtórnej profilaktyki nawrotów choroby. WYKŁAD nr 2. Choroby układu sercowo-naczyniowego. Kardiomiopatia. Kardiomiopatia rozstrzeniowa 1. Kardiomiopatia Kardiomiopatia - pierwotne izolowane zmiany w mięśniu sercowym o charakterze niezapalnym o nieznanej etiologii (idiopatyczne), nie są związane z wadami zastawkowymi lub przeciekami wewnątrzsercowymi, nadciśnieniem tętniczym lub płucnym, chorobą wieńcową serca lub chorobami ogólnoustrojowymi (takimi jak: kolagenozy, amyloidoza, hemochromatoza, itp.), aw końcowej fazie choroby rozwija się ciężka zastoinowa niewydolność serca i złożone zaburzenia rytmu serca i drożności. Klasyfikacja kardiomiopatii jest następująca: 1) kardiomiopatia rozstrzeniowa: a) idiopatyczny; b) toksyczny; c) zakaźny; d) z kolagenozami; 2) przerostowe; 3) restrykcyjny; 4) dysplazja arytmiczna prawej komory; 5) połączenie jednego z 4 typów kardiomiopatii z nadciśnieniem tętniczym. 2. Kardiomiopatia rozstrzeniowa Kardiomiopatia rozstrzeniowa (DCM) to choroba mięśnia sercowego charakteryzująca się rozlanym rozszerzeniem wszystkich komór serca (głównie lewej komory), w której na pierwszy plan wysuwa się patologia funkcji pompowania serca, a w rezultacie , przewlekła niewydolność serca (stąd druga nazwa to zastoinowa, gdy serce nie jest w stanie w pełni pompować krwi i „zatrzymuje się” w tkankach i narządach organizmu). Mięśniowa ściana serca pozostaje niezmieniona lub przerośnięta w różnym stopniu. Choroby i czynniki poprzedzające rozwój DCM opisano w poniższej tabeli (patrz Tabela 5). Tabela 5 Choroby i czynniki poprzedzające rozwój DCMP
Jest to najczęstsza forma uszkodzenia mięśnia sercowego. Częstość występowania wynosi 5-8 przypadków na 100 000 osób rocznie. Nie ma jasnego wywiadu rodzinnego dla tych pacjentów. Mężczyźni chorują 2-3 razy częściej niż kobiety. Patogeneza. W wyniku procesu zapalnego w mięśniu sercowym (zapalenie mięśnia sercowego) następuje śmierć poszczególnych komórek w różnych jego częściach. W tym przypadku zapalenie ma charakter wirusowy, a komórki dotknięte wirusem stają się obcymi czynnikami dla organizmu. W związku z tym, gdy w organizmie pojawiają się antygeny, rozwija się zespół reakcji odpowiedzi immunologicznej, którego celem jest ich zniszczenie. Stopniowo martwe komórki mięśniowe są zastępowane tkanką łączną, która nie ma zdolności do rozciągliwości i kurczliwości właściwej mięśniowi sercowemu. W wyniku utraty podstawowych funkcji mięśnia sercowego serce traci zdolność do funkcjonowania jako pompa. W odpowiedzi na to (w reakcji kompensacyjnej) komory serca rozszerzają się (tj. rozszerzają), a w pozostałej części mięśnia sercowego następuje pogrubienie i zagęszczenie (tj. rozwija się jego przerost). Aby zwiększyć dostarczanie tlenu do narządów i tkanek organizmu, dochodzi do trwałego wzrostu częstości akcji serca (tachykardia zatokowa). Ta kompensacyjna odpowiedź tylko tymczasowo poprawia funkcję pompowania serca. Jednak możliwości rozszerzenia i przerostu mięśnia sercowego są ograniczone ilością żywotnego mięśnia sercowego i są indywidualne dla każdego konkretnego przypadku choroby. Wraz z przejściem procesu do etapu dekompensacji rozwija się przewlekła niewydolność serca. Jednak na tym etapie w grę wchodzi inny mechanizm kompensacyjny: tkanki ciała zwiększają pozyskiwanie tlenu z krwi w porównaniu ze zdrowym ciałem. Ale ten mechanizm jest niewystarczający, ponieważ zmniejszenie funkcji pompowania serca prowadzi do zmniejszenia dopływu tlenu do narządów i tkanek, co jest niezbędne do ich normalnego funkcjonowania, podczas gdy ilość w nich dwutlenku węgla wzrasta. U 2/3 pacjentów w jamach komór w późnych stadiach choroby tworzy się skrzeplina ciemieniowa (z powodu zmniejszenia funkcji pompowania serca, a także nierównomiernego skurczu mięśnia sercowego w komorach serca ), a następnie rozwój zatorowości w krążeniu płucnym lub ogólnoustrojowym. Zmiany patohistologiczne i patomorfologiczne w sercu. Kształt serca staje się kulisty, jego masa wzrasta od 500 do 1000 g, głównie za sprawą lewej komory. Mięsień sercowy staje się zwiotczały, matowy, z zauważalnymi białawymi warstwami tkanki łącznej, występuje charakterystyczna przemiana kardiomiocytów przerośniętych i zanikowych. Mikroskopowo wykrywa się rozlane zwłóknienie, można je łączyć zarówno z atrofią, jak i przerostem kardiomiocytów, w którym występuje znaczny wzrost objętości jąder, liczba mitochondriów, rozrost aparatu Golgiego, wzrost liczby miofibryli , wolny i związany z rybosomami retikulum endoplazmatycznego, obfitość granulek glikogenu. Obraz kliniczny. Nie ma specyficznych objawów choroby. Obraz kliniczny jest polimorficzny i zależy od: 1) objawy niewydolności serca; 2) zaburzenia rytmu i przewodzenia; 3) zespół zakrzepowo-zatorowy. Wszystkie te zjawiska rozwijają się w końcowym stadium choroby, dlatego rozpoznanie DCM przed pojawieniem się tych objawów nastręcza znaczne trudności. W większości przypadków rokowanie choroby zależy od porażki lewej komory serca. Przed wystąpieniem niewydolności serca DCM jest utajony. Najczęstszymi skargami na już rozpoczętą niewydolność serca są skargi na zmniejszoną wydajność, zwiększone zmęczenie, duszność podczas wysiłku, a następnie w spoczynku. W nocy ma suchy kaszel (odpowiednik astmy sercowej), później - typowe ataki astmy. Pacjenci zgłaszają się z charakterystycznym bólem dławicowym. Wraz z rozwojem przekrwienia w krążeniu ogólnoustrojowym pojawia się ciężkość w prawym podżebrzu (z powodu powiększonej wątroby), obrzęk nóg. diagnostyka. W rozpoznaniu choroby ważnym objawem jest znaczne powiększenie serca (nie ma cech wady zastawkowej serca ani nadciśnienia tętniczego). Kardiomegalia objawia się rozszerzeniem serca w obu kierunkach, określonym przez opukiwanie, a także przesunięciem impulsu wierzchołkowego w lewo i w dół. W ciężkich przypadkach słychać rytm galopowy, tachykardię i dźwięki względnej niewydolności zastawki mitralnej lub trójdzielnej. W 20% przypadków rozwija się migotanie przedsionków. Ciśnienie krwi jest zwykle prawidłowe lub nieznacznie podwyższone (z powodu niewydolności serca). Badania biochemiczne krwi i moczu mogą wykryć różne substancje toksyczne, a także niedobory witamin. Instrumentalne metody badawcze umożliwiają wykrycie: 1) oznaki kardiomegalii; 2) zmiany wskaźników hemodynamiki centralnej; 3) zaburzenia rytmu i przewodzenia. EKG nie wykazuje żadnych charakterystycznych zmian lub przesunięcia są niespecyficzne. Są to oznaki wzrostu wielkości serca, zaburzenia przewodzenia w postaci blokady przedniej gałęzi lewej nogi pęczka przedsionkowo-komorowego (wiązka His) lub całkowitej blokady lewej nogi (15% przypadków); a także uporczywy tachykardia zatokowa (częstość akcji serca często przekracza 100 uderzeń na minutę). Fonokardiogram potwierdza dane osłuchowe w postaci rytmu galopu, dość częste wykrywanie szmeru skurczowego (z powodu względnej niewydolności zastawki mitralnej lub trójdzielnej). Przy przekrwieniu w krążeniu płucnym ujawnia się akcent tonu II. Rentgen ujawnia znaczny wzrost komór (często w połączeniu z umiarkowanym wzrostem lewego przedsionka) i stagnację krwi w krążeniu płucnym (małym). Naruszenia w krążeniu płucnym objawiają się wzrostem układu naczyń płucnych, a także pojawieniem się przesięku w jamach opłucnowych, który powstaje z powodu zwiększonego ciśnienia w naczyniach płuc. Metoda echokardiografii jest jedną z głównych metod diagnozowania choroby. Echokardiografia pomaga wykryć poszerzenie obu komór, hipokinezę tylnej ściany lewej komory, paradoksalny ruch przegrody międzykomorowej podczas skurczu. Ponadto echokardiografia pozwala wyjaśnić wzrost amplitudy ruchu niezmienionych płatków zastawki mitralnej. Dodatkowe badania instrumentalne nie są obowiązkowe do postawienia diagnozy, ale ich wyniki pozwalają nam szczegółowo określić stopień zaburzeń hemodynamicznych i charakter zmian morfologicznych w mięśniu sercowym. Przeprowadzane jest badanie radioizotopowe serca (scyntygrafia mięśnia sercowego) w celu wyjaśnienia stanu funkcji pompowania serca, a także określenia stref martwego mięśnia sercowego. Badanie wskaźników hemodynamiki centralnej ujawnia niską objętość minutową i wyrzutową (wskaźniki minutowe i udarowe), wzrost ciśnienia w tętnicy płucnej. Angiokardiograficznie wykrywa się te same zmiany, co na echokardiogramie. Żywa biopsja mięśnia sercowego nie dostarcza informacji do określenia etiologii kardiomiopatii. W niektórych przypadkach w biopsji można wykryć antygen wirusowy lub wzrost zawartości LDH, a także zmniejszenie produkcji energii przez mitochondria. Jednak ta metoda chirurgiczna może być wykorzystana do wyjaśnienia etiologii choroby i dalszej terapii. Manipulację przeprowadza się w następujący sposób: w znieczuleniu miejscowym przebija się (nakłuwa się) dużą tętnicę i żyłę, następnie do serca podaje się specjalny instrument z małymi nożyczkami na końcu. Połączenie biopsji mięśnia sercowego z koronarografią (wstrzyknięcie środka kontrastowego do tętnic wieńcowych zaopatrujących serce) pozwala wykluczyć u chorego chorobę wieńcową jako jedną z chorób o objawach zbliżonych do DCM. Te dwa badania są przeprowadzane pod kontrolą telewizji rentgenowskiej. Diagnostyka różnicowa. Wykonuje się go przede wszystkim przy zapaleniu mięśnia sercowego i dystrofiach mięśnia sercowego, czyli przy tych stanach, które czasami bezzasadnie nazywane są kardiomiopatiami wtórnymi. Biopsja mięśnia sercowego zapewnia znaczną pomoc w diagnostyce różnicowej kardiomiopatii rozstrzeniowej i choroby serca, występującej z wyraźnym jej wzrostem: 1) z ciężkim rozlanym zapaleniem mięśnia sercowego stwierdza się naciek komórkowy zrębu w połączeniu ze zmianami dystroficznymi i martwiczymi w kardiomiocytach; 2) z pierwotną amyloidozą występującą z uszkodzeniem serca (tzw. kardiopatyczny wariant pierwotnej amyloidozy) występuje znaczne odkładanie amyloidu w tkance śródmiąższowej mięśnia sercowego połączone z atrofią włókien mięśniowych; 3) z hemochromatozą (choroba spowodowana naruszeniem metabolizmu żelaza), w mięśniu sercowym znajdują się złogi pigmentu zawierającego żelazo, obserwuje się różne stopnie dystrofii i atrofii włókien mięśniowych oraz proliferację tkanki łącznej. Jako wariant DCM można rozważyć kardiomiopatie polekowe i toksyczne. Liczne środki mogą powodować toksyczne uszkodzenie mięśnia sercowego: etanol, emetyna, lit, kadm, kobalt, arsen, izoproterenol i inne trucizny. Zmiany histopatologiczne w tkankach mięśnia sercowego objawiają się jako ogniskowe dystrofie. W przyszłości następuje rozwój mikrozawałów, któremu towarzyszy obwodowa reakcja zapalna. Najbardziej uderzającym przykładem kardiomiopatii toksycznej jest kardiomiopatia, która występuje u osób nadużywających piwa. Wynika to z obecności w nim kobaltu, który dodaje się do piwa w celu poprawy piany. Kobalt blokuje działanie witaminy B1, a także bezpośrednio wpływa na zmianę procesów enzymatycznych komórki. W ostrej fazie przebiegu kardiomiopatii kobaltowej stwierdza się obecność zwyrodnienia wodniakowatego i tłuszczowego, zniszczenie organelli wewnątrzkomórkowych i ogniskową martwicę kardiomiocytów. W przyszłości rozwija się rozlane lub drobnoogniskowe zwłóknienie śródmiąższowe, końcowym efektem jest powstawanie rozległych blizn. Kardiomiopatia kobaltowa jest cięższa niż kardiomiopatia alkoholowa. Jeśli diagnoza zostanie postawiona na czas, obserwuje się kliniczne wyleczenie pacjentów. Kardiomiopatia alkoholowa. Etanol ma bezpośredni toksyczny wpływ na kardiomiocyty. Ponadto przy przewlekłym zatruciu etylem często brakuje odżywiania. Udowodniono, że alkohol prowadzi do komutacji kwasów tłuszczowych w kardiomiocytach, ponieważ brakuje energii niezbędnej do ich działania. Aldehyd octowy, który powstaje podczas metabolizmu alkoholu, może być czynnikiem bezpośredniego toksycznego wpływu na syntezę białek. Alkoholizmowi towarzyszy również aktywacja utajonych wirusów. Makroskopowo mięsień sercowy jest zwiotczały, glinopodobny, czasami widoczne są niewielkie blizny. Tętnice wieńcowe są nienaruszone. Badanie mikroskopowe wykazuje kombinację dystrofii (obwodu i tkanki tłuszczowej), atrofii i przerostu kardiomiocytów, mogą występować ogniska rozpadu kardiomiocytów i miażdżycy. Dotknięte obszary mięśnia sercowego kontrastują z niezmienionymi. Badanie pod mikroskopem elektronowym wycinków z biopsji serca wykazuje torbielowate rozszerzenie siateczki sarkoplazmatycznej i układu T kardiomiocytów, co jest charakterystyczne dla kardiomiopatii alkoholowej. Powikłania kardiomiopatii alkoholowej - nagła śmierć w wyniku migotania komór lub przewlekłej niewydolności serca, zespół zakrzepowo-zatorowy. Leczenie. Terapia kardiomiopatii jest zadaniem trudnym, gdyż nie są znane konkretne przyczyny ich występowania. Ogólne zasady leczenia DCM nie różnią się istotnie od leczenia przewlekłej niewydolności serca. W przypadku wtórnej DCM leczy się dodatkowo wcześniej przebytą chorobę (choroba zastawki serca itp.) i podejmuje się wszelkie działania mające na celu wyeliminowanie przyczyn DCM. Zasadniczo o leczeniu pacjentów z kardiomiopatią możemy mówić tylko wtedy, gdy pojawiają się objawy kliniczne. W niewydolności serca glikozydy nasercowe są nieskuteczne. Pacjenci szybko rozwijają nietolerancję na leki (zatrucie glikozydami), dlatego konieczne jest stosowanie glikozydów, które są szybko wydalane z organizmu (strofantyna, izolanid). Środki rozszerzające naczynia obwodowe są dość skuteczne, szczególnie w przypadku współistniejącego zespołu dławicowego (nitrong, sustak, nitrosorbid). Leki te powinny być przepisywane w przypadku ciężkiej niewydolności serca, trudnej do leczenia glikozydami i lekami moczopędnymi. W przypadku zespołu dusznicy bolesnej konieczne staje się stosowanie leków przeciwdławicowych, najlepiej przedłużonych azotanów (sustak, nitrong, nitrosorbid). Adrenoblockery są skuteczne (są przepisywane w przypadku braku objawów niewydolności serca). Spośród nowoczesnych metod chirurgicznego leczenia DCMP najskuteczniejszą jest przeszczep serca (transplantacja). Jednak możliwości przeprowadzenia tej operacji są znacznie ograniczone. Z tego powodu, jako alternatywę dla przeszczepu serca w nowoczesnym leczeniu, aby wydłużyć długość życia pacjentów z DCMP, opracowano i wykonuje się operacje rekonstrukcyjne, które mają na celu wyeliminowanie niewydolności zastawki mitralnej i trójdzielnej. Operacyjna eliminacja niewydolności tych zastawek pozwala na pewien czas „spowolnić” początek końcowego stadium choroby. Inną alternatywą dla przeszczepu serca u chorych z DCM było częściowe usunięcie lewej komory w celu zmniejszenia jej rozmiaru (operacja Baptiste). Nie tak dawno temu, do leczenia pacjentów z DCMP, opracowano specjalne modele rozruszników serca, które pozwalają na synchroniczną pracę komór serca. Prowadzi to do poprawy wypełnienia komór serca krwią i zwiększenia funkcji pompowania serca. Odrębną kwestię należy uznać za DCM u dzieci, która wynosi 5-10 przypadków na 100 000 dzieci rocznie. Warto zauważyć, że choroba może rozwijać się w różnych grupach wiekowych, w tym także u niemowląt. Dane uzyskane w badaniu grupy dzieci przedstawiają się następująco: pacjenci otrzymali 3 opcje leczenia (monoterapia prednizolonem, monoterapia digoksyną lub prednizolon + digoksyna). Skuteczność leczenia oceniano według następujących kryteriów: określano częstość akcji serca przed i po leczeniu, częstość oddechów, stan frakcji wyrzutowej i frakcji kurczliwości. Analiza uzyskanych wyników wskazuje, że największy efekt w leczeniu kardiomiopatii rozstrzeniowej u małych dzieci uzyskuje się przy zastosowaniu kombinacji kortykosteroidów i glikozydów (prednizolonu i digoksyny). Po zakończeniu głównego cyklu leczenia (prednizolon podawany 2 mg/kg dziennie przez 28 dni, digoksyna) nastąpiło wyraźne zmniejszenie częstości akcji serca, zmniejszenie duszności. Na tle monoterapii prednizolonem następuje zmniejszenie częstości akcji serca. Monoterapia digoksyną prowadzi do zmniejszenia częstoskurczu i duszności. Biorąc pod uwagę niewskazanie przepisywania leków cytostatycznych u małych dzieci, ponieważ zaobserwowano znaczną liczbę powikłań leczenia, w pediatrii bardziej optymalne jest stosowanie długo działających glikozydów nasercowych w połączeniu z hormonami kortykosteroidowymi w kardiomiopatii rozstrzeniowej. profilaktyka. Zapobieganie DCM polega na unikaniu alkoholu, kokainy i dokładnym monitorowaniu parametrów serca podczas chemioterapii nowotworu. Przydaje się hartowanie ciała od najmłodszych lat. Całkowita abstynencja od alkoholu w alkoholowej DCM poprawia kurczliwość serca i może wyeliminować konieczność przeszczepu serca. Fakt, że w większości przypadków diagnoza pojawia się na etapie niewydolności serca, może również prowadzić do negatywnych wyników leczenia. Wczesną diagnostykę kardiomiopatii rozstrzeniowej można przeprowadzić za pomocą wyrywkowej (przesiewowej) echokardiografii, która jest wykonywana podczas corocznego badania lekarskiego, a także przy badaniu osób z dziedzicznością obciążoną tą chorobą. W tym przypadku możliwe jest zwiększenie skuteczności leczenia farmakologicznego DCM. WYKŁAD nr 3. Choroby układu sercowo-naczyniowego. Kardiomiopatia przerostowa Kardiomiopatia przerostowa (HCM) to niewieńcowa choroba mięśnia sercowego komór (głównie lewej), charakteryzująca się masywnym przerostem ich ścian z występem przegrody międzykomorowej (IVS) do jamy prawej komory, która może ulec znacznemu pogrubieniu , zmniejszenie objętości wewnętrznej komór, prawidłowa lub zwiększona kurczliwość mięśnia sercowego i upośledzona relaksacja (dysfunkcja rozkurczowa). Najczęściej występuje izolowany przerost przegrody międzykomorowej (izolowane przerostowe zwężenie podaortalne – IHSS) lub części wierzchołkowej komór. Klasyfikacja. Klasyfikacja HCM według lokalizacji przerostu (ED Wigle i in., 1985 z dodatkami). I. Przerost LV. 1) Przerost asymetryczny, w którym występuje przerost mięśnia sercowego poszczególnych ścian lub odcinków komór (w tym przerost IVS - 90% z lub bez niedrożności drogi odpływu lewej komory, śródkomorowej - 1%, przerost wierzchołkowy lewej komory - 3%, przerost wolnej ściany lewej komory i tylna część IVS - 1%). 2) Symetryczny (koncentryczny) przerost lewej komory, gdy przerost mięśnia sercowego rozciąga się na wszystkie ściany komór, występuje w 5% przypadków. II. Przerost trzustki. W przypadku, gdy przerost mięśnia sercowego uniemożliwia prawidłowy odpływ krwi z komór serca, mówi się o obturacyjnej postaci HCM. W innych przypadkach HCM nie przeszkadza. Etiologia. Choroba może być wrodzona lub nabyta. Wrodzony HCM jest dziedziczony w sposób autosomalny dominujący. W obrębie tej samej rodziny można zaobserwować różne formy i warianty HCM. Najczęściej dziedziczony jest asymetryczny przerost przegrody międzykomorowej. Nabyta postać HCM występuje u starszych pacjentów z nadciśnieniem tętniczym w wywiadzie. Częstość występowania wynosi 0,02-0,05%. Przyczyny rozwoju przejętego HCM nie są w pełni zrozumiałe. Zgodnie z jedną z zaproponowanych hipotez, u osób z nabytym HCM w okresie prenatalnym rozwija się defekt receptorów adrenergicznych serca zaangażowanych w regulację czynności serca, w szczególności częstości akcji serca. W efekcie znacząco wzrasta wrażliwość na noradrenalinę i podobne hormony, które zwiększają częstość akcji serca, co wpływa na rozwój u nich przerostu mięśnia sercowego, a ostatecznie HCM. Obraz patohistologiczny. Zdezorientowany, nieprawidłowy, chaotyczny układ kardiomiocytów i miofibryli w kardiomiocytach, zwłóknienie mięśnia sercowego stanowi naruszenie architektury mięśnia sercowego. Patogeneza. Zaburzenia hemodynamiczne powstają w wyniku upośledzenia funkcji rozkurczowej serca. Podczas rozkurczu do komór (zwłaszcza lewej) napływa niewystarczająca ilość krwi ze względu na ich gęstość i sztywność, co prowadzi do szybkiego wzrostu ciśnienia końcoworozkurczowego. Zarówno zwiększona sztywność mięśnia sercowego, jak i zwiększone ciśnienie wewnątrzkomorowe powodują, że podczas skurczu z komory wyrzucana jest mniejsza ilość krwi. Aby zapewnić odpowiednie dostarczanie tlenu do narządów i tkanek ciała (przy normalnym funkcjonowaniu układu sercowo-naczyniowego), w celu wykonania dowolnego obciążenia, uwalnianie krwi z serca musi wzrosnąć. W związku z tym w odpowiedzi na obciążenie wzrasta częstość akcji serca. Wraz z rozwojem HCM, wypełnienie serca krwią cierpi również w spoczynku, a wraz ze wzrostem częstości akcji serca w okresie ćwiczeń, ma to jeszcze większy negatywny wpływ. W wyniku tego nie następuje odpowiedni wzrost funkcji pompowania serca podczas ćwiczeń w HCM. Aktywność fizyczna w HCM wpływa na wzrost ciśnienia śródkomorowego, co prowadzi do wzrostu ciśnienia w lewym przedsionku położonym powyżej, a także w naczyniach małego (płucnego) krążenia. W tych warunkach rozwija się nadczynność i przerost lewego przedsionka, a później nadciśnienie płucne („bierne”). W rezultacie pojawia się duszność, która jest proporcjonalna do stopnia obciążenia. Ponieważ podczas ćwiczeń wyrzut krwi z lewej komory nie odpowiada wzrostowi obciążenia, przepływ krwi w tętnicach wieńcowych, które zasilają sam mięsień sercowy, zaczyna cierpieć. Istotną rolę odgrywa również to, że w HCM występuje rozbieżność między znaczną masą przerośniętego mięśnia sercowego a możliwością ukrwienia naczyń wieńcowych, która pozostaje taka sama jak u osób zdrowych. Zmniejszenie przepływu krwi przez tętnice wieńcowe prowadzi do wystąpienia dławicy piersiowej w środkowej i lewej połowie klatki piersiowej, promieniującej do lewego ramienia, pod lewą łopatką. Podobnie jak duszność, dusznica bolesna jest wywoływana przez wysiłek fizyczny. W niektórych przypadkach HCM podczas ćwiczeń pogarsza się również dopływ krwi do mózgu, powodując omdlenia. Należy zauważyć, że w celu zmniejszenia wzrostu ciśnienia śródkomorowego podczas ćwiczeń istnieje mechanizm kompensacyjny, którego działanie opiera się na fakcie, że wnęka lewego przedsionka rozszerza się, a grubość jego ścian wzrasta. W rezultacie podczas ćwiczeń dochodzi do dodatkowego wypełnienia lewej komory krwią. Jest to jednak tylko chwilowa kompensacja z uwagi na fakt, że rezerwa lewego przedsionka jako „pompy” jest znikoma, a znaczne poszerzenie jamy lewego przedsionka prowadzi do rozwoju migotania przedsionków. Obraz kliniczny. HCM charakteryzuje się ogromną różnorodnością objawów, co powoduje błędną diagnozę. Obecność i moment wystąpienia dolegliwości w HCM zależą głównie od 2 czynników: postaci HCM i lokalizacji zmiany. Najpotężniejszą komorą serca jest lewa komora, dlatego przy przeroście ścian mięśnia sercowego dolegliwości mogą nie pojawiać się przez długi czas. Izolowane uszkodzenie prawej komory serca zdarza się niezwykle rzadko. W nieobturacyjnej postaci HCM, gdy nic nie zakłóca odpływu krwi z komory, pacjent może nie zgłaszać dolegliwości. Czasami może wystąpić duszność (przy znacznym wysiłku fizycznym), przerwy w pracy serca, a także nieregularne bicie serca. W obturacyjnej postaci HCM wyrzut krwi z serca podczas wysiłku jest znacznie zmniejszony ze względu na obecność utrudnienia odpływu krwi z komory. W tym przypadku typowe dolegliwości to duszność podczas wysiłku, dusznica bolesna i omdlenia. Choroba charakteryzuje się powolnym postępem dolegliwości od momentu jej wystąpienia. Ze względu na podobieństwo dolegliwości (ból w okolicy serca i za mostkiem) oraz dane z badań (intensywny szmer skurczowy) najczęściej błędnie rozpoznaje się chorobę reumatyczną serca i chorobę wieńcową. Obraz kliniczny HCM to: 1) oznaki przerostu mięśnia sercowego komorowego (głównie lewego); 2) oznaka niewystarczającej funkcji rozkurczowej komór; 3) zmienne oznaki niedrożności drogi odpływu lewej komory. diagnostyka. W procesie poszukiwań diagnostycznych najważniejsze jest wykrycie szmeru skurczowego, zmienionego tętna i przemieszczonego impulsu wierzchołkowego. Obraz osłuchowy serca u pacjentów z obturacyjnym HCM ma szereg cech: maksymalny dźwięk szmeru skurczowego (szmer wyrzutowy) określa się w punkcie Botkina i na wierzchołku serca, nasilenie szmeru jest proporcjonalne do stopień niedrożności, jej nasilenie następuje przy gwałtownym wstaniu, a także podczas próby Valsalvy; II ton jest zawsze zachowany; hałas nie jest wykonywany na naczyniach szyi. Puls jest zwykle wysoki i szybki. Wynika to z braku zwężenia dróg odpływowych z lewej komory na początku skurczu, ale potem, przy skurczu potężnych mięśni, pojawia się „funkcjonalne” zwężenie dróg odpływowych, w wyniku którego puls fala zmniejsza się przedwcześnie. Uderzenie wierzchołkowe w około 1/3 przypadków ma charakter „podwójny”: najpierw przy badaniu palpacyjnym odczuwa się uderzenie od skurczu lewego przedsionka, następnie od skurczu lewej komory. Dla wygody identyfikacji tej właściwości uderzenia wierzchołka najlepiej wykonywać badanie palpacyjne, gdy pacjent leży na lewym boku. W diagnostyce HCM największe znaczenie mają dane echokardiograficzne, pozwalające wyjaśnić anatomiczne cechy choroby, nasilenie przerostu mięśnia sercowego, niedrożność drogi odpływu lewej komory. Ujawniają się następujące objawy: asymetryczny przerost IVS, wyraźniejszy w górnej jednej trzeciej, jego hipokineza; skurczowy ruch przedniego płatka zastawki mitralnej w kierunku przednim; kontakt przedniego płatka zastawki mitralnej z IVS w rozkurczu. Niespecyficzne objawy to: przerost lewego przedsionka, przerost tylnej ściany lewej komory, zmniejszenie średniej prędkości rozkurczowej osłony przedniego płatka zastawki mitralnej. Na EKG wszelkie specyficzne zmiany znajdują się tylko przy wystarczająco rozwiniętym przeroście lewej komory. Rejestrując EKG przez 24 godziny (monitorowanie metodą Holtera), wykrywane są istniejące zaburzenia rytmu serca. Badanie EKG z dozowaną aktywnością fizyczną przy użyciu ergometru rowerowego lub bieżni rowerowej pozwala ocenić nasilenie objawów choroby, jej rokowanie oraz opracować odpowiednie leczenie. Izolowany przerost IVS powoduje wzrost amplitudy załamka Q w lewych odprowadzeniach klatki piersiowej (V5-6), co komplikuje diagnostykę różnicową ze zmianami ogniskowymi spowodowanymi zawałem mięśnia sercowego. Jednak niewielka szerokość załamka Q pozwala wykluczyć zawał mięśnia sercowego.W procesie rozwoju przeciążenia hemodynamicznego lewego przedsionka EKG może wykazywać oznaki przerostu lewego przedsionka: poszerzenie załamka P o ponad 0,10 s, wzrost w swojej amplitudzie pojawienie się dwufazowej fali P w odprowadzeniu V1 z drugą fazą o zwiększonej amplitudzie i czasie trwania. Diagnostyka rentgenowska ma znaczenie dopiero w zaawansowanym stadium choroby, kiedy można stwierdzić wzrost lewej komory i lewego przedsionka, poszerzenie zstępującej części aorty. Na fonokardiogramie zachowane są amplitudy tonów I i II, co jest znakiem różnicowym HCM od zwężenia ujścia aorty, a także wykrywany jest szmer skurczowy o różnym nasileniu. Inwazyjne metody badawcze (sondowanie lewej części serca, angiografia kontrastowa) nie są obecnie obowiązkowe, ponieważ echokardiografia dostarcza informacji, które są dość wiarygodne do postawienia diagnozy. Czasami jednak metody te są wykorzystywane w kontrowersyjnych przypadkach w celu wyjaśnienia diagnozy lub przygotowania pacjentów do operacji. Sondowanie serca jest stosowane pod kontrolą telewizji rentgenowskiej. Technika wykonania metody: poprzez nakłucie dużej tętnicy w znieczuleniu miejscowym z dalszym wprowadzeniem specjalnego cewnika do jamy serca mierzy się gradient ciśnienia (różnicę) między lewą komorą a wychodzącą z niej aortą. Zwykle ten gradient nie powinien być. Jednak w przypadku HCM różnica ciśnień między lewą komorą a aortą wynosi od 50 do 150 mm Hg. Art., wzrost ciśnienia końcoworozkurczowego w jamie lewej komory do 18 mm Hg. Sztuka. Gradient ciśnienia zmniejsza się po wprowadzeniu β-blokerów. Ponadto podczas sondowania serca do jamy komory wstrzykuje się środek kontrastowy (wentrykulografia), aby zbadać jego cechy anatomiczne. U wielu pacjentów (z reguły są to osoby powyżej 40 roku życia) przed operacją serca stosuje się jednocześnie angiografię tętnic wieńcowych (angiografia wieńcowa) w celu wyjaśnienia etiologii dławicy piersiowej i wykluczenia współistniejącej choroby wieńcowej. Leczenie. Podstawą farmakoterapii HCM są leki poprawiające dopływ krwi do komór serca w rozkurczu. Leki te to grupa β-blokerów (anaprilin, atenolol, metoprolol i propranolol, 160-320 mg/dzień itp.) oraz grupa antagonistów jonów wapnia (werapamil, ale z zachowaniem ostrożności). Nowokinamid i dyzopiramid również zmniejszają częstość akcji serca i działają przeciwarytmicznie. Na samym początku leczenia stosuje się małe dawki tych leków, następnie stopniowo zwiększa się dawkę do maksymalnej tolerowanej przez pacjenta. Beta-blokery stosuje się ostrożnie w cukrzycy, astmie oskrzelowej i niektórych innych chorobach. Podczas leczenia tymi lekami konieczne jest stałe monitorowanie ciśnienia krwi i tętna. Niebezpieczny jest spadek ciśnienia poniżej 90/60 mm Hg. Sztuka. i tętno poniżej 55 na minutę. Jeśli pacjent ma niebezpieczne arytmie, których nie można leczyć β-blokerami lub antagonistami jonów wapnia, w leczeniu takich pacjentów dodatkowo stosuje się inne leki antyarytmiczne. Powołanie antykoagulantów jest zalecane w przypadku napadowych arytmii i migotania przedsionków, a także w obecności zakrzepów krwi w komorach serca (warfaryna itp.). W okresie leczenia tymi lekami konieczne jest regularne monitorowanie szeregu wskaźników układu krzepnięcia krwi. Przy znacznym przedawkowaniu leków przeciwzakrzepowych możliwe jest krwawienie zewnętrzne (nosowe, maciczne itp.) I wewnętrzne (krwiaki itp.). Leczenie chirurgiczne wykonuje się u pacjentów z obturacyjnym HCM, gdy leczenie zachowawcze jest nieskuteczne lub gdy gradient między lewą komorą a aortą przekracza 30 mm Hg. Sztuka. (wykonuje się operację miotomii lub myektomii - wycięcie lub usunięcie części przerośniętego mięśnia sercowego lewej komory). Wykonywana jest również wymiana zastawki mitralnej i niechirurgiczna ablacja IVS. profilaktyka. U wszystkich chorych na HCM, zwłaszcza w postaci obturacyjnej, przeciwwskazane jest uprawianie sportów, które w krótkim czasie mogą znacznie zwiększyć aktywność fizyczną (lekkoatletyka, piłka nożna, hokej). Zapobieganie chorobie polega na wczesnej diagnostyce, która pozwala na wczesne rozpoczęcie leczenia choroby i zapobieganie rozwojowi ciężkiego przerostu mięśnia sercowego. Obowiązkowe jest wykonanie echokardiografii u genetycznych krewnych pacjenta. W diagnostyce ważne są także badania przesiewowe EKG i EchoCG, które przeprowadza się podczas corocznego badania lekarskiego. U pacjentów z obturacyjną postacią HCM konieczne jest zapobieganie infekcyjnemu zapaleniu wsierdzia (profilaktyka antybiotykowa itp.), Ponieważ obecność niedrożności stwarza warunki do rozwoju tego stanu zagrażającego życiu. WYKŁAD nr 4. Choroby układu krążenia. Kardiomiopatia restrykcyjna Kardiomiopatia restrykcyjna (RCMP) - (z łac. restrykcja - "restrykcja") - grupa schorzeń mięśnia sercowego i wsierdzia, w których w wyniku wyraźnego zwłóknienia i utraty elastyczności, z różnych przyczyn, występuje stałe ograniczenie wypełnienia komór w rozkurczu. Wypełnianie komór odbywa się w fazie wczesnego napełniania, po której następuje stabilizacja ciśnienia śródkomorowego. Chorobie towarzyszy niedostateczny dopływ krwi do serca, co dalej prowadzi do rozwoju przewlekłej niewydolności serca. Kardiomiopatia restrykcyjna jest najmniej zbadaną i najrzadziej powszechną spośród wszystkich kardiomiopatii. RCMP obejmuje: ciemieniowe włókniste zapalenie wsierdzia Leflera (występujące w krajach o klimacie umiarkowanym, opisane przez W. Lofflera i in., 1936) oraz zwłóknienie endomiokardialne (występujące w krajach tropikalnej Afryki, opisane przez D. Bedforda i E. Konstmana). Wcześniej uważano je za dwa niezależne procesy patologiczne. Jednak obraz patomorfologiczny w tych chorobach niewiele się różni. Przyczyny RCM. Pierwotny RCM występuje bardzo rzadko, a jedyną udowodnioną przyczyną jego występowania jest tzw. zespół hipereozynofilowy (choroba Lefflera, ciemieniowe włókniste zapalenie wsierdzia Lefflera). Występuje głównie u mężczyzn w wieku 30-40 lat. W przypadku zespołu hipereozynofilowego dochodzi do zapalenia wsierdzia, które z czasem kończy się znacznym zagęszczeniem wsierdzia i jego szorstkim przyleganiem do sąsiedniego mięśnia sercowego, co prowadzi do gwałtownego zmniejszenia rozciągliwości mięśnia sercowego. Zespół Leflera charakteryzuje się także utrzymującą się eozynofilią utrzymującą się przez 6 miesięcy lub dłużej (1500 eozynofili na 1 mm3), uszkodzenia narządów wewnętrznych (wątroby, nerek, płuc, szpiku kostnego). W zdecydowanej większości przypadków pochodzenie RCMP jest drugorzędne z innych powodów, wśród których najczęstsze to: 1) amyloidoza - choroba związana z naruszeniem metabolizmu białek w organizmie; jednocześnie powstaje nieprawidłowe białko (amyloid) i odkłada się w dużych ilościach w tkankach różnych narządów; gdy serce jest uszkodzone, amyloid powoduje zmniejszenie jego kurczliwości i rozciągliwości; 2) hemochromatoza - naruszenie metabolizmu żelaza w organizmie, któremu towarzyszy zwiększona zawartość żelaza we krwi, jego nadmiar odkłada się w wielu narządach i tkankach, w tym w mięśniu sercowym, powodując w ten sposób zmniejszenie jego rozciągliwości; 3) sarkoidoza – choroba o nieznanej etiologii, charakteryzująca się tworzeniem skupisk komórek (ziarniniaków) w narządach i tkankach; najczęściej dotknięte są płuca, wątroba, węzły chłonne i śledziona; a rozwijające się ziarniniaki w mięśniu sercowym prowadzą do zmniejszenia jego rozciągliwości; 4) choroby wsierdzia (zwłóknienie wsierdzia, fibroelastoza wsierdzia itp.), Gdy występuje znaczne pogrubienie i zagęszczenie wsierdzia, co również prowadzi do ostrego ograniczenia rozciągliwości mięśnia sercowego. W szczególności fibroelastoza wsierdzia może wystąpić tylko u niemowląt; ta choroba nie jest kompatybilna z życiem ze względu na wczesny rozwój ciężkiej niewydolności serca. Patogeneza. W przypadku RCM podatność mięśnia sercowego jest gorsza z różnych powodów. W rezultacie zmniejsza się napełnienie komór krwią i znacznie wzrasta ciśnienie wewnątrzkomorowe. Jednak w przeciwieństwie do HCM ryzyko wystąpienia kompensacyjnego przerostu mięśnia sercowego w kardiomiopatii restrykcyjnej jest niewielkie. Tak więc po pewnym czasie następuje stagnacja w krążeniu płucnym i zmniejsza się funkcja pompowania serca, co prowadzi do stopniowego zatrzymywania płynów w organizmie, rozwoju uporczywego obrzęku nóg, powiększenia wątroby i wodobrzusza. Jeśli zagęszczenie wsierdzia rozciąga się na zastawki przedsionkowo-komorowe (mitralna i trójdzielna), pogarsza się to z powodu rozwoju ich niewydolności, a także prowadzi do zakrzepicy w jamach serca z powodu ich zmniejszonej kurczliwości i rozciągliwości. Rozprzestrzenianie się fragmentów tych skrzepów krwi z krwiobiegu może powodować choroby zakrzepowo-zatorowe i blokadę dużych naczyń, zawał serca narządów wewnętrznych. Wraz z rozprzestrzenianiem się patologicznych wtrąceń mięśnia sercowego do strefy układu przewodzącego serca mogą pojawić się różne zaburzenia przewodzenia impulsu sercowego, którym towarzyszy rozwój blokad. W przypadku RCMP dość często obserwuje się również różne rodzaje arytmii. Na podstawie powyższego możemy stwierdzić, że choroba z patogenetycznego punktu widzenia przebiega w 3 etapach. Etap I - martwiczo - eozynofilowy naciek mięśnia sercowego i innych narządów. Etap II - zakrzepowy - tworzenie się skrzepów krwi w jamach lewej i prawej komory, rozwój powikłań zakrzepowo-zatorowych i stopniowe pogrubienie wsierdzia głównie w okolicach wierzchołkowych i w pobliżu zastawek przedsionkowo-komorowych. Etap III - włóknisty, charakteryzujący się pogrubieniem wsierdzia do kilku milimetrów, wyraża się zwłóknienie mięśnia sercowego - głównie obszary podwsierdziowe. Jama jest częściowo obliterowana z powodu zorganizowanych skrzeplin, obserwuje się zwłóknienie guzków zastawki mitralnej, niedomykalność zastawki mitralnej. Wyraźne rozszerzenie przedsionków. Obserwuje się restrykcyjną dysfunkcję rozkurczową. Obraz kliniczny. Objawy choroby są niezwykle wielopostaciowe i określane są objawami zaburzeń krążenia w małym lub dużym kole (w zależności od dominującego uszkodzenia prawej lub lewej komory). Skargi mogą być nieobecne lub mogą wynikać z przekrwienia w krążeniu płucnym lub ogólnoustrojowym. Pacjenci zwykle skarżą się na duszność, która pojawia się po raz pierwszy podczas wysiłku, a wraz z postępem choroby duszność obserwuje się w spoczynku. Ze względu na zmniejszenie funkcji pompowania serca pacjent skarży się na zmęczenie i słabą tolerancję na wszelkie obciążenia. Z czasem łączą się obrzęki nóg, powiększona wątroba i opuchlizna brzucha. Okresowo pojawia się nieregularne bicie serca, a wraz z rozwojem uporczywych blokad może dojść do omdlenia. Pierwszy etap rozwoju choroby (martwiczy) charakteryzuje się pojawieniem się gorączki, utraty wagi, kaszlu, wysypki skórnej i tachykardii. diagnostyka. Rozpoznanie RCM jest niezwykle trudne. O tej patologii można mówić z całą pewnością dopiero po wykluczeniu szeregu podobnych chorób (takich jak idiopatyczne zapalenie mięśnia sercowego typu Abramov-Fiedler, wysiękowe zapalenie osierdzia, wady zastawkowe serca). Podczas badania pacjentów z RCMP stwierdza się objawy charakterystyczne dla zastoinowej niewydolności serca (obrzęk, powiększenie wątroby i wodobrzusze), a także wyraźną pulsację żył szyi. Ta ostatnia wynika z trudności w dopływie krwi do serca z powodu słabej rozciągliwości mięśnia sercowego. Podczas osłuchiwania duże znaczenie ma wykrycie powiększonego serca, cichego późnego szmeru skurczowego i głośnego wczesnego III tonu (ze względu na szybkie napełnianie komór podczas rozkurczu). Szmery w sercu są również wykrywane u pacjentów z niewydolnością zastawki przedsionkowo-komorowej. Badanie EKG ujawnia umiarkowany przerost mięśnia sercowego, a także różne zaburzenia rytmu i przewodzenia impulsu serca oraz niespecyficzne zmiany załamka T w EKG. Echokardiografia jest jedną z najbardziej pouczających metod diagnozowania choroby, z jej pomocą, pogrubieniem wsierdzia, zmianą charakteru wypełnienia komór serca, zmniejszeniem funkcji pompowania serca, szybkim ruchem przedniego płatka zastawki mitralnej podczas rozkurczu i szybki wczesny ruch tylnej ściany lewej komory na zewnątrz. Rezonans magnetyczny pozwala uzyskać informacje o anatomii serca, określić patologiczne wtrącenia w mięśniu sercowym oraz zmierzyć grubość wsierdzia. Podczas badania parametrów hemodynamiki centralnej określa się podwyższone ciśnienie napełniania w obu komorach, a końcowe ciśnienie w lewej komorze jest wyższe niż w prawej komorze. Wentrykulografia ujawnia wzmożony skurcz lewej komory, gładkie kontury jej ścian, czasem z ubytkiem wypełnienia w wierzchołku (oznaczenie obliteracji). W niektórych przypadkach określa się zagłębienia w okolicy mięśni brodawkowatych. Istnieją oznaki niedomykalności zastawek, w szczególności zastawki mitralnej lub trójdzielnej. Diagnostyka różnicowa. W diagnostyce różnicowej RCM bardzo ważne jest uwzględnienie podobieństwa objawów zewnętrznych choroby do zwężającego zapalenia osierdzia, ale metoda leczenia tych chorób jest diametralnie odwrotna. Biopsję śródżyciową mięśnia sercowego i wsierdzia wykonuje się najczęściej jednocześnie z sondą kardiologiczną, co pozwala uzyskać więcej informacji pozwalających na wyjaśnienie charakteru choroby i dalsze leczenie. W niezwykle rzadkich przypadkach, gdy powyższe metody diagnostyczne nie pozwalają na odróżnienie RCM od zaciskającego zapalenia osierdzia, przeprowadza się bezpośrednią kontrolę osierdzia na stole operacyjnym. Wszyscy pacjenci z RCMP wymagają kompleksowego badania klinicznego, biochemicznego i dodatkowego w celu określenia pozasercowych przyczyn choroby. Leczenie. Leczenie choroby stwarza znaczne trudności. Większość leków stosowanych w leczeniu niewydolności serca może nie przynieść pożądanych rezultatów, ponieważ ze względu na charakterystykę choroby nie można uzyskać znaczącej poprawy podatności mięśnia sercowego (w niektórych przypadkach przepisuje się antagonistów jonów wapnia do tych celów). Diuretyki (aldakton) stosuje się w celu usunięcia nadmiaru płynów z organizmu. W celu wyeliminowania utrzymujących się zaburzeń przewodzenia może zaistnieć konieczność wszczepienia (wszczepienia) stałego rozrusznika serca. Jest to spowodowane chorobami takimi jak sarkoidoza i hemochromatoza, prowadzącymi do rozwoju wtórnego RCMP, podlegają one samoleczeniu. W leczeniu sarkoidozy stosuje się leki hormonalne (prednizolon itp.), A w przypadku hemochromatozy regularne upuszczanie krwi (w celu zmniejszenia stężenia żelaza w organizmie). Leczenie amyloidozy mięśnia sercowego jest bezpośrednio zależne od przyczyn jej wystąpienia. Wskazane jest stosowanie leków przeciwzakrzepowych na zakrzepicę w komorach serca. Leczenie chirurgiczne stosuje się w przypadkach RCMP spowodowanych uszkodzeniem wsierdzia. Podczas operacji, jeśli to możliwe, wycina się część wsierdzia, która uległa zmianom. W niektórych przypadkach, jeśli występuje niewydolność zastawek przedsionkowo-komorowych, wykonuje się ich protetykę. Niektóre formy amyloidowego uszkodzenia mięśnia sercowego leczy się przeszczepem serca. Zapobieganie RCMP. Niestety, środki zapobiegawcze w przypadku tej choroby są ograniczone. Przede wszystkim konieczna jest wczesna identyfikacja możliwych do uniknięcia przyczyn amyloidozy, sarkoidozy, hemochromatozy itp. Aby osiągnąć te cele, ogromne znaczenie mają coroczne badania lekarskie populacji. WYKŁAD nr 5. Choroby układu sercowo-naczyniowego. Infekcyjne zapalenie wsierdzia Infekcyjne zapalenie wsierdzia (IE) - choroba polegająca na polipowatości-wrzodziejącym uszkodzeniu aparatu zastawkowego serca (często z rozwojem niewydolności zastawkowej) lub wsierdzia ciemieniowego (rzadziej dotyczy to śródbłonka aorty lub najbliższej dużej tętnicy). Choroba jest wywoływana przez różne patogenne mikroorganizmy i towarzyszy jej ogólnoustrojowa zmiana narządów wewnętrznych (nerki, wątroba, śledziona) na tle zmienionej reaktywności organizmu. Do tej pory w różnych publikacjach drukowanych można było znaleźć wcześniej stosowane terminy „bakteryjne zapalenie wsierdzia”, „przedłużające się septyczne zapalenie wsierdzia” odnoszące się do tego patologicznego procesu. Jednak to określenie „infekcyjne zapalenie wsierdzia” zastąpił je lepiej odzwierciedla przyczynę choroby wywoływanej przez wiele różnych drobnoustrojów – czynniki bakteryjne, riketsje, wirusy i grzyby. Na całym świecie rośnie liczba pacjentów z IE. Wynika to z obecności tzw. grup ryzyka (pacjenci z miażdżycowymi, reumatycznymi, urazowymi uszkodzeniami zastawek, wadami serca lub zastawki, ubytkiem przegrody międzykomorowej, koarktacją aorty) w wyniku tego, że infekcja łatwiej zachodzi na patologicznie zmieniona zastawka lub wsierdzie. Etiologia. Patogennymi czynnikami sprawczymi choroby są najczęściej grupa kokosowa mikroorganizmów - paciorkowce (wcześniej wyizolowano streptococcus Viridans w 90% przypadków), gronkowce (złote, białe), enterokoki, pneumokoki. W ostatnich latach, w związku z powszechnym stosowaniem antybiotyków, zmienił się zakres patogenów drobnoustrojowych. Chorobę może wywołać flora Gram-ujemna (Escherichia coli, Pseudomonas aeruginosa, Proteus, Klebsiella); udowodniono ważną rolę patogennych grzybów, Sarcinus, Brucella i wirusów. Choroby wywoływane przez te patogeny mają cięższy przebieg, szczególnie zapalenie wsierdzia spowodowane infekcją grzybiczą (zwykle pojawia się na skutek nieracjonalnego stosowania antybiotyków). Jednak u części pacjentów nie udaje się wykryć prawdziwego czynnika wywołującego chorobę (częstotliwość ujemnych wyników posiewów krwi wynosi 20-50%). Często dochodzi do infekcji w miejscu protezy zastawki – tzw. protetyczna IE, która rozwija się głównie w ciągu 2 miesięcy po operacji wymiany zastawki serca. W tym przypadku czynnik sprawczy choroby najczęściej ma charakter paciorkowcowy. Tak więc źródła zakażenia i bakteriemii w IZW są bardzo różne (operacje w jamie ustnej, operacje i procedury diagnostyczne w okolicy moczowo-płciowej, interwencja chirurgiczna układu sercowo-naczyniowego (w tym wymiana zastawki), przedłużony pobyt cewnika w żyle, częste wlewy dożylne i metody badań endoskopowych, przewlekła hemodializa (przeciek tętniczo-żylny), dożylne podawanie leków). Istnieją tak zwane pierwotne IE, które rozwinęły się na nienaruszonych zastawkach, a także IE na tle wrodzonych i nabytych zmian w sercu i jego aparacie zastawkowym - wtórne zapalenie wsierdzia. Zmiany te umożliwiają wyodrębnienie chorych na odrębne grupy ryzyka: wady serca (wrodzone i nabyte), wypadanie płatka zastawki mitralnej, tętniaki tętniczo-żylne, tętniaki pozawałowe, przecieki, stan po operacjach serca i dużych naczyń. Patogeneza. Mechanizm rozwoju IZW jest złożony i niewystarczająco zbadany, jednak można zidentyfikować główne punkty rozwoju choroby. Jeśli w organizmie znajduje się ognisko infekcji pod wpływem zmienionej odporności humoralnej i miejscowej (komórkowej) z wypaczeniem reakcji immunologicznych, różnych czynników endogennych i egzogennych, rozwija się bakteriemia. Z krwi mikroorganizmy dostają się do zastawek serca, tworząc tam wtórne ognisko infekcji. Utrwalanie i rozmnażanie drobnoustrojów na wsierdziu jest ułatwione przez szereg czynników: wcześniejszą zmianę w tkance i powierzchni zastawki, obecność na niej mas zakrzepowych, powstających pod wpływem bezpośredniego uszkadzającego działania strumienia krwi gdy jego krążenie wewnątrzsercowe zmienia się w warunkach istniejącej choroby serca. W tym samym czasie różne komórki krwi (płytki krwi itp.) „Przyklejają się” do miejsca urazu, tworząc narośle przypominające sople lodu zwisające z zastawki. Rośliny te stają się dostępne dla infekcji, która dostała się do łożyska naczyniowego. Deformacja zastawek spowodowana występowaniem dużego gradientu ciśnienia, wąskim otworem i zmianami prędkości przepływu krwi również przyczynia się do wprowadzenia czynników zakaźnych do wsierdzia z utworzeniem ogniska zakaźnego. W przypadku uszkodzenia wcześniej nienaruszonej zastawki zachodzą zmiany, które zaburzają normalne właściwości poszczególnych odcinków tej zastawki (pojawia się obrzęk), procesy wysiękowe lub proliferacyjne ("śródmiąższowe zapalenie zastawek" - faza przedkliniczna). W rozwoju choroby można wyróżnić stadium III. Etap I (zakaźny-toksyczny) przebiega z różnym stopniem nasilenia zatrucia. Następuje rozwój bakterii, niszczenie zastawek, co prowadzi do rozwoju chorób serca; na tym samym etapie często dochodzi do uogólnienia procesu z powodu hematogennego rozprzestrzeniania się infekcji - kawałki guzków lub kolonii mikroorganizmów mogą oddzielić się od zastawki, guzki mogą pęknąć. Oderwanie się kawałków roślinności drobnoustrojów zastawkowych przyczynia się do wprowadzenia zainfekowanych zatorów do różnych części łożyska naczyniowego i zaostrzenia objawów septycznych. Kawałki zastawki lub roślinności drobnoustrojów krążą po ciele z przepływem krwi, gdy dostają się do mózgu, powodują zawały mózgu, którym towarzyszy paraliż, niedowład i różne inne zaburzenia neurologiczne. Zastawka, która uległa zniszczeniu, nie może pełnić swojej funkcji i wkrótce pojawia się błyskawicznie rozwijająca się niewydolność serca. Etap II - immunozapalny, w którym mikroorganizmy utrwalone na zastawkach powodują przedłużoną autouczulenie i hiperergiczne uszkodzenie narządów i tkanek organizmu (uogólnienie immunologiczne procesu). W tym okresie kompleksy immunologiczne krążą we krwi i są utrwalane w tkankach (serce, nerki, wątroba, naczynia krwionośne). Zaburzenia immunologiczne i autoimmunologiczne powodują rozwój zapalenia naczyń i trzewnych (immunokompleksowe zapalenie nerek, zapalenie mięśnia sercowego, zapalenie wątroby, zapalenie naczyń włosowatych itp.). Etap III - dystroficzny - występuje wraz z postępem procesu patologicznego: zaburzone są funkcje wielu narządów, dochodzi do niewydolności serca i nerek, co dodatkowo pogarsza przebieg choroby. Klasyfikacja. Obecnie stosuje się klasyfikację i nazewnictwo IZW uwzględniające postać kliniczną, wariant przebiegu, stopień aktywności, fazę patogenetyczną oraz postać kliniczną i morfologiczną choroby (patrz tabela 6). Tabela 6 Klasyfikacja IE
Rozróżnia się również aktywne i nieaktywne (uzdrowione) IE. Istnieje również klasyfikacja chirurgiczna, w której wyróżniają: 1) zmiana ogranicza się do płatków zastawki; 2) zmiana rozciąga się poza zastawkę. Ostra IZW (szybko postępująca, rozwija się w ciągu 8-10 tygodni) występuje rzadko, zwykle u osób, które wcześniej nie miały choroby serca, i klinicznie objawia się obrazem ogólnej sepsy. Dzięki nowoczesnym metodom leczenia możliwe jest przełożenie go na podostry. Podostre IE (najczęściej) trwa 3-4 miesiące, przy odpowiedniej terapii lekowej może dojść do remisji. Jednak możliwe są nawroty choroby. Przewlekłe IZW utrzymuje się przez wiele miesięcy z okresami zaostrzeń i remisji, charakteryzuje się łagodnymi objawami klinicznymi, niewielkimi parametrami laboratoryjnymi i zaburzeniami ogólnymi. Choroba zwykle dobrze reaguje na leczenie. Przy niekorzystnym przebiegu pojawiają się poważne powikłania, a pacjenci umierają z powodu postępującej niewydolności serca, zwiększając zatrucie septyczne. Obraz kliniczny. W zależności od czynnika wywołującego infekcję, IZW może wystąpić nagle i szybko się rozwijać (Staphylococcus aureus, enterococcus) lub mieć początek utajony (viridans streptococcus). Manifestacje IE prezentowane są w postaci syndromów. 1) Zespół zmian zapalnych i posocznicy (gorączka, dreszcze, wysypki krwotoczne, zmiany parametrów krwi ostrej fazy: leukocytoza z przesunięciem w lewo, wzrost ESR, pojawienie się białka C-reaktywnego, wzrost fibrynogenu, α2-globuliny. 2) Zespół ogólnego zatrucia organizmu (osłabienie, pocenie się, bóle głowy, bóle mięśni i stawów, utrata apetytu, bladość skóry z odcieniem żółtaczkowym). 3) Zespół uszkodzenia zastawki (powstawanie choroby serca). 4) Zespół „laboratoryjnych” zaburzeń immunologicznych (obecność kompleksów immunologicznych krążących we krwi lub utrwalonych w nerkach, mięśniu sercowym, naczyniach krwionośnych; hipergammaglobulinemia; pojawienie się czynnika reumatoidalnego; wykrycie przeciwciał przeciwtkankowych). 5) Zespół powikłań zakrzepowo-zatorowych (ogniskowe zapalenie nerek, zawał mięśnia sercowego, śledziona, jelita, choroba zakrzepowo-zatorowa w mózgu, naczynia kończyn dolnych itp.). 6) Zespół uogólnienia zmian (rozlane kłębuszkowe zapalenie nerek, zapalenie mięśnia sercowego, zapalenie wątroby, zapalenie naczyń itp.). Nasilenie tych zespołów jest różne. Zależy to od charakteru przebiegu IE, stadium, rodzaju patogenu. Na przykład gronkowcowy IE charakteryzuje się wysoką aktywnością procesu, ciężkimi objawami ogólnego zatrucia i rozwojem powikłań ropnych. Grzybiczemu zapaleniu wsierdzia towarzyszy zwykle zatorowe zamknięcie dużych tętnic, zwłaszcza kończyn dolnych. Typowy obraz choroby jest charakterystyczny dla IZW wywołanych przez paciorkowce viridans. Początek choroby jest często związany z ostrą infekcją lub zaostrzeniem przewlekłej infekcji, a także z szeregiem manipulacji medycznych. Szczególnie charakterystyczne jest połączenie wzrostu temperatury ciała o różnym stopniu (od przedłużonej gorączki do stanu podgorączkowego lub normalnej temperatury) z dreszczami i poceniem się. Pacjent składa jednocześnie skargi z powodu obecności procesu zakaźnego i zatrucia, a także powikłań zakrzepowo-zatorowych uszkodzenia serca. Pacjenci mogą mieć w wywiadzie epizody długotrwałego leczenia antybiotykami (ma to miejsce, gdy IE nawraca u wcześniej leczonych pacjentów). diagnostyka. Największe znaczenie dla postawienia prawidłowej diagnozy ma wykrycie uszkodzenia zastawek serca na skutek zmian w obrazie osłuchowym istniejących wcześniej wad serca; pojawienie się „dodatkowego” hałasu. Ujawniają się charakterystyczne zmiany na skórze i błonach śluzowych: zabarwienie skóry typu cafe au lait, krwotoki, dodatnie objawy Hechta (szczypanie) i Konczałowskiego-Rumpel-Leede (opaska uciskowa), a także węzły Oslera – bolesne, przekrwione, gęste guzki na powierzchni dłoniowej i dłoniowej. opuszki palców , objaw Lukina-Libmana (plamy Lukina) - krwotok na przejściowym fałdzie spojówki. W IZW często obserwuje się splenomegalię. Znacząca utrata masy ciała (czasami 15-20 kg) jest bardzo typowa. W rzadkich przypadkach rozwija się zapalenie osierdzia (słaby odgłos tarcia opłucnej powodowany przez złogi włókniste na osierdziu). Badanie fizykalne może ujawnić podwyższone ciśnienie krwi, co wskazuje na rozwój rozlanego kłębuszkowego zapalenia nerek. Czasami stwierdza się oznaki dysfunkcji ośrodkowego układu nerwowego (niedowład, hiperkineza, odruchy patologiczne itp.) W wyniku zatorowości naczyń mózgowych. W tym przypadku najczęstszym błędem diagnostycznym jest ocena konkretnego zespołu jako przejawu niezależnej choroby (na przykład z wyraźnymi objawami uszkodzenia wątroby, rozpoznano zapalenie wątroby itp.). Rozpoznanie IE opiera się jednak przede wszystkim na wczesnym wykryciu czynnika sprawczego choroby. W tym celu stosuje się następujące badania laboratoryjne i instrumentalne. 1) Uzyskanie dodatniego posiewu krwi jest najważniejszym objawem diagnostycznym IE. Niezbędna jest również analiza w celu wybrania najskuteczniejszego antybiotyku w tym przypadku. Co najmniej 2-3 z nich są wymagane do potwierdzenia diagnozy. Duże znaczenie ma technika pobierania i posiewu krwi, czas inokulacji (najlepiej w szczytowej fazie gorączki), stosowanie pożywek wzbogaconych. 2) Wykonanie NBT (test nitrobluttetrazolium) - diagnostyka ogólnoustrojowych infekcji bakteryjnych, która pozwala odróżnić infekcje bakteryjne od innych chorób zapalnych. Metoda opiera się na redukcji rozpuszczalnego barwnika NBT przez neutrofile do nierozpuszczalnego osadu formazanu. Jeżeli liczba komórek NBT-dodatnich przekracza 10%, test uznaje się za pozytywny. 3) Kliniczne badanie krwi w celu wykrycia wskaźników ostrej fazy: można wykryć wzrost ESR do 50 mm / h lub więcej, leukocytozę z przesunięciem formuły leukocytów w lewo lub (w stadium II) leukopenię i niedokrwistość hipochromiczną. Wartość diagnostyczna wiąże się z wykryciem histiocytów we krwi pobranej z płatka ucha. Ich zawartość powyżej 6 w polu widzenia może przemawiać na korzyść IE. Biochemiczne badanie krwi wykazuje wzrost zawartości fibrynogenu, α2-globuliny i α-globuliny - do 30-40%. 4) Identyfikacja zmian immunologicznych: hipergammaglobulinemia, krążące kompleksy immunologiczne, spadek miana dopełniacza, pojawienie się czynnika reumatoidalnego (antyglobulinowego), nasilenie reakcji władczej transformacji limfocytów z PHA (fitohemaglutyniną) i antygenami bakteryjnymi, wykrycie przeciwciał przeciwtkankowych. 5) Badanie moczu wykonuje się w celu wyjaśnienia zmian w różnych narządach i układach, gdy wykryte zostanie kłębuszkowe zapalenie nerek, objawiające się białkomoczem, cylindrurią i krwiomoczem. Wzrost zawartości bilirubiny, transaminaz wskazuje na uszkodzenie wątroby. 6) Bezpośredni znak diagnostyczny IE - obecność roślinności na zastawkach serca - jest wykrywany za pomocą echokardiografii. Tak więc z całej gamy objawów należy wyróżnić główne i dodatkowe. Główne kryteria rozpoznania IE: 1) gorączka o temperaturze powyżej 38 ° C z dreszczami; 2) Plamy Lukina; 3) guzki Oslera; 4) zapalenie wsierdzia na niezmienionych zastawkach (pierwotne) lub na tle reumatycznych i wrodzonych wad serca. zakaźne zapalenie mięśnia sercowego; 5) mnoga tętnicza choroba zakrzepowo-zatorowa, pęknięcia tętniaków grzybiczych z krwotokami; 6) splenomegalia; 7) dodatni posiew krwi; 8) wyraźny pozytywny efekt stosowania antybiotyków. Dodatkowe kryteria rozpoznania IE: 1) wzrost temperatury ciała do 38 ° C, schładzanie; 2) krwotoki na skórze; 3) szybka utrata wagi; 4) asymetryczne zapalenie stawów drobnych stawów rąk, stóp; 5) anemizacja; 6) ESR powyżej 40 mm/h; 7) ostro dodatnia SRV; 8) obecność czynnika reumatoidalnego; 9) α-globuliny powyżej 25%; 10) wzrost zawartości immunoglobulin M, E i A. Diagnostyka różnicowa. Chociaż w IZW najczęściej obserwuje się chorobę zakrzepowo-zatorową, nie należy wykluczać innych przyczyn zatorowości w tętnicy krążenia ogólnoustrojowego: zawału przezściennego mięśnia sercowego i tętniaka serca, idiopatycznego zapalenia mięśnia sercowego Abramova-Fiedlera oraz migotania przedsionków różnego pochodzenia, ale obserwowanego przede wszystkim w zwężeniach reumatycznych lewego ujścia przedsionkowo-komorowego. Największe znaczenie w diagnostyce różnicowej ma reumatyczne i infekcyjne zapalenie wsierdzia (tab. 7). Tabela 7 Różnicowe kryteria diagnostyczne dla reumatycznego zapalenia wsierdzia i przedłużonego IE
Charakterystycznymi objawami IE są powiększona śledziona. Jednak w amyloidozie obserwuje się dużą, jędrną, bezbolesną śledzionę; miękki, bezbolesny wskazuje na jego przerost septyczny. Bolesność odnotowuje się z zawałem śledziony, zlokalizowanym podtorebkowo. Splenomegalia może być jednym z objawów nadciśnienia wrotnego w prawokomorowej niewydolności serca. W tym przypadku łączy się go z wodobrzuszem i hepatomegalią. Dość często obserwuje się wzrost wielkości wątroby z przedłużonym IE. Rozrost septyczny charakteryzuje się stosunkowo niewielkim powiększeniem i miękką konsystencją wątroby. Występują zwyrodnienia tłuszczowe i niezwykle rzadko - zawały wątroby. Najczęściej wzrost wątroby jest związany z przekrwieniem żylnym z niewydolnością prawego serca. W przypadku braku wodobrzusza przekrwienie rozpoznaje się retrospektywnie na podstawie zmniejszenia wielkości wątroby po leczeniu glikozydami nasercowymi i lekami moczopędnymi. Leczenie. Leczenie IZW powinno być możliwie wczesne i etiotropowe, biorąc pod uwagę dane bakteriologiczne. Zanim leki przeciwbakteryjne znalazły szerokie zastosowanie w praktyce medycznej, większość pacjentów z IZW umierała z powodu infekcji i jej powikłań. Obecnie ponad 80% jest skutecznie wyleczonych. Jednak u prawie 20% pacjentów leczenie farmakologiczne jest nieskuteczne i wkrótce rozwija się u nich niewydolność serca, która jest prawie nieuleczalna. W związku z tym wskazane jest połączenie leczenia zachowawczego i chirurgicznego. W leczeniu IE w każdej grupie wiekowej stosuje się przede wszystkim antybiotyki, które działają bakteriobójczo na drobnoustroje, najlepiej w dawkach zindywidualizowanych w zależności od stężenia antybiotyku we krwi i wrażliwości patogenu na niego. Lekiem pierwszego wyboru nadal jest penicylina. Ma niską toksyczność, dzięki czemu może być stosowany przez długi czas w stosunkowo wysokich dawkach. Dzienna dawka - do 20 000 000 IU podawana jest dożylnie i domięśniowo. Nie należy jednak wykluczać, że u pacjentów w podeszłym wieku, leczonych penicyliną i innymi antybiotykami w dużych dawkach, często obserwuje się działanie kardiotoksyczne: pojawienie się lub nasilenie niewydolności serca, ból w sercu, tachykardię. Po zmniejszeniu dawki lub zmianie leku zjawiska te ustają. Przy nieznanej etiologii leczenie rozpoczyna się od wysokich dawek benzylopenicyliny domięśniowo lub dożylnie do 18 000 000-20 000 000 jednostek lub więcej, kombinacji ze streptomycyną do 1 g / m dziennie lub aminoglikozydami (gentamycyna, tobramycyna w ilości 4-6 mg / dzień) stosuje się kg na dzień). W przypadku braku efektu lub po określeniu patogenu stosuje się półsyntetyczne penicyliny (domięśniowo oksacylinę, metycylinę lub ampicylinę do 12 g / dzień). Cefalosporyny są również podstawowymi lekami stosowanymi w leczeniu IZW: najczęściej stosowane są klaforan, cefamizyna (4-10 g/dobę domięśniowo i dożylnie) oraz zeporyna (10-16 g/dobę) i kefzol (do 8-10 g dożylnie) itp.). Fusydyna ma dobre działanie przeciwgronkowcowe, w niektórych przypadkach jest skuteczna w oporności drobnoustrojów na inne antybiotyki (2-3 g/dobę). Leczenie antybiotykami jest przepisywane przez długi czas w ciągu 1,5-2 miesięcy, aż do całkowitego wyeliminowania infekcji. Po wyeliminowaniu infekcji poprawia się stan ogólny pacjenta, zanika roślinność zgodnie z echokardiografią i potwierdzeniem mikrobiologicznym. Przy zmniejszonej immunoreaktywności organizmu środki przeciwbakteryjne łączy się z immunoterapią bierną (na przykład z gronkowcowym zapaleniem wsierdzia - z osoczem przeciwgronkowcowym lub α-globuliną przeciwgronkowcową), stosując immunomodulatory (tymalina, T-aktywina itp.). W celu zapobiegania zakrzepicy, na przykład z zapaleniem wsierdzia, które rozwinęło się na tle posocznicy angiogennej, wytwarza się kontrolowaną hipokoagulację za pomocą heparyny (20 000-25 000 jm dożylnie lub podskórnie). Do hamowania enzymów proteolitycznych stosuje się contrical (do 40-000 60 IU dożylnie). Gdy IE zastawkowe przyczyniło się do powstania wady zastawkowej serca lub objawy choroby nie ustępują pomimo masywnej antybiotykoterapii, wskazane jest przeprowadzenie leczenia operacyjnego. Dodatkowym argumentem przemawiającym za interwencją chirurgiczną jest ponowny zator z uszkodzonych przez infekcję płatków zastawki serca. Czasami infekcja wykracza poza granice pierścienia zastawki, tworząc ropnie, co jest również wskazaniem do leczenia operacyjnego. Głównym celem operacji jest zachowanie własnej zastawki pacjenta. Czasem ograniczają się do usunięcia roślinności, zszycia pęknięć zastawek itp. Jeśli zastawka pod wpływem infekcji zostanie prawie całkowicie zniszczona, zastępuje się ją sztuczną (protezą) przy użyciu protez mechanicznych i biologicznych. profilaktyka. Zapobieganie IE polega na terminowym odkażaniu przewlekłych ognisk infekcji w jamie ustnej, migdałkach, nosogardzieli, zatokach przynosowych oraz stosowaniu aktywnej terapii przeciwbakteryjnej w przypadku ostrych chorób paciorkowcowych i gronkowcowych (dławica piersiowa itp.). Zalecane jest hartowanie organizmu. Wszyscy pacjenci z wadą zastawkową serca, a także z protezami zastawek, powinni profilaktycznie przyjmować antybiotyki dzień przed i krótko po każdej interwencji, po czym infekcja może dostać się do krwiobiegu. Konieczna jest obserwacja ambulatoryjna osób, które przeszły ostre infekcje paciorkowcowe, gronkowcowe. WYKŁAD nr 6. Choroby układu oddechowego. Astma oskrzelowa Do tej pory nie istnieje wyczerpująca definicja astmy, jednak najpełniejszą definicję tej choroby podał G. B. Fedoseev w 1982 roku. Astma oskrzelowa (BA) jest niezależną, przewlekłą, nawracającą chorobą z pierwotnym uszkodzeniem dróg oddechowych, głównym i obowiązkowym mechanizmem patogenetycznym jest zmieniona reaktywność oskrzeli spowodowana specyficznymi (immunologicznymi) i (lub) niespecyficznymi, wrodzonymi lub nabytymi mechanizmami, a głównym (obowiązkowym) objawem klinicznym jest atak astmy i (lub) stan astmatyczny (stan astmatyczny) z powodu skurczu mięśni gładkich oskrzeli, nadmiernego wydzielania, dyskrynii i obrzęku błony śluzowej oskrzeli. Etiologia. W występowaniu astmy ważną rolę odgrywa połączenie kilku czynników. Pod tym względem istnieją 2 formy astmy - atopowa (od łacińskiej atopii - „dziedziczna predyspozycja”) i zakaźno-alergiczna. Dziedziczna predyspozycja wynika ze związku niektórych antygenów zgodności tkankowej (HLA) z nasileniem astmy, a nasilenie choroby szczególnie często obserwuje się u nosicieli antygenów B35 i B40. Czynnikami wewnętrznymi w rozwoju choroby są biologiczne wady układu odpornościowego, hormonalnego, autonomicznego układu nerwowego, wrażliwość i reaktywność oskrzeli, klirens śluzowo-rzęskowy, śródbłonek naczyń płucnych, system szybkiej odpowiedzi (komórki tuczne itp.), metabolizm kwasu arachidonowego, itp. Czynniki zewnętrzne obejmują: 1) alergeny zakaźne (wirusy, bakterie, grzyby, drożdże itp.); 2) alergeny niezakaźne (pyłki, kurz, przemysłowe, lecznicze, spożywcze; alergeny kleszczy, owadów i zwierząt); 3) drażniące mechaniczne i chemiczne (metal, drewno, krzemiany, pyły bawełniane; opary kwasów, zasad; opary itp.); 4) czynniki meteorologiczne i fizykochemiczne (zmiany temperatury i wilgotności powietrza, wahania ciśnienia barometrycznego, pola magnetycznego Ziemi, wysiłek fizyczny itp.); 5) stresujące, neuropsychiczne skutki i aktywność fizyczna. Czynniki zakaźne mogą mieć nie tylko działanie alergizujące, ale także obniżać próg wrażliwości organizmu na alergeny niezakaźne (atopowe), zwiększać dla nich przepuszczalność błony śluzowej dróg oddechowych; w celu wytworzenia zmiany w reaktywności komórek docelowych (komórki tuczne, bazofile, monocyty itp.) i układów efektorowych. Patogeneza. Zmiana reaktywności oskrzeli jest głównym ogniwem w patogenezie choroby i może mieć charakter pierwotny lub wtórny. W pierwszym przypadku zmiany reaktywności mogą być wrodzone lub nabyte w wyniku bezpośredniego narażenia na czynniki chemiczne, mechaniczne, fizyczne i infekcji. Wtórne zmiany w reaktywności oskrzeli są przejawem zmian w reaktywności układu odpornościowego, hormonalnego i nerwowego organizmu. Zatem mówiąc o patogenezie AD, można wyróżnić 2 grupy mechanizmów: immunologiczne i nieimmunologiczne. W przebiegu choroby dominują mechanizmy immunologiczne. Naruszenia układu immunokompetentnego w błonie śluzowej dróg oddechowych, występujące zgodnie z typami I, III i IV reakcji nadwrażliwości, tj. ze zmianą odporności humoralnej i komórkowej, prowadzą do zmiany reaktywności oskrzeli. Jednocześnie następuje spadek wydzielania IgA, zaburzony jest układ fagocytozy, zmniejsza się funkcja supresora T limfocytów, zmniejsza się produkcja interferonu, co ostatecznie prowadzi do zmniejszenia obrony przeciwwirusowej organizmu. Typ I (atopowy, reaginiczny lub anafilaktyczny). W odpowiedzi na spożycie antygenów egzoalergenowych (pyłek, białka zwierzęce i roślinne, bakterie i leki) dochodzi do zwiększonej produkcji IgE (reagin), które są utrwalane i gromadzą się na komórkach tucznych (pierwotnych komórkach efektorowych). To jest immunologiczny etap AD. Następnie rozwija się patochemiczny etap procesu - degranulacja komórek tucznych z uwolnieniem substancji wazoaktywnych, skurczowych i chemotaktycznych (histamina, serotonina, różne czynniki chemotaktyczne itp.). Są to mediatory pierwotne, które działają na naczynia krwionośne i komórki docelowe (wtórne komórki efektorowe) – eozynofile, neutrofile, płytki krwi, monocyty makrofagów. Te ostatnie po ekspozycji na mediatory pierwotne wydzielają mediatory wtórne (leukotrieny, prostaglandyny, tromboksany, czynnik aktywujący płytki krwi i inne substancje należące do grupy eikozanoidów). Pod wpływem substancji biologicznie czynnych rozpoczyna się patofizjologiczny etap patogenezy: zwiększa się przepuszczalność złoża mikrokrążenia, co prowadzi do rozwoju obrzęku, surowiczego zapalenia i skurczu oskrzeli. Klinicznie objawia się to ostrym naruszeniem drożności oskrzeli i rozwojem ataku astmy. Reakcja typu III (immunokompleks, czyli zjawisko Arthusa) rozwija się pod wpływem egzoalergenów i endoalergenów (autoalergenów, których powstanie prowadzi do denaturacji białek oskrzelików i pęcherzyków płucnych w wyniku zapalenia infekcyjnego lub alergicznego różne czynniki drażniące). Reakcja zachodzi w strefie nadmiaru antygenu z udziałem wytrącających się przeciwciał należących do immunoglobulin klas O i M. Szkodliwe działanie utworzonego kompleksu antygen-przeciwciało jest realizowane poprzez aktywację dopełniacza, uwalnianie enzymów lizosomalnych. Występuje uszkodzenie błon podstawnych, skurcz mięśni gładkich oskrzeli, rozszerzenie naczyń krwionośnych i zwiększenie przepuszczalności mikronaczyń. Typ IV (nadwrażliwość komórkowa typu opóźnionego) charakteryzuje się tym, że uczulone limfocyty mają działanie niszczące. W tym przypadku mediatorami reakcji alergicznej są limfokiny (działają na makrofagi, komórki nabłonkowe), enzymy lizosomalne i aktywowany układ kininowy. Pod wpływem tych substancji rozwija się obrzęk, obrzęk błony śluzowej, skurcz oskrzeli, nadprodukcja lepkiej wydzieliny oskrzelowej. Konsekwencją jest ostre naruszenie drożności oskrzeli, objawiające się atakiem uduszenia. Mechanizmy nieimmunologiczne są podstawową zmianą reaktywności oskrzeli w wyniku wrodzonych i nabytych wad biologicznych. Mechanizmy nieimmunologiczne działają na pierwotne lub wtórne komórki efektorowe lub na receptory mięśni gładkich oskrzeli, naczyń krwionośnych, komórek gruczołów oskrzelowych. Zmienia to reaktywność komórek docelowych, a przede wszystkim komórek tucznych, czemu towarzyszy nadmierna produkcja substancji biologicznie czynnych (histamina, leukotrieny itp.). W odpowiedzi na ich uwolnienie rozwija się skurcz oskrzeli, obrzęk błony śluzowej, hiper- i dyskrynia gruczołów oskrzelowych. Wszystko to dramatycznie zmienia drożność oskrzeli i powoduje atak astmy. Opór oskrzeli może zmieniać się warunkowo i bezwarunkowo jako odruch. Na przykład niedrożność wynikająca z narażenia na zimne powietrze, wdychania drażniących gazów i pyłów oraz aktywności fizycznej jest spowodowana skurczem oskrzeli wynikającym z odruchu błędnego. Przyczyną skurczu oskrzeli może być również uszkodzenie stref efektorowych odruchu zwężającego oskrzela nerwu błędnego lub blokada receptorów β-adrenergicznych. Ostatnio mówi się o szczególnej roli w patogenezie naruszeń drożności oskrzeli w niewydolności glikokortykoidowej i zaburzeniach wymiotnych. Niedobór glikokortykosteroidów prowadzi do rozwoju nadreaktywności komórek tucznych, zmniejszenia syntezy katecholamin i aktywacji prostaglandyn F2a, a także naruszenie układu immunokompetentnego (tu mówimy o złożonym udziale w patogenezie AD oraz mechanizmach immunologicznych i nieimmunologicznych). Hiperestrogenemia i hipoprogesteronemia działają na receptory α- i β-adrenergiczne, zwiększając aktywność tych pierwszych i zmniejszając aktywność tych drugich. Klasyfikacja. Przewaga tego czy innego mechanizmu w patogenezie astmy pozwala zidentyfikować jej różne cechy patogenetyczne. Obecnie stosowana jest klasyfikacja zaproponowana przez G. B. Fedoseeva (1982). Etapy rozwoju AD. I - stan przed astmą (stany zagrażające rozwojowi: ostre i przewlekłe zapalenie oskrzeli, ostre i przewlekłe zapalenie płuc z elementami skurczu oskrzeli w połączeniu z naczynioruchowym nieżytem nosa, pokrzywką). II - klinicznie ukształtowane BA (uznawane za takie po pierwszym ataku lub natychmiastowym wystąpieniu stanu astmatycznego). Formy licencjackie: 1) immunologiczne; 2) nieimmunologiczne. Mechanizmy patogenetyczne (warianty kliniczne i patogenetyczne) AD: 1) atopowy; 2) zależne od infekcji; 3) autoimmunologiczny; 4) dyshormonalne; 5) brak równowagi neuropsychicznej; 6) zaburzenia równowagi adrenergicznej; 7) brak równowagi cholinergicznej; 8) pierwotna zmieniona reaktywność oskrzeli. U jednego pacjenta możliwe jest połączenie kilku wariantów klinicznych i patogenetycznych. W takiej sytuacji konieczne jest w momencie badania podkreślenie głównego wariantu dla tego pacjenta, co jest ważne dla odpowiedniej terapii. W trakcie długiego przebiegu BA możliwa jest zmiana mechanizmu patogenetycznego. Ciężkość BA: 1) łagodny przebieg (zaostrzenia są rzadkie, 2-3 razy w roku, krótkotrwałe ataki astmy są zatrzymywane przez przyjmowanie różnych leków rozszerzających oskrzela); 2) umiarkowane (częstsze zaostrzenia 3-4 razy w roku, ataki astmy są cięższe i zatrzymywane przez zastrzyki leków); 3) ciężki przebieg (charakteryzujący się częstymi i długotrwałymi zaostrzeniami, ciężkimi atakami, często przechodzącymi w stan astmatyczny). Podział licencjatu ze względu na stopień zaawansowania kursu jest warunkowy. Tak więc przy łagodnym przebiegu BA pacjent może umrzeć z powodu nagle rozwiniętego stanu astmatycznego. Fazy kursu BA: 1) zaostrzenie (obecność nawracających ataków astmy lub stanu astmatycznego); 2) ustępujące zaostrzenie (ataki stają się rzadsze i łagodniejsze, fizyczne i czynnościowe objawy choroby są mniej wyraźne niż w fazie zaostrzenia); 3) remisja (ustępują typowe objawy astmy: nie występują napady astmy, drożność oskrzeli zostaje całkowicie lub częściowo przywrócona). komplikacje: 1) płuc: rozedma, niewydolność płuc, niedodma, odma opłucnowa, stan astmatyczny itp.; 2) pozapłucne: serce płucne (skompensowane i zdekompensowane rozwojem prawokomorowej niewydolności serca), dystrofia mięśnia sercowego itp. Obraz kliniczny. Najbardziej charakterystycznym objawem astmy są skargi na ataki uduszenia (trudności w oddychaniu głównie podczas wydechu), duszność i różnego rodzaju kaszel (od suchego, napadowego lub z wydzielaniem lepkiej plwociny). Rozwój infekcji oskrzelowo-płucnej powoduje wzrost temperatury ciała. Wynikające z tego trudności w oddychaniu przez nos są objawem alergicznej rinozynosopatii (naczynioruchowego nieżytu nosa, polipowatości), która zwykle występuje w fazie przedastmowej. Dane z historii pomagają ustalić związek między rozwojem napadów a narażeniem na niektóre alergeny i inne czynniki. Najczęściej jest to infekcja dróg oddechowych, zwłaszcza w zaostrzeniu choroby. Z anamnezy dowiadują się o wpływie wysiłku fizycznego (takiego jak szybki marsz, śmiech itp.), zmian czynników meteorologicznych (takich jak zimno, wysoka wilgotność itp.), zaburzeń dysowariancji, czynników zawodowych na występowanie astmy ataki. Badanie historii alergii przyczynia się do rozpoznania atopowego wariantu BA. W takich przypadkach zaostrzenia choroby mają charakter sezonowy (częściej wiosną i latem), któremu towarzyszy nieżyt nosa, zapalenie spojówek. Tacy pacjenci mają pokrzywkę, obrzęk Quinckego; nietolerancja pokarmowa, wykryto szereg substancji leczniczych; istnieje dziedziczna predyspozycja do chorób alergicznych. Dane z wywiadu często pozwalają na stwierdzenie obecności tzw. astmy aspirynowej. W tym przypadku nie ma dziedzicznej postaci chorób alergicznych. Tacy pacjenci są zaniepokojeni zaburzeniami oddychania przez nos (polipami), a najbardziej charakterystycznym objawem jest nietolerancja niesteroidowych leków przeciwzapalnych (kwas acetylosalicylowy, indometacyna itp.), które powodują ataki astmy. W tym przypadku można już założyć, że AD jest mechanizmem prostaglandyn. Dane dotyczące rozwoju stanu astmatycznego w przeszłości wskazują na ciężkość przebiegu choroby i wskazują na potrzebę leczenia kortykosteroidami. diagnostyka. Duże znaczenie ma identyfikacja pozapłucnych objawów alergii, objawów niedrożności oskrzeli, powikłań astmy i innych chorób, którym towarzyszą ataki skurczu oskrzeli. Podczas badania skóry można wykryć objawy alergiczne: pokrzywkę, grudkowe wysypki rumieniowe, co wskazuje na immunologiczny wariant BA. Połączenie astmy z egzemą, neurodermitem, łuszczycą predysponuje do ciężkiej astmy. Często można zidentyfikować naruszenie oddychania przez nos. Nieżyt nosa i polipy są uważane za stan przedastmiczny. Zapalenie zatok i inne zapalenie zatok może powodować zadławienie. Badanie fizykalne płuc, często z powodu przewlekłego zapalenia oskrzeli, może ujawnić objawy rozedmy płuc prowadzące do rozwoju przewlekłej niewydolności oddechowej i serca płucnego. Wykrywane są osłuchowe oznaki niedrożności oskrzeli: zmiana w oddychaniu (wydłużony wydech, suchość, głównie świszczący oddech, świszczący oddech), wymuszony wydech, który objawia się utajonym skurczem oskrzeli (pojawienie się lub nasilenie suchego świszczącego oddechu). Osłuchiwanie płuc musi odbywać się w pozycji leżącej pacjenta: liczba suchych rzęsek wzrasta wraz z ich mechanizmem „błędnym”. Stale słuchane w określonym obszarze, wilgotne, dźwięczne („trzeszczące”) drobne bulgoczące rzęski mogą wskazywać na rozwiniętą pneumosklerozę. Obiektywne badanie pacjenta ujawnia objawy innych chorób („motyl” na skórze twarzy, powiększenie węzłów chłonnych w połączeniu ze wzrostem wątroby i śledziony, uporczywy wzrost ciśnienia krwi, uporczywą gorączkę itp.), W których występują napady skurczu oskrzeli, objawiające się uduszeniem (toczeń rumieniowaty układowy, guzkowe zapalenie okołotętnicy). Wtedy rzekoma diagnoza AD staje się mało prawdopodobna. Spirografia ujawnia charakterystyczne objawy obturacyjnego typu niedrożności oskrzeli: zmniejszenie natężonej objętości wydechowej w pierwszej sekundzie (FEV1), zmniejszenie współczynnika Tiffno (FEV1 do VC jako procent) i procent FEV1 do FZhEL. Podczas zaostrzenia BA resztkowa objętość płuc (RLV) i funkcjonalna pojemność resztkowa (FOC) przekraczają poziom początkowy o 100% lub więcej. Analizując spirogram stwierdza się objawy dyskinezy tchawiczo-oskrzelowej, przyczyniające się do naruszenia drożności oskrzeli, poprzez obecność wycięcia w górnej części opadającego koloru spirogramu (objaw Kolbeta-Wyssa). Pneumotachometria wykazuje przewagę mocy wdechu nad mocą wydechu, która jest charakterystyczna dla obturacji oskrzeli. Według pneumotachografii z konstrukcją krzywej „przepływ - objętość” naruszenie drożności oskrzeli diagnozuje się osobno na poziomie dużych, średnich i małych oskrzeli. Pojawienie się zwiększonej oporności oskrzeli, zarejestrowanej za pomocą spirografii, pneumotachometrii i pneumotachografii, w odpowiedzi na aktywność fizyczną, wdychanie zimnego powietrza, drażniących gazów i acetylocholiny wskazuje na zmienioną reaktywność oskrzeli. Testy alergologiczne przeprowadza się przy użyciu zestawu różnych alergenów niezakaźnych i zakaźnych, przeprowadza się je tylko poza zaostrzeniem choroby. Aby ocenić prowokujące działanie alergenu, wykonuje się skórne testy alergiczne (aplikacja, skaryfikacja i śródskórne metody podawania alergenu), alergen można aplikować na spojówkę oka, błonę śluzową nosa. Najbardziej wiarygodna jest swoista diagnoza astmy - identyfikacja specyficznej nadreaktywności oskrzeli za pomocą wziewnych testów prowokacyjnych. Nie należy jednak zapominać o tym, że ta droga podania może wywołać ciężki atak astmy lub rozwój stanu astmatycznego. Do specyficznej diagnozy AZS, np. gdy niemożliwe jest przeprowadzenie badania alergicznego, stosuje się również test radioimmunosorbent, który umożliwia ilościową ocenę przeciwciał IgE. Badania laboratoryjne pomagają potwierdzić proponowaną diagnozę, ocenić ewolucję choroby i skuteczność leczenia. Głównym kryterium diagnostycznym AD jest pojawienie się eozynofili w plwocinie, ale jest to objaw niespecyficzny, może służyć jako przejaw ogólnej reakcji alergicznej organizmu. Znaczenie diagnostyczne ma również wykrywanie spiral Kurshmana i kryształów Charcota-Leiden w plwocinie. Badania laboratoryjne dowodzą obecności aktywnego procesu zapalnego i stopnia jego nasilenia pod względem wzrostu wskaźników ostrej fazy. Wraz ze wzrostem niewydolności oddechowej w przypadku zaostrzenia astmy i stanu astmatycznego ważne jest zbadanie stanu kwasowo-zasadowego i składu gazometrii. Badanie rentgenowskie diagnozuje ogniska infekcji (w zatokach przynosowych, zębach, woreczku żółciowym) oraz obecność ostrego (zapalenie płuc) lub zaostrzenie przewlekłego procesu zapalnego w płucach, rozedmę i pneumosklerozę. Dane EKG świadczą o rozwoju skompensowanego serca płucnego – przerostu prawego serca. Diagnostyka różnicowa. BA różni się od astmy sercowej (patrz tabela 8). Tabela 8 Diagnostyka różnicowa AD
Niezbędne jest również różnicowanie astmy infekcyjno-alergicznej i atopowej (patrz Tabela 9). Tabela 9 Astma zakaźna-alergiczna i atopowa
Leczenie. W leczeniu astmy zaleca się podejście stopniowe, co tłumaczy się zmiennym nasileniem jej przebiegu u różnych osób i u tego samego pacjenta. Etap 1 to najmniej ciężka astma, etap 4 jest największy. Krok 1: Łagodny, przerywany przebieg, w którym objawy astmy pojawiają się po ekspozycji na wyzwalacz (np. pyłek lub sierść zwierząt) lub z powodu ćwiczeń. Długotrwałe stosowanie leków przeciwzapalnych w leczeniu takich pacjentów nie jest wskazane. Leczenie polega na podawaniu leków profilaktycznych, jeśli to konieczne (wziewne β2agoniści, kromoglikan, nedokromil lub leki antycholinergiczne). Czasami cięższe i przedłużone zaostrzenia wymagają krótkiej kuracji doustnymi kortykosteroidami. Jeśli astma objawia się częstszymi objawami, wzrostem zapotrzebowania na leki rozszerzające oskrzela, konieczne staje się przejście do następnego etapu. Etap 2. Lekko uporczywy kurs. Terapia podstawowa obejmuje leki przeciwzapalne, wziewne kortykosteroidy, kromoglikan sodu lub nedokromil sodu. Dawka kortykosteroidów wynosi 200-500 mikrogramów dipropionianu beklometazonu lub budezonidu dziennie. W leczeniu objawowym, wziewne β2-agoniści, ale nie więcej niż 3-4 razy dziennie. W przypadku cięższych i długotrwałych zaostrzeń podaje się krótki cykl doustnych kortykosteroidów. Jeśli objawy utrzymują się pomimo początkowej dawki wziewnych kortykosteroidów, dawkę dipropionianu beklometazonu należy zwiększyć do 750-800 mikrogramów na dobę. Jednak alternatywą dla zwiększenia dawki hormonów wziewnych, zwłaszcza w celu opanowania nocnych napadów astmy, jest dodatek długo działających leków rozszerzających oskrzela przyjmowanych na noc (w dawce wziewnych kortykosteroidów co najmniej 500 mcg). Etap 3 charakteryzuje się umiarkowanym nasileniem BA. Tacy pacjenci wymagają codziennego przyjmowania profilaktycznych leków przeciwzapalnych. Dawka kortykosteroidów wziewnych wynosi 800-2000 mcg w połączeniu z długo działającymi lekami rozszerzającymi oskrzela. Można stosować teofiliny długo działające (przy stałym monitorowaniu ich stężenia nie więcej niż 5-15 µg/ml), doustne i wziewne β2długo działający agoniści. Objawowo wyznaczyć β2- krótkodziałający agoniści lub leki alternatywne (etap 2). Etap 4. Ciężka astma, gdy nie jest całkowicie kontrolowana. W takim przypadku celem leczenia jest osiągnięcie jak najlepszych rezultatów. Leczenie podstawowe obejmuje duże dawki wziewnych kortykosteroidów (od 800 do 2000 mikrogramów dipropionianu beklometazonu na dobę) w połączeniu z długo działającymi lekami rozszerzającymi oskrzela. Jeśli to konieczne, wziewny β jest wskazany w celu złagodzenia objawów.2- krótkodziałający agoniści (nie więcej niż 3-4 razy dziennie). Cięższe zaostrzenie może wymagać leczenia doustnymi kortykosteroidami, które są przepisywane w minimalnych dawkach lub co drugi dzień. Aby zapobiec rozwojowi skutków ubocznych, wysokie dawki kortykosteroidów wziewnych podaje się przez spejser. Krok 5 obejmuje zmniejszenie dawki leków wspomagających. Jest to możliwe, jeśli astma pozostaje pod kontrolą przez co najmniej 3 miesiące, co pozwala zmniejszyć ryzyko wystąpienia działań niepożądanych i zwiększa podatność chorego na zaplanowane leczenie. "Redukcja" leczenia odbywa się pod stałą kontrolą objawów, objawów klinicznych i wskaźników funkcji oddechowych poprzez stopniowe zmniejszanie (anulowanie) ostatniej dawki lub dodatkowych leków. Zatrzymywanie ataków. Łagodny atak można leczyć w domu za pomocą krótko działających leków rozszerzających oskrzela. Leczenie prowadzi się do całkowitego ustąpienia objawów. Umiarkowane i ciężkie ataki wymagają nie tylko odpowiednich dawek krótko działających leków rozszerzających oskrzela (wziewnych β2-krótko działający agoniści), ale także wyznaczenie ogólnoustrojowych kortykosteroidów. Jeśli pacjent ma hipoksemię, należy podać tlen. W leczeniu ataków astmy w ośrodku medycznym lub szpitalu wysokie dawki wziewnego β2agonistów przez nebulizator. Bardzo skuteczne jest stosowanie inhalatora aerozolowego z odmierzaną dawką przez spejser. Korzystnie kortykosteroidy podaje się doustnie, a nie dożylnie. Stosując teofilinę lub aminofilinę w połączeniu z dużymi dawkami β2-agoniści dodatkowe działanie rozszerzające oskrzela nie jest zapewnione, ale zwiększa się ryzyko wystąpienia działań niepożądanych. Teofiliny można stosować tylko w przypadku braku β2Agoniści mogą być jednak podawani dożylnie w dawce 6 mg/kg aminofiliny (lub 5 mg/kg teofiliny) ze stałą dawką 0,5-1,0 mg/kg na godzinę przez 24 godziny.2Agoniści krótko działający mogą również stosować epinefrynę, ale przy jej stosowaniu możliwe są znaczne skutki uboczne. W leczeniu ataków astmy nie zaleca się stosowania wziewnych leków mukolitycznych, uspokajających i przeciwhistaminowych, siarczanu magnezu, fizjoterapii klatki piersiowej, nawadniania dużą ilością płynów u dorosłych i starszych dzieci, aby uniknąć nasilenia kaszlu. profilaktyka. Profilaktyka pierwotna astmy obejmuje leczenie pacjentów w stanie przedastmowym, identyfikację defektów biologicznych u praktycznie zdrowych osób z wywiadem rodzinnym, stwarzających zagrożenie wystąpieniem astmy, eliminację potencjalnie niebezpiecznych alergenów, substancji drażniących i innych czynników ze środowiska środowiska pacjentów, które mogą prowadzić do rozwoju choroby. W leczeniu pacjentów w stanie przedastmatycznym konieczne jest odkażenie ognisk infekcji, leczenie alergicznej rinozinusopatii, zastosowanie różnych metod leczenia nielekowego, w tym akupunktury i psychoterapii, terapii ruchowej, baroterapii i leczenia uzdrowiskowego. Przedstawiono przeprowadzanie odczulania specyficznego i niespecyficznego. WYKŁAD nr 7. Choroby układu oddechowego. Przewlekłe zapalenie oskrzeli Przewlekłe obturacyjne zapalenie oskrzeli jest rozlaną niealergiczną zmianą zapalną drzewa oskrzelowego, spowodowaną długotrwałym działaniem drażniącym na oskrzela różnymi czynnikami, która ma postępujący przebieg i charakteryzuje się obturacyjną wentylacją płucną, tworzeniem śluzu i funkcją drenażową oskrzeli drzewo, które objawia się kaszlem, plwociną i dusznością. Zgodnie z definicją WHO, jeśli pacjent przez większość dni kaszle plwociną przez co najmniej 3 kolejne miesiące przez ponad 2 kolejne lata, chorobę uważa się za przewlekłe zapalenie oskrzeli (CB). Przewlekłe zapalenie oskrzeli dzieli się na pierwotne i wtórne. Pierwotne przewlekłe zapalenie oskrzeli jest niezależną chorobą, która nie jest związana z innymi procesami oskrzelowo-płucnymi lub uszkodzeniem innych narządów i układów, w której występuje rozlana zmiana w drzewie oskrzelowym. Wtórna CB rozwija się na tle innych chorób - zarówno płucnych (gruźlica, rozstrzenie oskrzeli itp.), Jak i pozapłucnych (mocznica, zastoinowa niewydolność serca itp.). Najczęściej ma charakter lokalny (segmentowy). Rozważ pierwotną HB. Etiologia. Zarówno czynniki egzogenne (dym tytoniowy, zanieczyszczenie powietrza, niekorzystne warunki zawodowe, czynniki klimatyczne i zakaźne), jak i czynniki endogenne (patologia nosogardzieli, zaburzenia oddychania przez nos, nawracające ostre choroby układu oddechowego, ostre zapalenie oskrzeli i ogniskowe zakażenie górnych dróg oddechowych) odgrywają rolę w rozwoju szlaków CB, predyspozycji dziedzicznych, zaburzeń metabolicznych (otyłość)). Patogeneza. Pod wpływem czynników egzogennych i przy udziale czynników endogennych drzewa tchawiczo-oskrzelowego zmieniają się właściwości strukturalne i funkcjonalne błony śluzowej i warstwy podśluzowej, rozwija się stan zapalny błony śluzowej, zaburzona zostaje drożność i funkcja drenażowa oskrzeli. Zmiany strukturalne i czynnościowe w błonie śluzowej i warstwie podśluzówkowej wyrażają się hiperplazją i nadczynnością komórek kubkowych, gruczołów oskrzelowych, nadmiernym wydzielaniem gęstego i lepkiego śluzu, co prowadzi do zaburzeń w systemie transportu śluzowo-rzęskowego. Zmniejsza się ilość wydzielniczego lizozymu IgA i laktoferyny. Rozwija się obrzęk błony śluzowej, a następnie - atrofia i metaplazja nabłonka. Zapalenie błony śluzowej jest spowodowane różnymi czynnikami drażniącymi w połączeniu z infekcją (wirusową i bakteryjną). Substancje chemiczne (zanieczyszczenia) zawarte w powietrzu mają szkodliwy wpływ na drogi oddechowe, dochodzi do obrzęku błony śluzowej i zahamowania aktywności nabłonka rzęskowego. Prowadzi to do naruszenia ewakuacji i zmniejszenia funkcji barierowej błony śluzowej oskrzeli. Treść kataralna jest zastępowana przez katarowo-ropną, a następnie ropną. Rozprzestrzenianie się procesu zapalnego na dystalne odcinki drzewa oskrzelowego zaburza wytwarzanie środka powierzchniowo czynnego i zmniejsza aktywność makrofagów pęcherzykowych, które fagocytują obce cząstki. Jeśli skurcz oskrzeli, który występuje w przypadku zapalenia, jest wyraźny, rozwija się składnik oskrzeli (niealergiczny). Związane z tym zakażenie podczas zaostrzenia stanu zapalnego przyczynia się do rozwoju komponentu astmatycznego (alergicznego), co umożliwia przypisanie takiej CB do stanu przed astmą. Zespół obturacyjny rozwija się w wyniku połączenia wielu czynników: 1) skurcz mięśni gładkich oskrzeli w wyniku drażniącego działania czynników egzogennych i zmian zapalnych błony śluzowej; 2) nadmierne wydzielanie śluzu, zmiany jego właściwości reologicznych, prowadzące do zakłócenia transportu śluzowo-rzęskowego i zablokowania oskrzeli lepką wydzieliną; 3) metaplazja nabłonka od cylindrycznego do wielowarstwowego płaskonabłonkowego i jego przerost; 4) naruszenia produkcji środka powierzchniowo czynnego; 5) obrzęk zapalny i naciek błony śluzowej; 6) zapadnięcie się małych oskrzeli i zatarcie oskrzelików; 7) zmiany alergiczne w błonie śluzowej. Jeśli w proces zaangażowane są oskrzela dużego kalibru (proksymalne zapalenie oskrzeli), nie występuje niedrożność oskrzeli. Ale w przypadku uszkodzenia małych i średnich oskrzeli dochodzi do wyraźnego naruszenia drożności oskrzeli. Jednak przy izolowanej zmianie małych oskrzeli (dystalne zapalenie oskrzeli), pozbawionej receptorów kaszlowych, duszność może być jedynym objawem rozwiniętego zapalenia oskrzeli, a kaszel pojawia się, gdy w proces zaangażowane są większe oskrzela. Różne stosunki zmian w błonie śluzowej powodują powstawanie pewnej postaci klinicznej: 1) w przypadku nieobturacyjnego nieobturacyjnego zapalenia oskrzeli przeważają powierzchowne zmiany właściwości strukturalnych i funkcjonalnych błony śluzowej; 2) w przypadku śluzowo-ropnego (ropnego) zapalenia oskrzeli dominują procesy zakaźnego zapalenia. Jednak możliwa jest również sytuacja, w której długotrwałe nieżytowe zapalenie oskrzeli z powodu dodania infekcji może stać się śluzowo-ropne itp. W nieobturacyjnej odmianie wszystkich klinicznych postaci przewlekłego zapalenia oskrzeli zaburzenia wentylacji są nieznacznie nasilone; 3) zaburzenia obturacyjne początkowo pojawiają się tylko na tle zaostrzenia choroby i są spowodowane zmianami zapalnymi w oskrzelach, hiper- i dyskrynii, skurczem oskrzeli (odwracalne elementy niedrożności), ale potem utrzymują się stale, podczas gdy zespół obturacyjny rośnie powoli. W przewlekłym obturacyjnym zapaleniu oskrzeli dominuje pogrubienie błony śluzowej i warstwy podśluzowej, obrzęk i nadmierne wydzielanie, a także uporczywe zaburzenia wentylacji. Rozwinięta niedrożność małych oskrzeli prowadzi do rozedmy płuc. W swoim przebiegu HB przechodzi pewną ewolucję. W wyniku rozwoju rozedmy płuc i pneumosklerozy obserwuje się nierównomierną wentylację płuc, tworzą się obszary hiper- i hipowentylowane. W połączeniu z miejscowymi zmianami zapalnymi prowadzi to do upośledzenia wymiany gazowej, niewydolności oddechowej, hipoksemii tętniczej i nadciśnienia płucnego, a następnie do rozwoju głównego stanu zagrożenia życia – niewydolności prawej komory. Klasyfikacja. Obecnie nie ma ogólnie przyjętej klasyfikacji CB. Ważne jest, aby podzielić CB na warianty obturacyjne i nieobturacyjne, z których każdy może rozwinąć nieżytowy (śluzowy), nieżytowo-ropny lub ropny proces zapalny. Klasyfikacja obejmuje również rzadkie formy - krwotoczną i włóknikową CB. W zależności od stopnia uszkodzenia oskrzeli wyróżniają się: z dominującą zmianą, dużymi oskrzelami (proksymalne zapalenie oskrzeli) iz dominującą zmianą małych oskrzeli (dystalne zapalenie oskrzeli) (N. R. Paleev, 1985). Obraz kliniczny. Głównymi objawami CB są kaszel, wytwarzanie plwociny i duszność. Podczas zaostrzenia choroby lub z powodu niedotlenienia z rozwojem niewydolności płuc i innych powikłań identyfikuje się objawy ogólne (pocenie się, osłabienie, podwyższona temperatura ciała, zmęczenie itp.). Kaszel jest najbardziej typowym objawem choroby. Na podstawie charakteru i konsystencji plwociny można założyć wariant przebiegu choroby. W nieobturacyjnej wersji nieżytowego zapalenia oskrzeli kaszlowi towarzyszy wydzielanie niewielkiej ilości śluzowej, wodnistej plwociny (zwykle rano, po wysiłku fizycznym lub w wyniku wzmożonego oddychania). Na początku choroby kaszel nie przeszkadza pacjentowi; pojawienie się napadowego kaszlu wskazuje na rozwój niedrożności oskrzeli. Kaszel przybiera charakter szczekania i ma charakter napadowy z wyraźnym zapadnięciem się tchawicy i dużych oskrzeli podczas wydechu. W przypadku ropnego i śluzowo-ropnego zapalenia oskrzeli pacjenci bardziej martwią się odkrztuszaniem plwociny. W przypadku zaostrzenia choroby plwocina nabiera charakteru ropnego, jej ilość wzrasta, czasami plwocina jest z trudem wydalana (z powodu niedrożności oskrzeli podczas zaostrzenia). W obturacyjnym wariancie zapalenia oskrzeli kaszel jest nieproduktywny i hacking, któremu towarzyszy duszność, z niewielką ilością plwociny. Duszność występuje u wszystkich pacjentów z przewlekłym zapaleniem oskrzeli w różnym czasie. Pojawienie się duszności u pacjentów z "długotrwałym kaszlem" początkowo ze znacznym wysiłkiem fizycznym wskazuje na dodanie niedrożności oskrzeli. W miarę postępu choroby duszność staje się bardziej wyraźna i stała, tj. rozwija się niewydolność oddechowa (płucna). W wariancie nieobturacyjnym CB postępuje powoli, duszność zwykle pojawia się po 20-30 latach od zachorowania. Tacy pacjenci prawie nigdy nie naprawiają początku choroby, a jedynie wskazują na pojawienie się powikłań lub częstych zaostrzeń. Istnieje historia nadwrażliwości na zimno, a większość pacjentów zgłasza długotrwałe palenie. U wielu pacjentów choroba wiąże się z zagrożeniami zawodowymi w miejscu pracy. Analizując historię kaszlu, należy upewnić się, że pacjent nie ma innej patologii aparatu oskrzelowo-płucnego (gruźlica, guzy, rozstrzenie oskrzeli, pylica płuc, choroby ogólnoustrojowe tkanki łącznej itp.), której towarzyszą te same objawy. Czasami historia wskazuje na krwioplucie z powodu łagodnej wrażliwości błony śluzowej oskrzeli. Nawracające krwioplucie wskazuje na krwotoczną postać zapalenia oskrzeli. Ponadto krwioplucie w przewlekłym, długotrwałym zapaleniu oskrzeli może być pierwszym objawem raka płuca lub rozstrzenia oskrzeli. diagnostyka. Osłuchiwanie ujawnia ciężki oddech (wraz z rozwojem rozedmy płuc może zostać osłabiony) i suchy świszczący oddech o rozproszonym charakterze, którego barwa zależy od kalibru dotkniętych oskrzeli (świszczący oddech, dobrze słyszalny przy wydechu, jest charakterystyczny dla uszkodzenia małych oskrzeli ). Zmiany w danych osłuchowych będą minimalne w przewlekłym nieobturacyjnym zapaleniu oskrzeli w okresie remisji i najbardziej wyraźne podczas zaostrzenia procesu (mokre rzężenia różnych kalibrów, które mogą zniknąć po dobrym kaszlu i odkrztuszeniu plwociny). Wraz z zaostrzeniem obturacyjnego zapalenia oskrzeli wzrasta duszność, nasila się zjawisko niewydolności oddechowej. Ropny, lepki sekret dodatkowo komplikuje drożność oskrzeli. Składnik obturacyjny, który dołączył zarówno do nieżytowych, jak i śluzowo-ropnych postaci zapalenia oskrzeli, a także w okresie zaostrzenia lub w trakcie ich ewolucji, znacznie pogarsza przebieg zapalenia oskrzeli. Oznaki niedrożności oskrzeli: wydłużenie fazy wydechowej przy spokojnym i szczególnie wymuszonym oddychaniu; świszczący oddech przy wydechu (lepiej osłuchiwany przy wymuszonym oddychaniu iw pozycji leżącej); objawy obturacyjnej rozedmy płuc. W zaawansowanych przypadkach przewlekłego zapalenia oskrzeli i z dodatkowymi powikłaniami pojawiają się objawy rozedmy płuc, niewydolności oddechowej i serca (prawej komory) - pojawiają się niewyrównane serce płucne: akrocyjanoza, stwardnienie lub obrzęk nóg i stóp, zmiany w obrębie paznokci forma okularów zegarkowych i końcowych paliczków dłoni i stóp - w postaci pałeczek perkusyjnych, obrzęk żył szyjnych, pulsacja w nadbrzuszu z powodu prawej komory, akcent II tonu w II międzyżebrowym przestrzeń po lewej stronie mostka, powiększenie wątroby. Wpływa na obraz choroby i dodanie składnika astmatycznego (alergicznego), gdy występuje podobieństwo do astmy oskrzelowej. Wskaźniki laboratoryjne i instrumentalne mają różny stopień istotności w zależności od etapu procesu. W początkowym okresie choroby lub w fazie remisji zmiany mogą nie występować. Jednak te wskaźniki mają ogromne znaczenie dla identyfikacji aktywności procesu zapalnego; wyjaśnienie klinicznej postaci choroby; identyfikacja powikłań; diagnostyka różnicowa z chorobami o podobnych objawach klinicznych. Badanie rentgenowskie narządów klatki piersiowej jest wykonywane u wszystkich pacjentów z przewlekłym zapaleniem oskrzeli, jednak na zwykłych zdjęciach radiologicznych z reguły nie stwierdza się zmian w płucach. Może wystąpić deformacja siatki wzoru płuc z powodu rozwoju pneumosklerozy. Wraz z długim przebiegiem procesu ujawniają się oznaki rozedmy płuc. Wraz z rozwojem serca płucnego na lewym obrysie cienia serca pojawia się wybrzuszenie pnia tętnicy płucnej, rozszerzenie tętnic podstawnych, a następnie ich stożkowate zwężenie i zmniejszenie średnicy tętnicy płucnej. gałęzie peryferyjne. Badanie rentgenowskie odgrywa ważną rolę w diagnostyce powikłań (ostre zapalenie płuc, rozstrzenie oskrzeli) oraz w diagnostyce różnicowej chorób o podobnych objawach. Bronchografia służy wyłącznie do diagnozowania rozstrzenia oskrzeli. Bronchoskopia ma ogromne znaczenie w diagnostyce przewlekłego zapalenia oskrzeli i jego różnicowaniu z chorobami o podobnym obrazie klinicznym. Potwierdza obecność procesu zapalnego; wyjaśnia charakter zapalenia (rozpoznanie krwotocznego lub włóknikowego zapalenia oskrzeli następuje dopiero po tym badaniu); ujawnia zaburzenia czynnościowe drzewa tchawiczo-oskrzelowego (szczególnie ważne jest zidentyfikowanie zapaści wydechowej - dyskinezy tchawicy i dużych oskrzeli); pomaga w identyfikacji zmian organicznych drzewa oskrzelowego. Dodatkowo bronchoskopia pozwala na pobranie zawartości oskrzeli lub popłuczyn do badań mikrobiologicznych, parazytologicznych i cytologicznych. Badanie funkcji oddychania zewnętrznego prowadzi się w celu identyfikacji restrykcyjnych i obturacyjnych zaburzeń wentylacji płuc. Zgodnie ze spirogramem obliczany jest indeks Tiffno (stosunek wymuszonej objętości wydechowej w 1 s - FEV1 do pojemności życiowej płuc - VC w procentach) i wskaźnik prędkości powietrza - PSV (stosunek maksymalnej wentylacji płuc - MVL do VC). Wraz z rozwojem zespołu obturacyjnego następuje spadek bezwzględnych wskaźników prędkości oddychania zewnętrznego (MVL i FEV1), przekroczenie stopnia redukcji VC; spada indeks Tiffno i wzrasta oskrzelowa odporność na wydech. Według pneumotachometrii przewaga mocy wdechu nad mocą wydechu objawia się jako wczesny objaw obturacji oskrzeli. Identyfikacja naruszeń drożności oskrzeli na różnych poziomach drzewa oskrzelowego jest możliwa za pomocą specjalnych pneumotachografów, które umożliwiają uzyskanie krzywej „przepływ - objętość”. Niedrożność obwodowa charakteryzuje się znacznym spadkiem krzywej przepływ-objętość w obszarze małej objętości. Łączna ocena oporności oskrzeli i objętości płuc również pomaga w określeniu stopnia niedrożności. W przypadku niedrożności na poziomie dużych oskrzeli następuje wzrost objętości resztkowej płuc (RLV), a całkowita pojemność płuc (TLC) nie wzrasta. W przypadku niedrożności obwodowej obserwuje się bardziej znaczący wzrost TRL i wzrost TRL. Aby określić udział skurczu oskrzeli w całkowitym udziale niedrożności oskrzeli, po serii testów farmakologicznych bada się mechanikę wentylacji i oddychania. Po inhalacji aerozoli rozszerzających oskrzela sprawność wentylacji poprawia się w obecności spastycznego komponentu niedrożności dróg oddechowych. Radiopulmonografia z użyciem radioaktywnego izotopu 133Xe jest wykonywana w celu wykrycia nierównej wentylacji związanej z niedrożnością małych oskrzeli. Jest to najwcześniejszy objaw diagnostyczny tego typu niedrożności oskrzeli. Elektrokardiografia jest niezbędna do wykrycia przerostu prawej komory i prawego przedsionka, który rozwija się wraz z nadciśnieniem płucnym. Wyraźne odchylenie osi QRS w prawo, przesunięcie strefy przejściowej w lewo (R / S < 1 w V4-V6), EKG typu S; wysoka ostra fala P w odprowadzeniach VF, III, II. W badaniu klinicznym krwi stwierdza się wtórną erytrocytozę będącą wynikiem przewlekłego niedotlenienia z rozwojem ciężkiej niewydolności płuc. Wskaźniki „ostrej fazy” są wyrażane umiarkowanie: ESR jest normalne lub umiarkowanie podwyższone, leukocytoza jest niewielka, a także przesunięcie formuły leukocytów w lewo. Jako dowód objawów alergicznych możliwa jest eozynofilia. Badanie zawartości plwociny i oskrzeli pomaga w ustaleniu ciężkości stanu zapalnego. Przy ciężkim zapaleniu zawartość jest ropna lub ropna śluzowa, zawiera wiele neutrofili i pojedynczych makrofagów, słabo reprezentowane są dystroficznie zmienione komórki nabłonka rzęskowego i płaskonabłonkowego. Umiarkowane zapalenie charakteryzuje się treścią bliższą śluzowo-ropnej; zmniejsza się liczba neutrofili, wzrasta liczba makrofagów, śluzu i komórek nabłonka oskrzeli. Przy łagodnym zapaleniu treścią oskrzeli są śluzowe, dominują złuszczone komórki nabłonka i oskrzeli; makrofagi i neutrofile są nieliczne. Badanie mikrobiologiczne plwociny i treści oskrzelowej jest ważne dla określenia etiologii zaostrzenia przewlekłego zapalenia oskrzeli i wyboru terapii przeciwdrobnoustrojowej. Diagnostyka różnicowa. Tabela 10 Różnicowe kryteria diagnostyczne dla CB
Leczenie. Obejmuje zestaw środków różniących się w okresie zaostrzenia i remisji choroby. W okresie zaostrzenia choroby przewlekłej wyróżnia się dwa kierunki leczenia: etiotropowy i patogenetyczny. Leczenie etiotropowe ma na celu wyeliminowanie procesu zapalnego w oskrzelach: wskazana jest terapia antybiotykami, lekami sulfanilamidowymi, antyseptycznymi, fitoncydami itp. Leczenie rozpoczyna się od antybiotyków z serii penicylin (penicylina, ampicylina) lub grupy cefalosporyn (cefamezyna , tseporin), a przy braku efektu stosuje się rezerwę antybiotyków z grupy (gentamycyna itp.). Najkorzystniejszą drogą podania jest droga dotchawicza (aerozol lub napełnienie strzykawką krtaniową przez bronchoskop). Leczenie patogenetyczne ma na celu poprawę wentylacji płuc; przywrócenie drożności oskrzeli; kontrola nadciśnienia płucnego i niewydolności prawej komory. Przywrócenie wentylacji płucnej, oprócz eliminacji procesu zapalnego w oskrzelach, ułatwia tlenoterapia i terapia ruchowa. Najważniejsze w leczeniu przewlekłego zapalenia oskrzeli - przywrócenie drożności oskrzeli - osiąga się poprzez poprawę ich drenażu i wyeliminowanie skurczu oskrzeli. Aby poprawić drenaż oskrzeli, przepisuje się środki wykrztuśne (gorący napój alkaliczny, wywary z ziół, mukaltin itp.), leki mukolityczne (acetylocysteina, bromheksyna; z ropną lepką wydzieliną - aerozole enzymów proteolitycznych - chymopsin, trypsyna); stosuje się bronchoskopię terapeutyczną. Aby wyeliminować skurcz oskrzeli, stosuje się eufilinę (dożylnie, w czopkach, tabletkach), efedrynę, atropinę; możliwe są pojedyncze wizyty w aerozolu leków sympatykomimetycznych: fenoterol, siarczan orcyprenaliny (astmopenta) i nowy lek domowy „Soventol”, leki antycholinergiczne: atrovent, troventol. Skuteczne preparaty przedłużonej aminofiliny (teopec, teodur, theobelong itp.) - 2 razy dziennie. W przypadku braku efektu takiej terapii, małe dawki kortykosteroidów podaje się doustnie (10-15 mg prednizolonu dziennie) lub dotchawiczo (zawiesina hydrokortyzonu - 50 mg). Jako dodatkową terapię przepisywane są: 1) leki przeciwkaszlowe: z bezproduktywnym kaszlem - libexin, tusuprex, bromheksyna, z kaszlem hackingiem - kodeina, dionina, stoptussin; 2) leki zwiększające odporność organizmu: witaminy A, C, grupa B, stymulanty biogenne. Obecnie w leczeniu przewlekłego zapalenia oskrzeli coraz częściej stosuje się leki immunokorekcyjne: T-aktywinę lub tymalinę (100 mg podskórnie przez 3 dni); wewnątrz - katergen, nukleinian sodu lub pentoksyl (w ciągu 2 tygodni), lewamizol (dekaris). Zabieg fizjoterapeutyczny: przepisać diatermię, elektroforezę chlorku wapnia, kwarc na klatkę piersiową, masaż klatki piersiowej i ćwiczenia oddechowe. Przy umiarkowanym i ciężkim zapaleniu oskrzeli, wraz z leczeniem przeciwnawrotowym i sanatoryjnym, wielu pacjentów jest zmuszonych do ciągłego przyjmowania leków wspomagających. Terapia podtrzymująca ma na celu poprawę drożności oskrzeli, zmniejszenie nadciśnienia płucnego oraz walkę z niewydolnością prawej komory. Te same leki są przepisywane jak w okresie zaostrzenia, tylko w mniejszych dawkach, na kursach. Prognoza. Prognozy dotyczące całkowitego wyzdrowienia są niekorzystne. Najmniej korzystne rokowanie dotyczy CB obturacyjnej i CB z dominującym uszkodzeniem dystalnych oskrzeli, co szybko prowadzi do rozwoju niewydolności płuc i powstania serca płucnego. Najkorzystniejsze rokowanie dotyczy powierzchownego (nieżytowego) CB bez niedrożności. WYKŁAD nr 8. Choroby układu oddechowego. Zapalenie płuc Zapalenie płuc jest ostrą chorobą zakaźną i zapalną o charakterze ogniskowym, w której w proces patologiczny zaangażowane są sekcje oddechowe i śródmiąższowa tkanka łączna płuc. Klasyfikacja według EV Gembitsky'ego (1983). Według etiologii: 1) bakteryjny (wskazujący na patogen); 2) wirusowy (wskazujący na patogen); 3) zrogowaciały; 4) riketsjalny; 5) mykoplazma; 6) grzybicze; 7) mieszane; 8) zakaźno-alergiczny; 9) nieznana etiologia. Według patogenezy: 1) pierwotny (niezależny ostry proces zapalny); 2) wtórne (powikłania chorób układu sercowo-naczyniowego z zaburzeniami krążenia w krążeniu płucnym, przewlekłe choroby nerek, układu krwionośnego, przemiany materii, choroby zakaźne lub rozwijają się na tle przewlekłych chorób układu oddechowego). Charakterystyka kliniczna i morfologiczna: 1) miąższowy (w przypadku pneumokokowego zapalenia płuc): krupowaty; ogniskowy; 2) pełnoekranowy. Według lokalizacji i zasięgu: jednostronne; dwustronny. Według ciężkości: wyjątkowo ciężki; ciężki; umiarkowany; łagodny i nieudany. Downstream: ostry; przedłużony (radiologiczne i kliniczne ustąpienie zapalenia płuc). Etiologia. Większość zapaleń płuc ma podłoże zakaźne. Alergiczne zapalenie płuc oraz wywołane czynnikami fizycznymi lub chemicznymi są rzadkie. Bakteryjne zapalenie płuc diagnozuje się częściej u osób w średnim i starszym wieku; wirusowe zapalenie płuc - u młodych ludzi. W etiologii pierwotnego bakteryjnego zapalenia płuc wiodącą rolę odgrywają pneumokoki. W czasie epidemii grypy wzrasta rola zespołów wirusowo-bakteryjnych (najczęściej gronkowców), a także mikroorganizmów oportunistycznych. We wtórnym zapaleniu płuc wiodącą rolę etiologiczną odgrywają bakterie Gram-ujemne (klebsiella pneumonia i pałeczka grypy); w występowaniu zachłystowego zapalenia płuc duże znaczenie ma infekcja beztlenowa. Patogeneza. Zakaźny patogen wchodzi z zewnątrz do dróg oddechowych płuc przez oskrzela: wdychanie i aspiracja (z nosogardła lub jamy ustnej i gardła). Drogą krwiopochodną patogen przedostaje się do płuc głównie podczas wtórnego zapalenia płuc lub podczas zakrzepowej genezy zapalenia płuc. Limfogenne rozprzestrzenianie się infekcji z występowaniem zapalenia płuc obserwuje się tylko w przypadku ran klatki piersiowej. Istnieje również endogenny mechanizm rozwoju stanu zapalnego w tkance płucnej, ze względu na aktywację mikroflory w płucach. Jego rola jest świetna we wtórnym zapaleniu płuc. Rozwój zapalenia płuc jest promowany przez niekorzystne czynniki środowiska zewnętrznego i wewnętrznego, pod wpływem których następuje spadek ogólnej niespecyficznej odporności organizmu (tłumienie fagocytozy, wytwarzanie bakteriolizyn itp.) oraz tłumienie miejscowych mechanizmy obronne (upośledzony klirens śluzowo-rzęskowy, zmniejszenie aktywności fagocytarnej makrofagów pęcherzykowych i neutrofili itp.) . Duże znaczenie w patogenezie zapalenia płuc mają także reakcje alergiczne i autoalergiczne. Saprofity i patogenne mikroorganizmy, stając się antygenami, przyczyniają się do wytwarzania przeciwciał, które są utrwalane na komórkach błony śluzowej dróg oddechowych, gdzie zachodzi reakcja antygen-przeciwciało, co prowadzi do uszkodzenia tkanek i rozwoju procesu zapalnego. W obecności wspólnych determinant antygenowych mikroorganizmów i tkanki płucnej lub jeśli tkanka płucna jest uszkodzona przez wirusy, mikroorganizmy, toksyny i substancje toksyczne, co prowadzi do manifestacji jej właściwości antygenowych, rozwijają się procesy autoalergiczne. Procesy te przyczyniają się do dłuższego istnienia zmian patologicznych i przedłużającego się przebiegu choroby. Obraz kliniczny. Główne syndromy: 1) zatrucie (ogólne osłabienie, zmęczenie, bóle głowy i mięśni, duszność, kołatanie serca, bladość, utrata apetytu); 2) zespół ogólnych zmian zapalnych (uczucie gorąca, dreszcze, gorączka, zmiany parametrów ostrej fazy krwi: leukocytoza z przesunięciem wzoru leukocytów w lewo, wzrost OB, poziom fibrynogenu, α2-globuliny, pojawienie się białka C-reaktywnego); 3) zespół zmian zapalnych w tkance płucnej (pojawienie się kaszlu i plwociny, skrócenie odgłosu opukiwania), nasilenie drżenia głosu i oskrzeli, zmiany częstotliwości i charakteru oddychania, pojawienie się wilgotnych rzęsek, zmiany radiologiczne; 4) zespół zajęcia innych narządów i układów. Nasilenie tych objawów charakteryzuje ciężkość przebiegu zapalenia płuc (patrz Tabela 11). Tabela 11 Objawy i przebieg zapalenia płuc
W różnych stadiach przebiegu zapalenia płuc obraz kliniczny może się zmieniać z powodu dodania pewnych powikłań: płucnych i pozapłucnych. Płucne: tworzenie ropni; zapalenie opłucnej (para- i metapneumoniczne), rzadziej - ropniak opłucnej; możliwe jest przystąpienie składnika astmatycznego, powstanie obrzęku płuc i rozwój ostrej niewydolności oddechowej. Powikłania pozapłucne: wstrząs zakaźny toksyczny (z objawami ostrej niewydolności naczyniowej, ostrej niewydolności lewej komory i nerek, owrzodzenia błony śluzowej przewodu pokarmowego i krwawienia, rozwoju rozsianego wykrzepiania śródnaczyniowego; infekcyjno-alergicznego zapalenia mięśnia sercowego; infekcyjnego zapalenia wsierdzia; zapalenia osierdzia; zapalenie opon mózgowo-rdzeniowych lub zapalenie opon mózgowo-rdzeniowych, zapalenie nerek, zapalenie wątroby W ciężkim krupowym zapaleniu płuc możliwy jest rozwój psychoz zatrucia, aw zlewnym całkowitym zapaleniu płuc - ostre serce płucne. Główne dolegliwości pacjenta z zapaleniem płuc: kaszel, wydzielanie plwociny, ból w klatce piersiowej, nasilone oddychaniem i kaszlem, duszność, pogorszenie ogólnego samopoczucia, gorączka. Kaszel może być suchy lub z plwociną (śluzową, śluzowo-ropną, ropno-śluzową, krwawą). "Rdzawa" plwocina jest charakterystyczna dla płatowego zapalenia płuc, krwawa - na zapalenie płuc wywołane przez Klebsiella (różdżka Fridlandera) i wirusowe; ropna krwawa plwocina wskazuje na zapalenie płuc pochodzenia paciorkowcowego. Utrzymujący się kaszel z niewielką ilością śluzowo-ropnej plwociny obserwuje się przy mykoplazmalnym zapaleniu płuc, które charakteryzuje się również uczuciem bólu w gardle. Ból w boku, nasilany głębokim oddychaniem i kaszlem, jest charakterystyczny dla pneumokokowego zapalenia płuc, a także zaangażowania opłucnej w proces patologiczny. Wraz z lokalizacją zapalenia płuc w dolnych partiach płuc i zaangażowaniem w ten proces opłucnej przeponowej ból może promieniować do jamy brzusznej, symulując obraz ostrego brzucha. Jeśli w proces zaangażowany jest górny lub dolny segment trzcinowy lewego płuca, bóle są zlokalizowane w okolicy serca. U 25% pacjentów skarga na duszność jest jedną z głównych, zwłaszcza w przypadku zapalenia płuc, które rozwinęło się na tle przewlekłych chorób układu oddechowego i niewydolności serca. Nasilenie duszności wzrasta równolegle z naruszeniem ogólnego samopoczucia. Objawy ciężkiego zatrucia są najbardziej charakterystyczne dla zrogowaciałego i mykoplazmalnego zapalenia płuc, a także obserwuje się je w gronkowcowym, grypie i pneumokokowym (zakrzywionym) zapaleniu płuc. Pacjent może być zaniepokojony dreszczami i wzrostem temperatury ciała do gorączki. Na ogólnym tle zatrucia i gorączki pojawiają się objawy miejscowe. diagnostyka. Aby postawić diagnozę etiologiczną, ważna jest prawidłowa ocena objawów choroby już na jej początku. Chrypka lub niemożność mówienia jest charakterystyczna dla zapalenia płuc wywołanego wirusem paragrypy. Łzawienie, ból oczu, ból gardła podczas połykania, obfite wydzieliny z nosa bez zmiany innych odcinków dróg oddechowych występują przy zapaleniu płuc wywołanym adenowirusem. Najistotniejsze dla diagnozy jest obecność zespołu zmian zapalnych w tkance płucnej. Zespół ten składa się z następujących objawów: 1) opóźnienie w oddychaniu dotkniętej chorobą strony klatki piersiowej; 2) skrócenie dźwięku perkusyjnego w obszarze projekcji zmiany w większym lub mniejszym stopniu; 3) wzmożone drżenie głosu i bronchofonia w tym samym obszarze; 4) zmiana charakteru oddychania (twardy, oskrzelowy, osłabiony itp.); 5) pojawienie się patologicznych odgłosów oddechowych (mokre, dźwięczne, drobne bulgoczące rzęsy i trzeszczenie). Natura oddychania może się zmieniać na różne sposoby. W początkowej fazie krupowego zapalenia płuc oddychanie może być osłabione, z przedłużonym wydechem; w fazie hepatyzacji wraz ze wzrostem przytępienia dźwięku perkusji słychać oddech oskrzelowy; przy rozdzielczości ogniska płucnego ze spadkiem otępienia perkusyjnego oddychanie staje się trudne. W przypadku ogniskowego zapalenia płuc najbardziej stałymi objawami są trudności w oddychaniu i wilgoć, dzwoniąc na drobne bulgoczące rzężenia. Jednak w przypadku zapalenia płuc ośrodkowej wnęki dane fizykalne są przedstawiane bardzo słabo, a rozpoznanie zapalenia płuc jest możliwe dopiero po badaniu rentgenowskim. Zapalenia płuc wywołane przez Mycoplasma wyróżniają się niedoborem danych fizycznych. W zapaleniu płuc wywołanym przez Klebsiella pneumonia obserwuje się ciężkie zatrucie w połączeniu z bardzo małą liczbą świszczących oddechów. W niektórych przypadkach podczas osłuchiwania na pierwszy plan wysuwa się duża liczba basowo-górnych suchych rzęsek, nietypowa dla zespołu nacieku zapalnego. Dzieje się tak w przypadku zapalenia płuc, które rozwinęło się na tle przewlekłego zapalenia oskrzeli; zapalenie płuc wywołane przez kij Pfeiffera; w przypadku przystąpienia do zapalenia płuc składnika alergicznego. Objawy pomagają postawić diagnozę etiologiczną: 1) wykrycie wysypki o małych plamkach, jak w przypadku różyczki, w połączeniu z limfadenopatią jest charakterystyczne dla infekcji adenowirusem; 2) miejscowe powiększenie węzłów chłonnych wskazuje na okołoogniskowe zapalenie płuc; 3) grzybicze zapalenie płuc połączone ze zmianami błon śluzowych, skóry i paznokci; 4) zespół wątrobowo-płucny i lekka żółtaczka występują w zapaleniu płuc w przebiegu kornitu i Curickettsi; 5) w przypadku typowego krupowego zapalenia płuc charakterystyczny jest wygląd pacjenta: blada twarz z gorączkowym rumieńcem po stronie zmiany, wykwity opryszczkowe, obrzęk skrzydeł nosa podczas oddychania. Najważniejszą metodą wyjaśnienia obecności zapalenia płuc i stopnia zaangażowania tkanki płucnej w proces jest fluorografia wielkoformatowa i badanie rentgenowskie narządów klatki piersiowej. Zapalenia płuc gronkowcowe wyróżniają się wyraźną segmentacją zmian w płucach z udziałem kilku segmentów w procesie. Ich charakterystycznym objawem radiologicznym jest tworzenie się wielu ubytków w płucach typu pneumocele w 5-7 dniu od zachorowania, a później - ubytków martwiczych z obecnością płynu. W przeciwieństwie do prawdziwych ropni, konfiguracja i liczba ubytków zmieniają się szybko. Uszkodzenie płatowe jest przejawem krupowego zapalenia płuc lub zapalenia płuc wywołanego przez Klebsiella. Najczęściej dotyczy to płata górnego, głównie prawego płuca. Badanie rentgenowskie ujawnia wysięk w jamie opłucnej. Często taki wysięk występuje przy paciorkowcowym zapaleniu płuc, przy zapaleniu płuc wywołanym przez pałkę Pfeiffera, która jest zlokalizowana w dolnym płacie i u 2/3 pacjentów wychwytuje więcej niż jeden płat płuca. Dane z badań rentgenowskich są szczególnie ważne w wykrywaniu zapalenia płuc z łagodnymi zmianami osłuchowymi (śródmiąższowe i wnękowe zapalenie płuc). W niektórych przypadkach do wyjaśnienia diagnozy wskazane są tomografia i bronchografia, które pomagają wyjaśnić diagnozę w przypadkach opóźnionej regresji zmian naciekowych o skomplikowanym przebiegu (ropień, wysięk w jamie opłucnej). Służą do wykluczenia innych procesów patologicznych o podobnych obrazach klinicznych i radiologicznych. Bronchografia ujawnia próchnicę w tkance płucnej, a także obecność rozstrzeni oskrzeli, wokół której w czasie zaostrzenia możliwe są zmiany naciekowe (perifocal pneumonia). W diagnostyce zawałowego zapalenia płuc pewną rolę odgrywa radionuklidowe badanie przepływu krwi w płucach, ujawniające jego naruszenia. Badanie bakteriologiczne plwociny (lub popłuczyn oskrzelowych) przed wyznaczeniem antybiotyków pomaga wykryć patogen i określić jego wrażliwość na antybiotyki. Nie zawsze zidentyfikowany mikroorganizm jest przyczyną zapalenia płuc. Dokładniejszą diagnozę etiologiczną można postawić na podstawie badań immunologicznych: reakcji wiązania dopełniacza (RCC) i reakcji hamowania hemaglutynacji (HITA) z antygenami wirusowymi i bakteryjnymi. W diagnostyce wirusowego i wirusowo-bakteryjnego zapalenia płuc ważne są badania wirusologiczne i serologiczne (wyniki badania hodowli plwociny, w tym testu biologicznego na myszach, metoda hodowli wirusów w rozwijającym się zarodku kurzym, metoda immunofluorescencji, metoda serologiczna wykorzystująca sparowane surowice przeciw wirusom, przywiązują wagę tylko do 4-krotnego wzrostu miana przeciwciał). Badanie plwociny pomaga wyjaśnić naturę zapalenia płuc. Duża liczba eozynofili wskazuje na procesy alergiczne, obecność komórek atypowych wskazuje na zapalenie płuc pochodzenia nowotworowego; Mycobacterium tuberculosis występuje w gruźlicy; włókna elastyczne - dowody na zapadnięcie się tkanki płucnej. W przypadku grzybiczego zapalenia płuc, wraz z wykryciem grzybów, odnotowuje się brak flory pyogennej z powodu hamującego działania produktów odpadowych grzybów. Według mikroskopii rozmazów plwociny barwionych metodą Grama możemy mówić o drobnoustrojach Gram-ujemnych lub Gram-dodatnich, które żyją w oskrzelach już w pierwszym dniu pobytu pacjenta w szpitalu. Nasilenie procesu zapalnego ocenia się na podstawie nasilenia parametrów krwi ostrej fazy i ich dynamiki (leukocytoza ze zmianą wzoru leukocytów, wzrost ESR, zwiększona zawartość α2-globuliny, fibrynogen, pojawienie się SRV, wzrost poziomu kwasów sialowych). Przy przedłużającym się przebiegu zapalenia płuc i rozwoju powikłań badana jest reaktywność immunologiczna organizmu. Obniżenie odporności humoralnej (IgM) i komórkowej (opóźniona migracja leukocytów, zmiany w testach charakteryzujących układ limfocytów T) wymaga leczenia immunomodulującego. Leczenie. Natychmiast po rozpoznaniu konieczne jest rozpoczęcie leczenia etiotropowego zapalenia płuc. Empiryczne pomysły na temat możliwego patogenu mają ogromne znaczenie, ponieważ badanie bakteriologiczne plwociny przeprowadza się dość długo i u większości pacjentów, nawet przy nowoczesnym podejściu do tego badania, daje niepewne, a czasem błędne wyniki. Obecnie penicyliny straciły na znaczeniu jako lek z wyboru w leczeniu zapalenia płuc. Wynika to z faktu, że etiologicznie istotne dla rozwoju zapalenia płuc, obok pneumokoków i Haemophilus influenzae, są bezwzględnie wewnątrzkomórkowe mikroorganizmy - Mycoplasma pneumoniae i Chlamydia pneumoniae, które są oporne na bakteriobójcze działanie antybiotyków z grupy β-laktamów. Nie sposób zapomnieć o tym, że u pacjentów szybko rozwija się nadwrażliwość na te leki. W związku z powyższym w leczeniu zapalenia płuc dużą wagę przywiązuje się do makrolidów, które okazały się skuteczne nie tylko przeciwko pneumokokom, ale także przeciwko Mycoplasma pneumoniae, Chlarnydia pneumoniae. Nie należy jednak zapominać o tym, że erytromycyna, która jest standardem w tej grupie leków ze względu na niską stabilność w środowisku kwaśnym (a co za tym idzie niską biodostępność), a także szerokie rozpowszechnienie szczepów pneumokoków opornych do erytromycyny, traci swoje znaczenie kliniczne. Jako leki z wyboru zostały zastąpione innymi lekami z klasy makrolidów - azytromycyną, roksytromycyną, rovamycyną itp. Szereg makrolidów stosuje się również do stosowania doustnego i pozajelitowego (na przykład rovamycyna). W rezultacie ich stosowanie jest uzasadnione w ciężkim przebiegu procesu zapalnego w płucach (na przykład początkowo rovamycynę podaje się dożylnie przez 2-3 dni, a następnie, przy dodatniej dynamice procesu patologicznego, pacjent przechodzi na przyjmowanie tego leku do środka). Zaleta rovamycyny jest niezaprzeczalna, ponieważ nie wchodzi w interakcje z teofilinami, jednocześnie zapobiegając możliwości przedawkowania tych leków, ponieważ teofiliny i rovamycynę stosuje się razem w leczeniu pacjentów z przewlekłymi obturacyjnymi chorobami płuc. Wiadomo również, że ta podgrupa makrolidów (16-członowych makrolidów) to leki o minimalnym poziomie skutków ubocznych. U pacjentów powyżej 65. roku życia, ze względu na niejednorodność etiologicznego spektrum zapalenia płuc i współistniejące przewlekłe obturacyjne choroby płuc, półsyntetyczne penicyliny mogą być stosowane do początkowej antybiotykoterapii, a przy braku pozytywnego efektu po tej terapii na 3-4 dni uzasadnione jest stosowanie cefalosporyn. Należy przypomnieć, że spektrum działania cefalosporyn I i niektórych II generacji to mikroorganizmy Gram-dodatnie i Gram-ujemne, a cefalosporyny III generacji działają głównie na patogeny Gram-ujemne. Cefalosporyny I generacji są reprezentowane przez cefalotynę (Keflin), cefazolinę (Kefzol) itp. Leki II generacji obejmują cefuroksym (Ketocef), cefoksytynę (Boncefin) i inne.Cefalosporyny III generacji: cefotaksym (Claforan), cefoperazon (Cefobid () Longacef). Aspiracyjne zapalenie płuc związane jest z mikroflorą beztlenową lub gram-ujemną, co warunkuje stosowanie aminoglikozydów lub cefalosporyn III generacji w połączeniu z półbursztynianem metronidazolu (500 mg dożylnie 2-3 razy dziennie). Stany niedoboru odporności wpływają również na charakter wybranych leków, który w tym przypadku zależy od charakteru patogenu. W takich przypadkach zastosowany schemat składa się z aminoglikozydów i nowoczesnych cefalosporyn. Czas trwania skutecznej antybiotykoterapii u pacjenta z zapaleniem płuc wynosi 7-10 dni. Przepisując leczenie, należy wziąć pod uwagę, że w 7-15% przypadków ta terapia może nie przynieść efektu. Wskazuje to na potrzebę zastąpienia antybiotyków na podstawie wyników badania mikrobiologicznego. Inną opcją jest stosowanie leków alternatywnych, tzw. antybiotyków drugiego wyboru: nowoczesnych cefalosporyn, imipenemów, monobaktamów, fluorochinolonów. Fluorochinolony (ofloksacyna, pefloksacyna, cyprofloksacyna) są skuteczne przeciwko patogenom Gram-ujemnym, w tym Pseudomonas aeruginosa i niektórym ziarniakom Gram-dodatnim (Staphylococcus aureus), ale są nieaktywne w przypadku ekspozycji na beztlenowce. Fluorochinolony można słusznie uznać za alternatywę dla makrolidów w zakażeniach chlamydiami, legionellą i mykoplazmą. Antybiotyki monobaktamowe w swojej nowoczesnej postaci są reprezentowane przez aztreonam (azactam), który działa głównie na bakterie Gram-ujemne (Salmonella, Shigella, Proteus, Escherichia coli, Klebsiella itp.); i jest również stabilny pod działaniem β-laktamaz. Imipenem - lek przeciwbakteryjny z grupy karbapenemów, przepisywany jest wyłącznie w połączeniu z cylastatyną, która hamuje metabolizm imipenemu. Lek jest wysoce skuteczny przeciwko wielu beztlenowców, Gram-dodatnim ziarniakom i Gram-ujemnym pałeczkom. Dawkowanie antybiotyków stosowanych w leczeniu zapalenia płuc. 1) Penicyliny: penicylina benzylowa (500 000-1 000 000 IU dożylnie co 6-8 godzin lub 500 000-1 000 000 IU co 4 godziny domięśniowo), ampicylina (0,5-1,0-2,0 g domięśniowo co 6-8 godzin lub 0,5 g co 6 godzin dożylnie), amoksycylina (0,5-1,0 g co 8 godzin doustnie lub 0,5-1,0 g co 8-12 godzin domięśniowo, dożylnie), oksacylina (0,5 g co 4-6 godzin doustnie, domięśniowo, dożylnie). 2) Cefalosporyny: I generacja - cefalotyna (keflin) (0,5-2,0 g co 4-6 godzin domięśniowo, dożylnie), cefazolina (kefzol) (0,5-2,0 g, co 8 godzin domięśniowo, dożylnie), II generacja - cefuroksym (zinacef , ketocef) (0,75-1,5 g co 6-8 godzin domięśniowo, dożylnie), III generacja - cefotaksym (klaforan) (1,0-2,0 g, maksymalnie do 12 g/dobę co 12 godzin domięśniowo, dożylnie), ceftriakson (longacef, rocefina) (1,0-2,0-4,0 g co 24 godziny domięśniowo, dożylnie). 3) Aminoglikozydy: genetamycyna (80 mg co 12 godzin domięśniowo, dożylnie), amikacyna (10-15 mg/kg co 12 godzin domięśniowo, dożylnie), tobramycyna (brulamycyna) (3-5 mg/kg co 8 godzin domięśniowo, dożylnie) . 4) Makrolidy: erytromycyna (0,5 g co 6-8 godzin doustnie lub 0,5-1,0 g co 6-8 godzin dożylnie), rovamycyna (3,0 mln j.m. co 8-12 godzin doustnie lub 1,5-3,0 mln j.m. co 8-12 godzin godziny dożylnie). 5) Fluorochinolony: pefloksacyna (leflacyna) (400 mg co 12 godzin doustnie, i.v.), cyprofloksacyna (cyprobay) (500 mg co 12 godzin doustnie lub 200-400 mg co 12 godzin dożylnie), ofloksacyna (zanocyna, tarivid) (200 mg co 12 godzin doustnie). 6) Tetracykliny: doksycyklina (wibramycyna) (200 mg w 1. dobie, w kolejnych dniach – 100 mg co 24 h doustnie), minocyklina (minocyna) (200 mg w 1. dobie, w kolejnych dniach – 100 mg co 12 h doustnie), aztreonam (azactam) (1,0-2,0 g co 8-12 godzin), imipenem/cylstatyna (tienam) (500 mg co 6-8 godzin domięśniowo). Istotne jest również to, że z reguły przedłużający się lub postępujący przebieg choroby wynika z niedostatecznej początkowej antybiotykoterapii. Jednak oprócz tego istnieje szereg lokalnych i ogólnoustrojowych przyczyn, które prowadzą do długiego i uporczywego przebiegu stanu zapalnego w płucach: są to miejscowa niedrożność dróg oddechowych (rak, gruczolak, zablokowanie śluzówki itp.); rozstrzenie oskrzeli (wrodzone, nabyte); mukowiscydoza; wady układu odpornościowego (nabyte); nawracająca aspiracja (achalazja, rak przełyku itp.); aktywacja utajonego zakażenia gruźlicą; rozwijający się ropień płuca; nieodpowiednia terapia antybiotykowa. WYKŁAD nr 9. Choroby przewodu pokarmowego. Choroby przełyku. Zapalenie przełyku i wrzód trawienny przełyku 1. Ostre zapalenie przełyku Ostre zapalenie przełyku to zmiana zapalna błony śluzowej przełyku trwająca od kilku dni do 2-3 miesięcy. Etiologia i patogeneza. Czynniki etiologiczne: choroby zakaźne, urazy, oparzenia, zatrucia, reakcje alergiczne, błędy żywieniowe. Spośród czynników zakaźnych najbardziej charakterystyczne dla ostrego zapalenia przełyku są błonica, szkarlatyna, dur brzuszny i tyfus, grypa, paragrypa, infekcja adenowirusowa, świnka. Fizyczne i chemiczne czynniki uszkadzające są reprezentowane przez promieniowanie jonizujące, oparzenia chemiczne, gorące i bardzo zimne potrawy oraz przyprawy. Klasyfikacja. Nie ma jednej klasyfikacji. Można zastosować roboczą klasyfikację ostrego zapalenia przełyku. Morfologicznie wyróżnia się wymienione typy ostrego zapalenia przełyku: nieżytowe, obrzękowe, nadżerkowe, rzekomobłoniaste, krwotoczne, złuszczające, martwicze, ropowica. Według etiologii: zakaźna, chemiczna, fizyczna, pokarmowa. Według etapów endoskopowych: 1. - obrzęk i przekrwienie błony śluzowej, 2. - pojawienie się pojedynczych nadżerek na szczytach obrzękowych fałdów błony śluzowej, 3. - znaczny obrzęk i przekrwienie błony śluzowej z ogniskami erozji i krwawiących błon śluzowych, 4. - "płacząca" - błona śluzowa w sposób rozproszony zerodowana, krwawi przy najmniejszym dotknięciu endoskopu. Obraz kliniczny. Nieżytowe zapalenie przełyku jest najczęstszą postacią ostrego zapalenia przełyku. Występuje na tle błędów żywieniowych: podczas spożywania pikantnych, zimnych, gorących potraw, przy drobnych urazach, poparzeniach alkoholowych. Klinicznie objawia się pieczeniem i bólem za mostkiem, zmuszając pacjentów do odmowy jedzenia przez kilka dni. Endoskopowo stwierdzono zapalenie przełyku I-II stopnia, prześwietlenie - hiperkinezja przełyku. Erozyjne zapalenie przełyku występuje w przypadku chorób zakaźnych (płetwy, tyfus, posocznica, procesy grzybicze) i alergii. Pojawia się również przy oparzeniach chemicznych i urazach przełyku. W rzeczywistości ta forma zapalenia przełyku jest fazą ewolucji nieżytowego zapalenia przełyku. Główny obraz kliniczny składa się z objawów choroby podstawowej. Objawy kliniczne są podobne do objawów nieżytowego zapalenia przełyku: silny ból w klatce piersiowej podczas pasażu pokarmu; zgaga, odbijanie się, nadmierne ślinienie się, zgniły zapach z ust (kakosmia). Endoskopowo określić objawy zapalenia przełyku II-III stopnia. W badaniu histologicznym stwierdzono przekrwienie, obrzęk błony śluzowej, krwotok, erozję. Badanie rentgenowskie wykazuje obfitość śluzu w przełyku, restrukturyzację reliefu z utworzeniem płaskich złogów baru o podłużnym kształcie do 1 cm długości oraz hiperkinezę ścian przełyku. Krwotoczne zapalenie przełyku jest rzadką kliniczną postacią nadżerkowego zapalenia przełyku. Etiologia jest taka sama jak w przypadku nadżerkowego zapalenia przełyku. Klinicznie typowe są zespół silnego bólu i krwawe wymioty. Endoskopia ujawnia stan zapalny III-IV stopnia z przewagą komponentu krwotocznego. Istnieje oderwanie krwawiącej błony śluzowej w postaci wąskich cienkich pasków. Włókniste (rzekomobłoniaste) zapalenie przełyku. Czynniki etiologiczne to szkarlatyna, błonica, choroby krwi, choroby grzybicze, skutki radioterapii. W klinice dominuje dysfagia i silny ból, nasilający się po jedzeniu, nudnościach, wymiotach. Z wymiocinami uwalniane są filmy fibrynowe, może wystąpić krwioplucie. Endoskopowo na zaatakowanych obszarach błony śluzowej stwierdza się szare i żółto-szare włókniste blaszki, utworzone z warstw fibryny i detrytusu pokrywających powierzchnię błony śluzowej. Wraz z odrzuceniem błon rzekomych powstają płaskie, wolno gojące się nadżerki, czasem krwawiące wrzody. Po ciężkim procesie zakaźnym w przełyku pozostają błoniaste zwężenia, które znikają po powtórnym wybrzuszeniu. Błoniaste (złuszczające) zapalenie przełyku ma etiologię chemiczną (oparzenia przełyku), zakaźne (przyczyny to posocznica, półpasiec, ospa, uogólnione zakażenie opryszczką). Klinika choroby jest zróżnicowana – od łagodnych, zdiagnozowanych endoskopowo, po ciężkie. W klinice ciężkiego błoniastego zapalenia przełyku przeważa zatrucie, dysfagia i zespół bólowy. Możliwe krwawienie, perforacja przełyku, zapalenie śródpiersia, które z reguły kończą się śmiercią. W badaniu endoskopowym obserwuje się uszkodzenie wszystkich warstw przełyku, którego nabłonek jest odrzucany przez warstwy. Gdy choroba podstawowa ustępuje, w przełyku czasami pozostają symetryczne i asymetryczne, błoniaste lub szorstkie, bliznowate zwężenia. Martwicze zapalenie przełyku jest rzadką postacią ostrego zapalenia przełyku. Jego rozwojowi sprzyja obniżona odporność w tak poważnych chorobach jak posocznica, dur brzuszny, kandydoza, schyłkowa niewydolność nerek. Klinika charakteryzuje się bolesną dysfagią, wymiotami, ogólnym osłabieniem, krwawieniem, częstym rozwojem zapalenia śródpiersia, zapalenia opłucnej, zapalenia płuc. Po leczeniu choroby podstawowej w przełyku pozostają zwężenia, rozpoznane jako fakultatywne zmiany przedrakowe. Septyczne zapalenie przełyku jest rzadkim miejscowym lub rozlanym zapaleniem ścian przełyku o etiologii paciorkowcowej lub gdy błona śluzowa jest uszkodzona przez ciało obce, z oparzeniami, owrzodzeniami i może przejść z sąsiednich narządów. Czasami ostre zapalenie przełyku występuje jako powikłanie jakiejkolwiek postaci ostrego zapalenia przełyku, prowadzące do ropnego zespolenia ścian przełyku. Zapadnięciu się ścian towarzyszy przebicie się ropy do tkanki śródpiersia, rozwój zapalenia śródpiersia, zapalenia opłucnej, ropnego zapalenia oskrzeli, zapalenia płuc, zapalenia stawów kręgosłupa, pęknięcia aorty lub innych dużych naczyń. Przystąpienie zakażenia beztlenowego może prowadzić do rozedmy śródpiersia lub samoistnej odmy opłucnowej. Obraz kliniczny charakteryzuje się silnym zatruciem, wysoką gorączką, bólem za mostkiem i karkiem, wymiotami. W badaniu występuje obrzęk szyi, ruchomość w tej części kręgosłupa jest ograniczona. Pozycja głowy jest wymuszona, pochylona na bok. Choroba często przechodzi w ropne zapalenie śródpiersia. W badaniach krwi - hiperleukocytoza, przyspieszone ESR. Badanie instrumentalne (RTG, endoskopowe) w ostrej fazie nie jest wskazane. W okresie bliznowacenia obowiązkowe jest badanie rentgenowskie ze względu na ryzyko wystąpienia poważnych deformacji i zwężenia bliznowatego przełyku. Leczenie. Zasady leczenia ostrego zapalenia przełyku: etiotropowe, patogenetyczne i objawowe. Leczenie etiotropowe - leczenie choroby podstawowej. W chorobach zakaźnych powikłanych ostrym zapaleniem przełyku stosuje się antybiotyki (pozajelitowo). Przy wyraźnych zmianach martwiczych i krwotocznych w przełyku zaleca się powstrzymanie się od jedzenia przez 2-3 tygodnie. W tym okresie wskazane jest żywienie pozajelitowe, dożylne podawanie hydrolizatów białkowych, mieszanin aminokwasów, intralipidów, witamin oraz terapia detoksykacyjna. Po zmniejszeniu stanu zapalnego przepisywane są pokarmy oszczędzające termicznie i chemicznie: ciepłe mleko, śmietana, zupy warzywne, płynne płatki zbożowe. Aby zmniejszyć miejscowe objawy stanu zapalnego - wewnątrz roztworów taniny 1%, collargol - 2%, novocaine - 1-2% przed posiłkami. Środki ściągające są przyjmowane w pozycji poziomej z nisko opuszczoną głową łóżka. W przypadku braku działania miejscowego podawania preparatów ściągających, nie-narkotyczne środki przeciwbólowe są przepisywane pozajelitowo. Aby zmniejszyć skutki dyskinezy przełyku, leki prokinetyczne (cerucal, raglan, cyzapryd) stosuje się doustnie przed posiłkami. W przypadku wielu erozji wskazane są preparaty bizmutu (denol, vikair), zastrzyki solcoseryl. W krwotocznym zapaleniu przełyku, powikłanym krwawieniem, stosuje się preparaty kwasu aminokapronowego, vikasol, dicynone. W przypadku masywnego krwawienia zalecana jest transfuzja krwi lub osocza. W przypadku ropnego, martwiczego zapalenia przełyku pacjent powinien być przez długi czas żywiony pozajelitowo, stosuje się masową terapię kilkoma antybiotykami, a ropień jest drenowany. Zwężenia przełyku są korygowane przez bougienage. W rzadkich przypadkach zakłada się gastrostomię. Prognoza. Rokowanie w przypadku nieżytowego i nadżerkowego zapalenia przełyku jest korzystne. Samoistne ustąpienie objawów zapalenia przełyku jest możliwe pod warunkiem odpowiedniego wyleczenia choroby podstawowej. Rokowanie w przypadku rzekomobłoniastego, złuszczającego i ropniaczego zapalenia przełyku jest poważne. We wszystkich przypadkach, po wyzdrowieniu z choroby podstawowej, zapalenie przełyku kończy się utworzeniem zwężeń blizn, które następnie wymagają korekcji. Pacjenci z ciężkimi postaciami zapalenia przełyku powikłanego zwężeniem przełyku są niezdolni do pracy. Zapobieganie ostremu zapaleniu przełyku polega na odpowiedniej i terminowej diagnozie i leczeniu choroby podstawowej. 2. Przewlekłe zapalenie przełyku Przewlekłe zapalenie przełyku to przewlekłe zapalenie błony śluzowej przełyku trwające do 6 miesięcy. Najczęstszym wariantem jest zapalenie przełyku (refluksowe zapalenie przełyku), które może być powikłane chorobą wrzodową przełyku. Etiologia i patogeneza. Główną przyczyną choroby jest ciągłe zarzucanie treści żołądkowej do przełyku, czasami żółci i treści jelitowej, czyli trawienne zapalenie przełyku to aseptyczne oparzenie przełyku przez kwas żołądkowy. W patogenezie refluksowego zapalenia przełyku ważne są niedomykalność kwaśnej treści i naruszenie jej oczyszczania i opróżniania przełyku. Szybkość usuwania przełyku z podrażnienia chemicznego nazywana jest oczyszczaniem przełyku. Przy prawidłowym klirensie pojedynczy refluks agresywnych wydzielin nie powoduje refluksowego zapalenia przełyku. Gorące jedzenie, alkohol, palenie i inne czynniki egzogenne zmniejszają klirens przełyku. Czynniki te obejmują fast food, w którym wraz z jedzeniem połykana jest znaczna ilość powietrza. Liczy się też jakość jedzenia: tłuste mięso, smalec, makaron, ostre przyprawy pomagają opóźnić ewakuację pokarmu z żołądka, a następnie cofanie się treści do przełyku. Leki znacznie zmniejszają napięcie dolnego zwieracza przełyku i sprzyjają refluksowi: antagoniści wapnia, azotany, narkotyczne leki przeciwbólowe, leki antycholinergiczne, teofilina i jej analogi, leki z grupy prostaglandyn. Istnieje pięć kryteriów patogeniczności refluksu w genezie zapalenia przełyku: częstotliwość, objętość, niedomykalność, skład chemiczny, stan błony śluzowej przełyku i wrażliwość na czynnik chemiczny (zapalenie ścian zmniejsza wrażliwość), szybkość opróżniania (klirens) , który zależy głównie od aktywnej perystaltyki, alkalizującego działania śliny i śluzu. Występowaniu refluksowego zapalenia przełyku sprzyja przepuklina przełykowego ujścia przepony, wrzód dwunastnicy, zaburzenia po gastroresekcji, alergie. Predyspozycje alergiczne również mają znaczenie. Badanie morfologiczne pacjentów z zapaleniem przełyku ujawnia obrzęk, przekrwienie błony śluzowej, naciekanie błony podśluzowej nadprzeponowego odcinka przełyku. Istnieją dwie możliwości rozprzestrzeniania się przewlekłego stanu zapalnego - całkowite i miejscowe refluksowe zapalenie przełyku. Przy zaangażowaniu w proces ponad 2/3 błony śluzowej przełyku możliwy jest rozwój refluksowego zapalenia tchawicy, refluksowego zapalenia oskrzeli. Na szczytach fałd przełyku pojawiają się nadżerki, małe owrzodzenia (w miejscach maksymalnego nawadniania treścią żołądkową). Przewlekłe zapalenie przełyku prowadzi do przykurczu spastycznego i skrócenia narządu. Obraz kliniczny. Typowe objawy refluksowego zapalenia przełyku obejmują uczucie pieczenia za mostkiem, zgagę, zarzucanie treści żołądkowej, które nasilają się w pozycji leżącej, dysfagię i pozytywny wpływ przyjmowania leków zobojętniających sok żołądkowy. Po jedzeniu może wystąpić ból w klatce piersiowej, przypominający dusznicę bolesną. Występowanie bólu w refluksowym zapaleniu przełyku wiąże się z podrażnieniem trawiennym ściany przełyku i jej skurczami podczas zarzucania kwaśnej treści żołądkowej, a także z naruszeniem wypadniętej błony śluzowej. Charakterystyczne cechy tego bólu: jego długi, palący charakter, lokalizacja w wyrostku mieczykowatym, napromieniowanie wzdłuż przełyku, rzadziej do lewej połowy klatki piersiowej, brak zauważalnego efektu przyjmowania leków zobojętniających, przeciwskurczowych, nasilonych w pozycji poziomej, zwłaszcza po jedzenie. Szczególną uwagę w diagnostyce klinicznej należy zwrócić na drobne objawy dysfagii, takie jak uczucie guzka za mostkiem, uczucie gorącego pokarmu przechodzącego przez przełyk. Oznaką stopniowo rozpoczynającego się zapalenia przełyku może być ślinotok i nawyk picia wody z jedzeniem. Badanie fizykalne pacjentów z refluksowym zapaleniem przełyku nie dostarcza informacji istotnych diagnostycznie. Powikłania refluksowego zapalenia przełyku obejmują krwawienie, owrzodzenie, zwężenia, skrócenie przełyku i nowotwór złośliwy. Przewlekłe refluksowe zapalenie przełyku może prowadzić do rozwoju osiowej przepukliny rozworu przełykowego. Diagnoza i diagnostyka różnicowa. Najcenniejszą metodą badawczą tej patologii jest endoskopia, podczas której stwierdza się przekrwienie, obrzęk i pogrubienie fałdów błony śluzowej. Niezawodny jest białawy nalot pokrywający błonę śluzową, który w początkowych stadiach choroby może być cienki, ledwo zauważalny, ale z długim procesem - masywny biały lub brudnoszary. W niektórych obszarach na tle białej płytki nazębnej często widoczna jest jaskrawoczerwona błona śluzowa przełyku. W niektórych przypadkach wykrywane są defekty erozyjne i wrzodziejące w postaci pasków. Zmiany w błonie śluzowej mogą odpowiadać dowolnemu z czterech etapów zapalenia przełyku: od przekrwienia do „płaczącej” błony śluzowej. W przypadku ciężkiego zapalenia przełyku w świetle gromadzi się dużo śliny i śluzu. pH-metria, w przeciwieństwie do endoskopii, pozwala na bardziej obiektywną ocenę klirensu przełyku. Zdjęcie rentgenowskie ujawnia refluks żołądkowo-przełykowy. Konieczne jest różnicowanie refluksowego zapalenia przełyku z chorobą wrzodową żołądka i dwunastnicy, chorobą wieńcową, przewlekłym zapaleniem pęcherzyka żółciowego i zapaleniem trzustki. Wiodącym objawem w diagnostyce różnicowej jest ból. Różnicowaniu z chorobą wrzodową pomaga brak późnych i „głodnych” bólów w zapaleniu przełyku, a także dane uzyskane z endoskopii przełyku i żołądka. Ból wieńcowy, w przeciwieństwie do zapalenia przełyku, charakteryzuje się powiązaniem ze stresem fizycznym i emocjonalnym, działaniem azotanów, objawami niedokrwienia na zapis EKG, w tym według ergometrii rowerowej. Dane ultrasonograficzne narządów jamy brzusznej pomagają wykluczyć patologię pęcherzyka żółciowego i trzustki jako przyczyny zespołu bólowego. Leczenie. Terapia refluksowego zapalenia przełyku obejmuje leczenie chorób, które go spowodowały i przepisanie terapii przeciwrefluksowej. Pacjentom zaleca się unikanie podnoszenia ciężarów, schylania się. Podczas odpoczynku i snu konieczne jest przyjęcie prawidłowej pozycji (zagłówek jest podniesiony o 15-20 cm, pod kątem 30-50 °). Zaleca się normalizację masy ciała, jedzenie ułamkowe (ostatni posiłek - 3 godziny przed snem). Alkohol i pikantne potrawy są wyłączone z diety. Przypisz adsorbenty i leki alkalizujące, które mają działanie ochronne na błonę śluzową. Substancje te obejmują Venter, który podaje się doustnie w dawce 1 g (najlepiej w postaci zawiesiny) 30-40 minut przed posiłkiem 3 razy dziennie i 4 raz na czczo przed snem. Przebieg leczenia wynosi 8-10 tygodni. Podobny efekt mają Almagel, phosphalugel, maalox, gastal. Leki te stosuje się w okresie międzytrawiennym (1/2-2 godziny po posiłkach iw nocy) aż do całkowitej remisji. Phosphalugel i Maalox są przepisywane 1-2 opakowania 2-3 razy dziennie, gastal - 2-3 tabletki dziennie. Nie zaleca się stosowania sody herbacianej, mieszanki glinki Bourget, białej ze względu na niewystarczającą wydajność. Otulające i ściągające działanie ma azotan bizmutu 1 g 3-4 razy dziennie. Zaobserwowano wysoką aktywność przeciwrefluksową nowego środka zobojętniającego kwas, topalkan. Wody mineralne - "Borjomi", "Essentuki nr 4", "Jermuk", "Smirnovskaya" mają działanie alkalizujące. Aby zmniejszyć kwaśne wydzielanie żołądkowe, przepisywane są blokery H.2receptory histaminowe (cymetydyna, ranitydyna, famotydyna), inhibitory Ka-K-ATPazy (omeprazol), selektywny bloker receptorów M-cholinergicznych komórek okładzinowych, jego analog buscopan. Cymetydynę przepisuje się 400 mg 2 razy dziennie, ranitydynę - 300 mg i famotydynę - 40 mg raz wieczorem po obiedzie. Omeprazol jest zalecany w przypadku opornych postaci nadżerkowego i wrzodziejącego zapalenia przełyku. Jest przepisywany w dawce 30-40 mg dziennie przez 3-4 tygodnie. W celu normalizacji zaburzeń motorycznych w chorobie refluksowej przepisuje się metoklopramid (cerucal, raglan, perinorm, biomral), prepulsid (sizepride, motilium, domperidon, coordinax). Metoklopramid i jego analogi II generacji zwiększają napięcie dolnego zwieracza przełyku, obniżają ciśnienie wewnątrzżołądkowe i przyspieszają ewakuację z żołądka. Przypisz metoklopramid 2 tabletkę 1-3 razy dziennie przed posiłkami lub 4 ml domięśniowo 2 razy dziennie. Lek jest zwykle dobrze tolerowany. Przy jego stosowaniu możliwa jest suchość w ustach, senność, szumy uszne, które zmniejszają się po jedzeniu. Sizepride jest nowym środkiem prokinetycznym dla przewodu pokarmowego. Zwiększa napięcie dolnego zwieracza przełyku, poprawia klirens przełykowy, poprawia funkcję motoryczną przewodu pokarmowego i hamuje patologiczne refluksy (żołądkowo-żołądkowe). Lek, w przeciwieństwie do metoklopramidu, nie blokuje receptorów donaminowych, nie jest bezpośrednim stymulantem receptorów antycholinergicznych i jest pozbawiony skutków ubocznych związanych z cerukalem i jego analogami. Jest przepisywany doustnie w dawce 5 lub 10 mg 2-3 razy dziennie. Przebieg leczenia trwa od 2-3 tygodni do 2-3 miesięcy. Cezapryd z refluksowym zapaleniem przełyku można stosować w monoterapii. Rokowanie i zapobieganie. Prognozy dotyczące życia i pracy są pomyślne. W skomplikowanych przypadkach rokowanie zależy od terminowości i jakości opieki medycznej. Pacjentom z ciężką chorobą przydziela się grupę niepełnosprawności. Pacjenci z przewlekłym refluksowym zapaleniem przełyku powinni być pod kontrolą gastroenterologa. Badania endoskopowe i morfologiczne wskazane są przynajmniej 2 razy w roku ze względu na możliwość wystąpienia nowotworu złośliwego. 3. Wrzód trawienny przełyku Wrzód trawienny przełyku to ostra lub przewlekła choroba charakteryzująca się owrzodzeniem błony śluzowej dalszego odcinka przełyku pod wpływem aktywnego soku żołądkowego. Etiologia i patogeneza. Przewlekłe wrzody trawienne przełyku są powikłaniem refluksowego zapalenia przełyku i przepukliny rozworu przełykowego. Ich występowaniu sprzyja krótki wewnętrzny przełyk, ogniskowa metaplazja błony śluzowej, heterotopia błony śluzowej żołądka do przełyku, choroba refluksowa z niewydolnością wpustu, choroby towarzyszące częstym wymiotom (zespół po wagotomii, zespół pętli doprowadzającej, przewlekły alkoholizm). Ostre wrzody przełyku są możliwe z patologiczną suchością błony śluzowej przełyku (kseroza), alergiami na leki, stosowaniem NLPZ, infekcjami grzybiczymi, infekcjami wirusowymi, oparzeniami skóry i chorobami ośrodkowego układu nerwowego. Te wrzody są uważane za objawowe. Obraz kliniczny. Niektórzy pacjenci mają połączone wrzodziejące uszkodzenie błony śluzowej przełyku i strefy żołądkowo-dwunastniczej. Objawy wrzodu trawiennego przełyku przypominają obraz kliniczny trawiennego zapalenia przełyku: uporczywa zgaga, nasilająca się po jedzeniu, podczas zginania ciała, w pozycji leżącej, niedomykalność, ból podczas połykania i utrudnione wydalanie stałego pokarmu. Powikłania typowe dla wrzodów przełyku: perforacja, krwawienie, penetracja, zwężenie. Krwawienie objawia się krwawymi wymiotami, meleną, niedokrwistością hipochromiczną i zmniejszeniem czynności serca. Perforację przełyku diagnozuje się niezwykle rzadko. Objawy kliniczne perforacji są nie do odróżnienia od objawów ostrego penetrującego i niepenetrującego urazu mechanicznego przez ciała obce. Około 14% owrzodzeń przełyku przenika do otaczających tkanek. Diagnoza i diagnostyka różnicowa. Niezwykle trudno jest podejrzewać wrzód trawienny na podstawie objawów klinicznych. Rozpoznanie weryfikowane jest w trakcie badań instrumentalnych i laboratoryjnych. Najbardziej pouczające jest badanie rentgenowskie i endoskopowe. Radiologicznie owrzodzenie wygląda jak nisza w przełyku nadsercowym z niewielkim okołoogniskowym obrzękiem błony śluzowej. Przełyk w obszarze wrzodu jest spastycznie skurczony, a nad nim wykrywa się niewielką ekspansję nadstenotyczną. Owrzodzeniu towarzyszą objawy hiperkinezy i refluksowego zapalenia przełyku, a objawy przepukliny rozworu przełykowego są bardzo częste. Czasami wrzód przypomina mały uchyłek nadprzeponowy, jednak ten ostatni nie ma typowego przebiegu klinicznego i nie łączy się z niewydolnością serca, przepukliną czy zapaleniem przełyku. Trudniej jest odróżnić wrzód trawienny przełyku od owrzodzonego raka endofitycznego, któremu towarzyszy sztywność ścian i odciążenie błony śluzowej oraz asymetryczny trzon, za pomocą objawów radiologicznych. Najbardziej wiarygodne informacje w weryfikacji choroby wrzodowej przełyku dostarcza endoskopia i biopsja wielokrotna z brzegów wrzodu. Podczas przesuwania endoskopu do wrzodu trawiennego ujawniają się objawy zapalenia przełyku w stadium I-IV, dysfunkcja motoryczna przełyku, obrzęk okołoogniskowy i przekrwienie błony śluzowej. Ostry wrzód jest zwykle okrągły lub owalny, o stromych krawędziach, pokryty białawym lub zielonym nalotem. Przewlekły wrzód ma płaskie dno o gęstych i nierównych ścianach, łagodne brzegi, złogi ropno-włókniste, ogniska ziarninowania i bliznowate naloty. Aby wykluczyć nowotwór złośliwy, pobiera się 4-6 biopsji z brzegów owrzodzenia. Badanie endoskopowe ujawnia pojedyncze wady trawienne, wydłużone wzdłuż osi przełyku. Ich długość waha się w granicach 1-10 cm, ale częściej nie przekracza 1 cm, wrzód jest często płytki, jego dno pokryte jest białawą powłoką. Przekrwienie, obrzęk błony śluzowej i pojedyncze nadżerki często odzwierciedlają umiarkowaną okołoogniskową reakcję zapalną. Po wygojeniu wrzodu trawiennego w przełyku pozostaje szorstka liniowa lub gwiaździsta blizna lub szorstka uchyłkowata deformacja ściany i zwężenie światła przełyku. Konieczne jest odróżnienie wrzodów trawiennych przełyku od owrzodzeń o określonym charakterze (z gruźlicą, kiłą). W takich sytuacjach znacząco pomagają specyficzne testy serologiczne, wyniki badań histologicznych i bakteriologicznych. Połączenie patologii przełyku z uszkodzeniem płuc i innych narządów powoduje, że konieczne jest celowe zbadanie pacjenta w odniesieniu do określonego procesu. Leczenie. Leczenie obejmuje dietę: zaleca się dietę łagodną mechanicznie i chemicznie, przyjmowaną w małych porcjach 5-6 razy dziennie. Aby zapobiec cofaniu się treści z żołądka do przełyku, należy ułożyć pacjenta w łóżku z podniesionym wezgłowiem. Leki przyjmuje się na leżąco. W monoterapii przepisuje się lek z jednej z następujących grup farmakologicznych: leki przeciwwydzielnicze, w tym leki zobojętniające sok żołądkowy i adsorbenty, stymulatory funkcji motorycznej żołądka (prokinetyka), leki - symulatory śluzu. Terapię prowadzi się przez długi czas - 1,5-3 miesiące. Wskazania do leczenia operacyjnego - brak gojenia w ciągu 6-9 miesięcy, przebieg skomplikowany (perforacja, penetracja, zwężenie, krwawienie). Rokowanie i zapobieganie. Przebieg choroby ma charakter nawrotowy. Prognozy dotyczące życia i pracy są pomyślne. Zaleca się okresowe (1-2 razy w roku) badanie ambulatoryjne przez gastroenterologa z wykorzystaniem endoskopii i biopsji. Prowadzona jest sezonowa (wiosna - jesień) zapobieganie refluksowemu zapaleniu przełyku. WYKŁAD nr 10. Choroby przewodu pokarmowego. Choroby żołądka. Przewlekłe zapalenie żołądka Przewlekłe zapalenie błony śluzowej żołądka jest chorobą, która klinicznie charakteryzuje się niestrawnością żołądka, a morfologicznie - zmianami zapalnymi i zwyrodnieniowymi błony śluzowej żołądka, zaburzeniami procesów odnowy komórek oraz wzrostem liczby komórek plazmatycznych i limfocytów we własnej błonie śluzowej. Etiologia i patogeneza. Na obecnym etapie rozwoju gastroenterologii ustalono, że występowaniu przewlekłego zapalenia błony śluzowej żołądka sprzyja ekspansja drobnoustrojów Helicobacter pylori (HP), która w 95% przypadków powoduje antralne zapalenie błony śluzowej żołądka i w 56% przypadków zapalenie błony śluzowej żołądka. Z kolei tak zwane czynniki etiologiczne występowania przewlekłego zapalenia błony śluzowej żołądka można z dużą pewnością przypisać czynnikom ryzyka (nieregularna niezbilansowana dieta, palenie tytoniu, spożywanie alkoholu, nadmierne wydzielanie kwasu solnego i pepsyny). Wiodącą rolę w rozwoju choroby odgrywają również mechanizmy autoimmunologiczne, którym towarzyszy nagromadzenie przeciwciał przeciwko komórkom okładzinowym błony śluzowej żołądka, pogorszenie dziedziczności, a także stosowanie leków, które mają szkodliwy wpływ na błonę śluzową żołądka. Klasyfikacja. W 1990 roku na IX Międzynarodowym Kongresie Gastroenterologów w Australii przyjęto nową systematyzację przewlekłego zapalenia błony śluzowej żołądka, zwaną systemem Sydney. Histologiczne podstawy klasyfikacji. 1) Etiologia: przewlekłe zapalenie żołądka związane z HP, autoimmunologiczne, idiopatyczne, ostre polekowe zapalenie żołądka. 2) Topografia: antralna, dna, pangastritis. 3) Morfologia: formy ostre, przewlekłe, specjalne. Endoskopowe podstawy klasyfikacji: 1) zapalenie żołądka antrum żołądka; 2) zapalenie żołądka ciała żołądka; 3) zapalenie żołądka; 4) zmiany w błonie śluzowej żołądka: obrzęk, rumień, podatność błony śluzowej, wysięk, nadżerki płaskie, uniesione nadżerki, przerost fałdów, zanik fałdów, widoczność układu naczyniowego, krwotoki nadśluzówkowe. Obraz kliniczny. Przewlekłe zapalenie błony śluzowej żołądka jest jedną z najczęstszych chorób w klinice chorób wewnętrznych. Jego częstotliwość wśród mieszkańców świata waha się od 28 do 75%. Przewlekłe zapalenie żołądka częściej objawia się objawami niestrawności żołądka i bólu w okolicy nadbrzusza. Rzadko przebiega bezobjawowo. Ból jest zwykle zlokalizowany w okolicy nadbrzusza. Istnieje wyraźny związek między jego występowaniem z przyjmowaniem pokarmu a lokalizacją procesu zapalnego w żołądku. U pacjentów z zapaleniem żołądka odcinka podsercowego i sercowego żołądka ból w okolicy nadbrzusza występuje 10-15 minut po posiłku, z patologią ciała żołądka - 40-50 minut po posiłku. Bóle „późne”, „głodne” są typowe dla zapalenia żołądka części wyjściowej żołądka lub dwunastnicy. Ból "dwufalowy" - po jedzeniu i na czczo - obserwuje się przy zapaleniu żołądka podsercowego i antrum. W procesie rozproszonym ból jest zlokalizowany w okolicy nadbrzusza, pojawia się po jedzeniu i ma charakter uciskający. Mówią o bezobjawowym przebiegu zapalenia żołądka, gdy nie można ustalić związku między bólem w okolicy nadbrzusza a zmianą, która występuje, gdy ma pochodzenie endogenne (zapalenie żołądka staje się wtórne do patologii innych narządów i układów). Równie ważne miejsce w obrazie klinicznym przewlekłego zapalenia żołądka zajmuje zespół dyspeptyczny: nudności, odbijanie (kwaśne, gorzkie, zgniłe), zgaga, zaparcia lub biegunka, niestabilne stolce. W przypadku izolowanego antralnego zapalenia żołądka najważniejsze stają się dolegliwości związane z zgagą i zaparciami, wynikające z nadmiernego wydzielania kwasu solnego i pepsyny. W przypadku zapalenia żołądka z objawami ciężkiej atrofii dominują nudności, odbijanie „zgniłe”, niestabilne stolce lub biegunka, co jest typowe dla hiposekrecji kwasu solnego i pepsyny. Uporczywe nudności są charakterystyczne dla wtórnego zapalenia żołądka w przewlekłym zapaleniu trzustki, przewlekłym zapaleniu pęcherzyka żółciowego, występującym przy dyskinezie hipomotorycznej pęcherzyka żółciowego. diagnostyka. Przewlekłe zapalenie błony śluzowej żołądka trwa długo, a objawy nasilają się w miarę upływu czasu. Zaostrzenia są wywoływane przez zaburzenia odżywiania. Fizyczny obraz przewlekłego zapalenia żołądka jest raczej słaby. U 80-90% pacjentów podczas zaostrzenia choroby obiektywne badanie określa jedynie miejscowy ból w okolicy nadbrzusza. Gdy przewlekłe zapalenie błony śluzowej żołądka łączy się z zapaleniem dwunastnicy, zapaleniem pęcherzyka żółciowego lub zapaleniem trzustki, można określić lokalizację bólu, który nie jest typowy dla zapalenia żołądka, ale charakterystyczny dla patologii innego narządu. Ogólne badania krwi i moczu, parametry biochemiczne krwi u pacjentów z przewlekłym zapaleniem żołądka nie różnią się od odpowiednich parametrów u osób zdrowych. W badaniu koprologicznym nie ma zmian w analizach lub mogą występować objawy zaburzeń trawienia. Podczas badania zawartości wydzielania kwasu w żołądku za pomocą pH-metrii odnotowuje się zarówno oznaki nadmiernego wydzielania kwasu, jak i zmniejszenia produkcji kwasu. Wskaźniki tworzenia pepsyny w przewlekłym zapaleniu żołądka są bardziej trwałe i zmniejszają się na tle uporczywej kwasowości w rozproszonym uszkodzeniu narządów. Badanie rentgenowskie jest bardziej prawdopodobne, aby wykluczyć inne choroby żołądka (wrzody, nowotwory), pomóc w diagnozie choroby Menetriera niż potwierdzić rozpoznanie przewlekłego zapalenia żołądka. Ze względu na brak objawów klinicznych choroby, a także niespecyficzność badań laboratoryjnych, rozpoznanie przewlekłego zapalenia żołądka opiera się na wynikach badań endoskopowych i morfologicznych. Endoskopia ujawnia zmiany w nasileniu błony śluzowej żołądka o różnym nasileniu: obrzęk, rumień, wrażliwość błony śluzowej, wysięk, płaskie nadżerki, uniesione nadżerki, przerost lub zanik fałdów, widoczność układu naczyniowego, krwotoki podśluzówkowe. Mówią o przewlekłym zapaleniu żołądka ze wzrostem liczby komórek plazmatycznych i limfocytów we własnej błonie śluzowej (w przeciwieństwie do ostrego zapalenia żołądka, gdy pojawiają się leukocyty wielojądrzaste). W związku z powyższym morfologiczna identyfikacja zapalenia w zapaleniu żołądka może nie pokrywać się z interpretacją danych lekarza. Aktywność zmian zapalnych błony śluzowej żołądka ocenia się morfologicznie i morfometrycznie w zależności od stopnia naciekania leukocytów blaszki właściwej lub nabłonka. Nie wolno nam tracić z oczu faktu, że autoimmunologiczne zapalenie żołądka nie jest aktywne. Zmiany morfologiczne (słabe, umiarkowane i ciężkie) – stan zapalny, aktywność, atrofia, metaplazja – oraz stopień zanieczyszczenia HP są określane ilościowo. Objawy kliniczne charakterystyczne dla zapalenia żołądka obserwuje się również w innych chorobach przewodu pokarmowego, dlatego w procesie diagnozy konieczne jest badanie ultrasonograficzne jamy brzusznej, dokładne badanie endoskopowe i morfologiczne narządów trawiennych. Diagnostyka różnicowa. Najtrudniejsza jest diagnostyka różnicowa zapalenia błony śluzowej żołądka z chorobami czynnościowymi żołądka, wrzodem trawiennym żołądka i dwunastnicy, przewlekłym zapaleniem pęcherzyka żółciowego i zapaleniem trzustki oraz rakiem żołądka. Choroby czynnościowe żołądka, podobne do przewlekłego zapalenia błony śluzowej żołądka, mogą występować latentnie lub towarzyszyć im ból i objawy dyspeptyczne. Charakteryzują się krótkim czasem trwania, występowaniem ogólnych objawów nerwicowych, które przeważają w obrazie klinicznym choroby (takich jak osłabienie, zmęczenie, drażliwość, ból głowy, chwiejny nastrój, pocenie się). Przy zaburzeniach funkcji żołądka ból nie zależy od jakości pokarmu lub pojawia się po zastosowaniu ściśle określonego produktu. Często występuje zespół kwasicy (zgaga, kwaśne odbijanie, kwaśny smak w ustach), który w przeciwieństwie do zapalenia żołądka o zwiększonej funkcji wydzielniczej nie zwiększa się po jedzeniu, ale z podnieceniem, długimi przerwami w jedzeniu. Wymioty w patologiach czynnościowych żołądka rozwijają się zgodnie z mechanizmem odruchu warunkowego, przynoszą ulgę pacjentowi i nie prowadzą do znacznego pogorszenia stanu ogólnego. W przewlekłym zapaleniu błony śluzowej żołądka występuje zwykle podczas zaostrzenia i nie przynosi ulgi pacjentowi. Częstym objawem dysfunkcji żołądka jest głośne wyrzucanie powietrza. W przewlekłym zapaleniu żołądka wiąże się z upośledzeniem trawienia pokarmu lub motoryki żołądka i może mieć kwasowość, jeśli wydzielina jest zachowana, lub zapach zgniłych jaj, jeśli jest zmniejszony. W badaniu wydzielania żołądkowego w zapaleniu żołądka na początku choroby wykrywa się normalne wartości wydzielania, aw przyszłości tendencję do zmniejszania wydzielania soku żołądkowego. W przypadku funkcjonalnych chorób żołądka często obserwuje się heterochilię. Badanie rentgenowskie żołądka umożliwia potwierdzenie takich postaci zapalenia żołądka, jak sztywne, angralowe, olbrzymie przerosty, polipowatość, a w przypadku naruszenia funkcji motoryczno-ewakuacyjnej żołądka (gastroptoza, niedociśnienie) wskazuje na funkcjonalny charakter choroba. Najcenniejszą metodą badawczą w diagnostyce różnicowej przewlekłego zapalenia błony śluzowej żołądka i chorób czynnościowych żołądka jest gastroskopia, która w kontrowersyjnych przypadkach pozwala stwierdzić zmiany w błonie śluzowej żołądka charakterystyczne dla zapalenia żołądka lub chorób czynnościowych żołądka. Diagnostyka różnicowa przewlekłego zapalenia żołądka z wrzodem trawiennym została opisana w następnym wykładzie. Rak żołądka ma bardzo podobny obraz z zapaleniem żołądka o zmniejszonej funkcji wydzielniczej. Wczesna diagnoza raka żołądka na podstawie objawów klinicznych jest trudna, zwłaszcza u pacjentów cierpiących na nieżyt żołądka od dłuższego czasu. Duże znaczenie dla rozpoznania nowotworu ma pojawienie się uporczywego, uporczywego bólu, mało zależnego od przyjmowanych pokarmów, brak motywacji ogólnego osłabienia i zmęczenia, wypaczenie apetytu, a także postępujący spadek masy ciała pacjenta. Wykrycie guza w badaniu palpacyjnym odnosi się do późniejszych etapów procesu nowotworowego. Objawy, takie jak zmiana samopoczucia pacjenta, szybki spadek kwasowości soku żołądkowego, „niedobór” kwasu solnego, pojawienie się nietypowych komórek w soku żołądkowym, pozytywna reakcja na krew utajoną w kale spowodować, że lekarz podejrzewa raka żołądka. Decydujące znaczenie w diagnostyce różnicowej mają badania rentgenowskie i gastroskopowe z celowaną biopsją błony śluzowej żołądka. U pacjentów z przewlekłym zapaleniem błony śluzowej żołądka z obniżoną funkcją wydzielniczą w badaniu RTG stwierdza się zanik błony śluzowej, co potwierdza również gastroskopia. Przy celowanej biopsji w takich przypadkach ujawniają się zmiany strukturalne i atrofia błony śluzowej. W przypadku raka żołądka badanie rentgenowskie charakteryzuje się obecnością ubytku wypełnienia, brakiem fałdów błony śluzowej lub zmianą ich charakteru oraz brakiem perystaltyki w niektórych obszarach. Endoskopia żołądka umożliwia wykrycie guza w najwcześniejszym stadium jego rozwoju, gdy guz znajduje się jeszcze w obrębie błony śluzowej żołądka, a leczenie chirurgiczne prowadzi do wyzdrowienia w ponad 90% przypadków. Przewlekłe zapalenie pęcherzyka żółciowego. W przewlekłym zapaleniu pęcherzyka żółciowego ból jest zlokalizowany w prawym podżebrzu i ma charakter tępy. W przypadku kamienistego zapalenia pęcherzyka żółciowego ból jest ostry, kolkowy, promieniujący do prawego obszaru podłopatkowego. Początek bólu wiąże się ze spożywaniem tłustych potraw lub szarpaniną za kierownicą. W przewlekłym zapaleniu żołądka ból w nadbrzuszu jest rozproszony, tępy, nie ma napromieniowania, pojawia się natychmiast po zjedzeniu suchej karmy lub z naruszeniem diety. W przypadku zapalenia żołądka i zapalenia pęcherzyka żółciowego bólowi towarzyszą objawy dyspeptyczne, ale bardziej charakterystyczne dla zapalenia żołądka jest uczucie ciężkości w nadbrzuszu, pełność, odbijanie pokarmu lub powietrza, metaliczny smak w ustach. Wymioty w przewlekłym zapaleniu żołądka są rzadkie. Obiektywnie w przewlekłym zapaleniu pęcherzyka żółciowego, zwłaszcza wyrostka zębodołowego, wykrywa się napięcie w przedniej ścianie jamy brzusznej, przeczulicę skóry w prawym podżebrzu, co nie jest typowe dla przewlekłego zapalenia błony śluzowej żołądka. W badaniu palpacyjnym brzucha w przypadku przewlekłego zapalenia pęcherzyka żółciowego obserwuje się ból w lokalizacji pęcherzyka żółciowego. Przewlekłe zapalenie żołądka charakteryzuje się rozlaną bolesnością. U pacjentów z przewlekłym zapaleniem pęcherzyka żółciowego badanie żółci ujawnia wzrost ilości śluzu i leukocytów. Przewlekłe zapalenie żołądka charakteryzuje się normalnym obrazem żółci na tle zmian w wydzielaniu i kwasowości soku żołądkowego, a także innych funkcji żołądka (wchłanianie, motoryka). Badanie rentgenowskie pęcherzyka żółciowego u pacjentów z przewlekłym zapaleniem pęcherzyka żółciowego ujawnia zmianę jego funkcji ewakuacyjnej, a także kamienie. Przewlekłe zapalenie trzustki. W przewlekłym zapaleniu trzustki ból jest zlokalizowany w lewej połowie brzucha i promieniuje do lewej okolicy podłopatkowej, dolnej części pleców i okolic. Występowanie dolegliwości bólowych wiąże się ze spożywaniem obfitych, często tłustych potraw oraz alkoholu. Jeśli przewlekłe zapalenie żołądka charakteryzuje się długim, monotonnym przebiegiem choroby, to w przewlekłym zapaleniu trzustki jest to stopniowe. Badanie obiektywne w przypadku przewlekłego zapalenia trzustki ujawnia przeczulicę skóry w lewym podżebrzu, ból topograficznie odpowiada lokalizacji trzustki. W badaniu laboratoryjnym soku trzustkowego w przewlekłym zapaleniu trzustki stwierdzono trwałą zmianę zasadowości i enzymów: poziom diastazy we krwi i moczu może się zmienić, co nie ma miejsca w przypadku przewlekłego zapalenia żołądka. Radiologicznie przewlekłe zapalenie trzustki charakteryzuje się zwiększonym odwróceniem pierścienia dwunastnicy, gwałtownym wzrostem jego brodawki głównej (objaw Frostberga), a czasem obecnością obszarów zwapnienia trzustki. Należy również przeprowadzić diagnostykę intranosologiczną różnych postaci przewlekłego zapalenia żołądka. Tak więc choroba związana z HP przebiega klinicznie z objawami wrzodów dwunastnicy, a w niektórych przypadkach może przebiegać latentnie. Badanie endoskopowe i morfologiczne ujawnia antropyloroduodenitis. Nadżerki w zapaleniu żołądka Helicobacter pylori są zwykle zlokalizowane w obszarze ciężkiego stanu zapalnego (strefa antropyloryczna żołądka). Autoimmunologiczne przewlekłe zapalenie błony śluzowej żołądka charakteryzuje się klinicznie uczuciem ciężkości w okolicy nadbrzusza, nieprzyjemnym posmakiem w ustach, zgniłym odbijaniem i nudnościami. Z powodu niewystarczającej produkcji kwasu solnego pojawia się biegunka. W 10% przypadków na tle autoimmunologicznego zapalenia żołądka występują objawy B12- niedokrwistość niedokrwienna: osłabienie, bladość skóry i błon śluzowych, łamliwość paznokci, w badaniach krwi - hiperchromiczna niedokrwistość megaloblastyczna. Szczególne postacie choroby obejmują ziarniniakowe, eozynofilowe, przerostowe (choroba Menetriera), limfocytarne zapalenie żołądka. Ziarniniakowe zapalenie żołądka działa jako niezależna postać choroby lub częściej - jeden ze składników poważniejszej patologii (choroba Leśniowskiego-Crohna, gruźlica, sarkoidoza). Rozpoznanie zawsze potwierdzają wyniki badania histologicznego wycinków z biopsji błony śluzowej żołądka. Eozynofilowe zapalenie żołądka jest niezwykle rzadkie i jest spowodowane układowym zapaleniem naczyń. Obowiązkowa jest historia reakcji alergicznych. Badanie histologiczne ujawnia naciek eozynofilowy błony śluzowej żołądka. Przerostowe zapalenie żołądka (choroba Menetriera) objawia się klinicznie bólem w okolicy nadbrzusza i nudnościami. Niektórzy pacjenci mogą odczuwać utratę wagi z powodu biegunki. W badaniach endoskopowych, radiologicznych i morfologicznych znaleziono gigantyczne przerośnięte fałdy błony śluzowej, przypominające zwoje mózgu. Limfocytowe zapalenie żołądka jest klinicznie bezobjawowe; morfologicznie postać ta charakteryzuje się wyraźną infiltracją błony śluzowej żołądka przez limfocyty. Leczenie. Pacjenci z zapaleniem błony śluzowej żołądka wymagają ogólnych środków medycznych: regularnego, zbilansowanego odżywiania, normalizacji harmonogramów pracy i odpoczynku, wyrównywania stresujących sytuacji w życiu codziennym i pracy. Farmakoterapia jest wskazana tylko w przypadku klinicznych objawów przewlekłego zapalenia żołądka. Pacjenci z zapaleniem żołądka związanym z HP są leczeni programem wrzodów trawiennych (patrz następny wykład). Osoby z autoimmunologicznym zapaleniem żołądka potrzebują suplementacji witaminą B12 (500 mcg raz dziennie podskórnie przez 1 dni, a następnie powtórzenie kursów leczenia), kwas foliowy (30 mg dziennie), kwas askorbinowy (do 5 g dziennie). W razie potrzeby przeprowadza się terapię zastępczą preparatami enzymatycznymi (mezim-forte, festal, enzistal, creon, pancitrate, acidin-pepsyna). Zespół bólowy zwykle zatrzymuje się przez wyznaczenie leków zobojętniających (maalox, almagel, gastal) lub blokerów receptora H-histaminowego (ranitydyna, famotydyna) w średnich dawkach terapeutycznych. W przypadku specjalnych postaci zapalenia żołądka konieczne jest leczenie choroby podstawowej. Rokowanie i zapobieganie. Prognozy dotyczące życia i pracy są pomyślne. Pacjenci z przewlekłym zapaleniem błony śluzowej żołądka powinni zostać zarejestrowani u gastroenterologa. Są badane klinicznie i endoskopowo z biopsją przynajmniej raz w roku, aby wykluczyć transformację nowotworu. Najbardziej niebezpieczne pod względem zwyrodnienia nowotworowego są przerostowe, rozsiane zanikowe zapalenie żołądka z dysplazją nabłonka. W erozyjnej postaci choroby powikłanej krwawieniem, a także w zdekompensowanej postaci choroby Menetriera, rokowanie zależy od terminowości i adekwatności leczenia chirurgicznego. Zapobieganie zapaleniu żołądka ogranicza się do racjonalnego odżywiania, przestrzegania reżimu pracy i odpoczynku, ograniczenia przyjmowania NLPZ. WYKŁAD nr 11. Choroby przewodu pokarmowego. Choroby żołądka. wrzód trawienny Wrzód trawienny (wrzód trawienny) jest przewlekłą, nawracającą chorobą, klinicznie objawiającą się funkcjonalną patologią strefy żołądkowo-dwunastniczej, a morfologicznie - naruszeniem integralności jej warstwy śluzowej i podśluzówkowej, a zatem wrzód zawsze goi się z tworzeniem blizna. Etiologia. Głównym czynnikiem etiologicznym choroby wrzodowej żołądka jest ekspansja drobnoustrojów HP na powierzchni nabłonka żołądka. Znaczenie agresji bakteryjnej w etiologii choroby badano od 1983 r., kiedy to J. Warren i B. Marshall donieśli o odkryciu dużej liczby bakterii S-spirali na powierzchni nabłonka jamy żołądka. Helicobacteria są w stanie egzystować w środowisku kwaśnym dzięki produkcji enzymu ureazy, który przekształca mocznik (z krwiobiegu) w amoniak i dwutlenek węgla. Produkty hydrolizy enzymatycznej neutralizują kwas solny i stwarzają warunki do zmiany pH środowiska wokół każdej komórki bakteryjnej, zapewniając tym samym dogodne warunki dla żywotnej aktywności mikroorganizmów. Całkowita kolonizacja HP zachodzi na powierzchni komórek nabłonka żołądka, czemu towarzyszy uszkodzenie nabłonka pod wpływem fosfolipaz. Te ostatnie zapewniają powstawanie toksycznych lecytyn i proteinaz z żółci, powodując niszczenie ochronnych kompleksów białkowych i śluzu. Na tle "alkalizacji" błon komórkowych nabłonka amoniakiem zmienia się potencjał błonowy komórek, wzrasta odwrotna dyfuzja jonów wodorowych, śmierć i złuszczanie nabłonka błony śluzowej żołądka. Wszystkie te zmiany prowadzą do wnikania HP w głąb błony śluzowej żołądka. Nie mniej ważne w rozwoju wrzodów trawiennych są efekty neuropsychiczne, predyspozycje dziedziczne, czynniki zakaźne, błędy żywieniowe i przyjmowanie niektórych leków oraz złe nawyki. Po raz pierwszy neurogenna koncepcja początku choroby została sformułowana przez Bergmana, który twierdził, że dziedziczno-konstytucyjne zaburzenia autonomicznego układu nerwowego prowadzą do skurczu mięśni i naczyń krwionośnych w ścianie żołądka, niedokrwienia i zmniejszenia w odporności błony śluzowej na agresywne działanie soku żołądkowego. Teorię tę rozwinęli dalej K.N. Bykov i I.T. Kurtsin (1952). Uzasadnili oni teorię korowo-narządową wrzodu, która opiera się na danych dotyczących zmian w podwyższonej aktywności nerwowej wynikających z przewlekłej traumatyzacji neuropsychicznej. Uzupełniona i uszczegółowiona przez doktrynę biochemicznych i hormonalnych powiązań w regulacji wydzielania, motoryki i trofizmu żołądka, ta teoria wrzodowogenezy ponownie zyskała w ostatnich latach wielu zwolenników. Czynniki dziedziczne są popularne wśród badaczy: bezwładność głównych procesów nerwowych, specyficzne dla grupy właściwości krwi, cechy immunologiczne i biochemiczne, zespół obciążenia dziedzicznego. W występowaniu choroby wrzodowej duże znaczenie miały zaburzenia odżywiania. Jednak badania kliniczne i eksperymentalne przeprowadzone w ciągu ostatnich dwóch dekad w większości przypadków nie wykazały szkodliwego wpływu produktów spożywczych na błonę śluzową żołądka i dwunastnicy. O wiodącej roli czynników żywieniowych świadczy również występowanie choroby wrzodowej żołądka wśród znaczących grup osób o odmiennych nawykach żywieniowych. Zaburzenia rytmu i regularności żywienia, długie przerwy między posiłkami, przedwczesne jedzenie są niezbędne do wystąpienia wrzodów trawiennych. Badacze wyrazili stosunkowo sprzeczne poglądy na temat roli alkoholu we wrzodzieniu. Wiadomo, że alkohol powoduje zmiany zanikowe w błonie śluzowej żołądka. Obserwacje te stoją w sprzeczności z ogólną koncepcją owrzodzenia. Jednak częstemu spożywaniu alkoholu towarzyszą naruszenia diety, zmiany jakościowe w składzie pokarmu, które ostatecznie mogą powodować wrzód trawienny żołądka i dwunastnicy. Aktywnie badana jest rola efektów leczniczych we wrzodzieniu. Opublikowane w piśmiennictwie wyniki badań oraz dane własne wskazują, że najsilniejsze właściwości wrzodziejące mają niesteroidowe leki przeciwzapalne i hormony glikokortykosteroidowe. Patogeneza. Patogeneza choroby wrzodowej żołądka i jelit wciąż nie jest w pełni poznana. Rozważając procesy powstawania wrzodów, należy podkreślić szereg postulatów: 1) charakteryzuje się sezonowością zaostrzeń choroby wrzodowej; 2) występuje dominująca lokalizacja wrzodów trawiennych w strefie antropylorodunalnej; 3) stwierdzono obecność kwasu solnego i pepsyny w soku żołądkowym; 4) zauważalna jest wysoka częstość (do 70%) samoistnego gojenia wrzodów żołądka i dwunastnicy; 5) występuje przewlekłe antralne zapalenie żołądka związane z HP; 6) antropyloryczna część żołądka i początkowa część dwunastnicy to „podwzgórze” przewodu pokarmowego; 7) istnieje dziedziczna predyspozycja do występowania wrzodów trawiennych; 8) wystąpienie owrzodzenia, jego nawrót i remisja są możliwe przy wszystkich powyższych czynnikach. Tak więc ujednolicona koncepcja wrzodzenia jest następująca. U pacjenta z dziedziczną predyspozycją do choroby wrzodowej w obecności przewlekłego bakteryjnego zapalenia błony śluzowej żołądka w okresie jesiennej lub wiosennej dyshormonozy stwierdza się jedynie przerost i nadczynność komórek endokrynnych wydzielających gastrynę, histaminę, melatoninę i serotoninę. Główne hormony i aminy biogenne wytwarzane przez strefę antropylorudwunastniczą biorą udział zarówno w stymulowaniu wydzielania żołądkowego, jak i zmianie trofizmu i proliferacji komórek, głównie w tej strefie. Na tle aktywnego bakteryjnego zapalenia żołądka i dwunastnicy powstają sprzyjające warunki do powstawania owrzodzeń. Wraz z powstaniem defektu trawiennego zmniejsza się aktywność funkcjonalna komórek endokrynnych. Prowadzi to do zmniejszenia agresji kwasowo-dwunastniczej, poprawy trofizmu tkanek w strefie antropylorodunalnej i stworzenia warunków do gojenia się wrzodów żołądka i dwunastnicy, nawet na tle postępującej ekspansji mikrobiologicznej HP. W ostrym okresie choroby wrzodowej obserwuje się przerost komórek wytwarzających α-endorfiny, które są uniwersalnymi cytoprotektorami. Pełnią one rolę głównych mechanizmów ochronnych w chorobie wrzodowej i zapewniają proces samoograniczenia wrzodu i jego gojenia, zarówno bezpośrednio, jak i poprzez stymulację układu odpornościowego. Jednocześnie przeciwciała przeciwko HP, syntetyzowane w błonie podśluzowej żołądka i dwunastnicy, skutecznie wiążą się z komórkami bakteryjnymi i neutralizują toksyny HP oraz przyczyniają się do ich śmierci. Wszystko to przyczynia się do stworzenia równowagi między tzw. czynnikami agresji a czynnikami ochrony i gojenia się wady trawiennej w obrębie żołądka i dwunastnicy. Klasyfikacja. Klasyfikacja (Panfilov Yu. A., Osadchuk M. A., 1991) Lokalizacja wady trawiennej: 1) wrzód żołądka (przekroje podsercowe i sercowe, część odźwiernika i kanał odźwiernika, skrzywienie mniejsze i większe); 2) wrzód dwunastnicy (odcinek opuszkowy i zaopuszkowy); 3) wrzody żołądka i dwunastnicy. Przebieg choroby wrzodowej. 1. Łatwy. Zaostrzenie owrzodzenia trwa nie więcej niż 1 raz w ciągu 1-3 lat, wygojenie wady trawiennej kończy się w 5-6 tygodniu od rozpoczęcia terapii, nasilenie objawów bólowych i dyspeptycznych jest umiarkowane. 2. Umiarkowane. Nawrót co najmniej 2 razy w roku, nabłonek wrzodowy - w ciągu 7-12 tygodni nasilenie bólu i zespoły dyspeptyczne. 3. Ciężki. Okresy remisji nie przekraczają 3-4 miesięcy. Oprócz silnego bólu występują komplikacje. Fazy choroby: 1) zaostrzenie nawrotów wrzodów lub zaburzeń czynnościowych układu żołądkowo-dwunastniczego; 2) całkowita remisja (w aspekcie klinicznym, radiologicznym, endoskopowym i czynnościowym); 3) niekompletny (z zachowaniem zaburzeń czynnościowych lub strukturalnych w strefie żołądka i dwunastnicy). Stan błony śluzowej żołądka i dwunastnicy: 1) przewlekłe zapalenie żołądka; 2) przewlekłe zapalenie dwunastnicy. Stan funkcjonalny układu żołądkowo-dwunastniczego Wydzielina: normalna, zwiększona, zmniejszona. Ruchliwość: normalna, przyspieszona, wolna; ewakuacja: normalna, przyspieszona, opóźniona, dwunastostaza. Powikłania: krwawienie, perforacja, penetracja, zapalenie perygastritis, periduodenitis, bliznowacenie żołądka i dwunastnicy. Obraz kliniczny. Obraz kliniczny choroby wrzodowej jest polimorficzny. Objawy zależą od płci i wieku pacjenta, pory roku, lokalizacji i wielkości owrzodzenia, cech osobistych i społecznych pacjenta oraz jego kwalifikacji zawodowych. Klinikę określa kombinacja objawów: przewlekły przebieg choroby od momentu jej wystąpienia, obecność objawów zaostrzenia i remisji choroby, gojenie się ubytku błony śluzowej żołądka i dwunastnicy z utworzeniem blizna. Wrzód trawienny jest reprezentowany przez dwa warianty kliniczne i morfologiczne: wrzód żołądka i wrzód dwunastnicy. Tradycyjnie rozróżnia się zespoły bólowe i dyspeptyczne. Wiodącym objawem klinicznym jest ból w górnej części brzucha. Z natury zespołu bólowego prawie niemożliwe jest odróżnienie przewlekłego bakteryjnego zapalenia żołądka od wrzodu trawiennego. Ból w nadbrzuszu, na czczo, głównie wiosną i jesienią, jest równie powszechny zarówno w chorobie wrzodowej, jak i przewlekłym bakteryjnym zapaleniu żołądka. Złagodzenie zespołu bólowego za pomocą pokarmowych i leczniczych środków zobojętniających kwas osiąga się zarówno w przewlekłym bakteryjnym zapaleniu żołądka, jak i wrzodzie trawiennym. Charakterystyczną cechą wrzodu dwunastnicy jest jedynie obecność bólu w nadbrzuszu w nocy. Wymioty z wrzodem trawiennym są rzadkie. Nudności są znacznie częstsze w przypadku wrzodów żołądka i dwunastnicy. Zaparcie towarzyszy przewlekłemu wrzodowi dwunastnicy. Objawy choroby wrzodowej są determinowane liczbą defektów wrzodziejących i ich lokalizacją. Mnogie wrzody żołądka występują 3 razy częściej u mężczyzn. Obraz kliniczny w tym przypadku zależy od lokalizacji wad trawiennych. W przypadku wrzodów w ciele żołądka obserwuje się tępy ból w nadbrzuszu bez napromieniania, który występuje 20-30 minut po jedzeniu i nudności. W przypadku owrzodzeń okolicy podsercowej charakterystyczne są tępe bóle w procesie wyrostka mieczykowatego, promieniujące do lewej połowy klatki piersiowej. Połączone wrzody żołądka i wrzody dwunastnicy są połączeniem czynnego wrzodu żołądka i wygojonego wrzodu dwunastnicy. Charakteryzują się długotrwałym utrzymywaniem zespołu bólowego, uporczywym przebiegiem choroby, częstymi nawrotami choroby, powolnym bliznowaceniem owrzodzenia i częstymi powikłaniami. Owrzodzenia pozabulwiaste obejmują owrzodzenia zlokalizowane w okolicy zwieracza opuszkowo-dwunastniczego i dystalnie do niego. Ich obraz kliniczny ma swoje własne cechy i ma wiele wspólnego z wrzodami dwunastnicy. Występują głównie u pacjentów w wieku 40-60 lat. Owrzodzenia pozaopuszkowe są ciężkie i podatne na częste zaostrzenia, którym towarzyszy masywne krwawienie. Ból zlokalizowany w prawym górnym kwadrancie brzucha, promieniujący do pleców lub pod prawą łopatką, występuje w 100% przypadków. Nasilenie, nasilenie bólu, który ustępuje dopiero po zażyciu narkotycznych leków przeciwbólowych, doprowadza pacjentów do ciężkiej neurastenii. Sezonowość zaostrzeń owrzodzeń pozabulwiastych odnotowuje się u prawie 90% pacjentów. U wielu pacjentów krwawienie z przewodu pokarmowego staje się objawem kardynalnym. Owrzodzenia kanału odźwiernika charakteryzują się zespołem objawów zwanym zespołem odźwiernika: bóle w nadbrzuszu, nudności, wymioty i znaczna utrata masy ciała. Zaostrzenie choroby trwa bardzo długo. Na tle intensywnej terapii przeciwwrzodowej blizna wrzodowa zanika w ciągu 3 miesięcy. Obfity dopływ krwi do kanału odźwiernika powoduje masywne krwawienie z żołądka. diagnostyka. W niepowikłanym przebiegu wrzodu trawiennego nie ma zmian w ogólnych badaniach krwi, możliwe jest nieznaczne zmniejszenie ESR i niewielka erytrocytoza. Kiedy w badaniach krwi pojawiają się powikłania, pojawia się niedokrwistość, leukocytoza - gdy otrzewna jest zaangażowana w proces patologiczny. Nie ma zmian w ogólnej analizie moczu. W analizie biochemicznej krwi w przypadkach powikłanego przebiegu choroby wrzodowej możliwe są zmiany parametrów próby sialowej, białka C-reaktywnego, odczynu DPA. Tradycyjną metodą badań w patologii żołądka jest określenie kwasowości treści żołądkowej. Możliwe są różne wskaźniki: podwyższone i normalne, w niektórych przypadkach nawet obniżone. Wrzód dwunastnicy występuje przy wysokiej kwasowości soku żołądkowego. W badaniu rentgenowskim wrzód trawienny jest „niszą” - magazynem zawiesiny baru. Poza tak bezpośrednim objawem radiograficznym, w diagnostyce ważne są pośrednie objawy wady trawiennej: nadmierne wydzielanie treści żołądkowej na czczo, zaburzenia opróżniania, refluks dwunastniczy, dysfunkcja serca, skurcze miejscowe, zbieżność fałdów błony śluzowej, bliznowata deformacja żołądka i dwunastnicy. Gastroduodenoskopia z biopsją jest najbardziej wiarygodną metodą diagnozowania choroby wrzodowej. Pozwala ocenić charakter zmian w błonie śluzowej na krawędzi owrzodzenia, w strefie okołowrzodowej i gwarantuje trafność diagnozy na poziomie morfologicznym. Badania endoskopowe i morfologiczne wykazały, że większość owrzodzeń żołądka znajduje się w okolicy krzywizny mniejszej i antrum, znacznie rzadziej - na krzywiźnie większej oraz w okolicy kanału odźwiernika. 90% owrzodzeń dwunastnicy znajduje się w okolicy opuszkowej. Wrzód trawienny jest zwykle okrągły lub owalny. Jej dno składa się z martwiczych mas, pod którymi znajduje się ziarnina. Obecność ciemnych plam na dnie wskazuje na krwawienie. Faza gojenia owrzodzenia charakteryzuje się zmniejszeniem przekrwienia błony śluzowej i wału zapalnego w strefie okołowrzodowej. Ubytek staje się mniej głęboki, stopniowo usuwany z włóknistej płytki nazębnej. Blizna wygląda jak przekrwiony obszar błony śluzowej z liniowymi lub gwiaździstymi cofnięciami ściany. W przyszłości podczas badania endoskopowego w miejscu dawnego owrzodzenia określa się różne naruszenia odciążenia błony śluzowej: deformacje, blizny, zwężenia. W endoskopii dojrzała blizna z powodu zastąpienia ubytku tkanką ziarninową ma białawy wygląd, nie ma oznak aktywnego zapalenia. W badaniu morfologicznym wycinka biopsyjnego pobranego z dna i brzegów owrzodzenia ujawniono pozostałości komórkowe w postaci nagromadzenia śluzu z domieszką gnijących leukocytów, erytrocytów i złuszczonych komórek nabłonka, pod którymi znajdują się włókna kolagenowe. Diagnostyka różnicowa. Wraz z powszechnym stosowaniem endoskopii diagnostyka różnicowa owrzodzeń żołądka i dwunastnicy (wrzody objawowe, owrzodzenia specyficzne w gruźlicy, kiła, choroba Leśniowskiego-Crohna, pierwotny rak wrzodziejący, wtórne wrzody złośliwe) staje się szczególnie ważna. W przypadku owrzodzeń objawowych musi istnieć przyczyna, która je spowodowała (ekstremalne narażenie, kliniczne i morfologiczne objawy chorób endokrynologicznych, zaburzenia sercowo-naczyniowe i oddechowe, choroby reumatyczne). Bardziej niż w przypadku wrzodów trawiennych charakteryzują się mnogością zmian, dominującą lokalizacją w żołądku i znacznym rozmiarem. W przypadku wrzodu trawiennego dominuje zespół bólowy, a przy przewlekłym zapaleniu żołądka - objawy dyspeptyczne. W przewlekłym zapaleniu żołądka ból jest łagodny lub nieobecny, nie ma sezonowości choroby i ograniczony ból w badaniu palpacyjnym; zaostrzenie choroby często zależy od rodzaju żywności. Stan funkcji wydzielniczej żołądka z zapaleniem żołądka może być inny. Decydujące znaczenie ma gastroskopia i gastrobiopsja, w których wykrywa się zmiany w błonie śluzowej charakterystyczne dla zapalenia żołądka i wrzodu w chorobie wrzodowej. Przepuklinom rozworu przełykowego (HH) często towarzyszy również ból w nadbrzuszu. Jednak w przeciwieństwie do choroby wrzodowej, choroba ta charakteryzuje się głównie podeszłym wiekiem pacjentów, związkiem bólu z pozycją ciała (ból nasila się w pozycji leżącej, słabnie w pozycji pionowej). Rozpoznanie HH potwierdzają wyniki badania rentgenowskiego. Przewlekłe zapalenie pęcherzyka żółciowego charakteryzuje się bólem w prawym podżebrzu i nadbrzuszu, często promieniującym do prawej łopatki, do barku, do kąta żuchwy po prawej stronie. W przypadku niekamiczego zapalenia pęcherzyka żółciowego mają nudny, monotonny, uciskowy charakter, a przy kamienistym zapaleniu pęcherzyka żółciowego nabierają charakteru kolki. Obserwuje się nudności, zaparcia, wzdęcia. Możliwy jest trwały stan podgorączkowy. Przy przedłużającej się niedrożności dróg żółciowych może dołączyć żółtaczka. Rozpoznanie uszkodzenia dróg żółciowych jest weryfikowane przez dane USG jamy brzusznej, badanie rentgenowskie (cholecystografia), endoskopową cholepankreatografię wsteczną (ERCP), a także wyniki sondowania dwunastnicy, które są wskazane tylko dla procesu bezkamiennego. W ostrym zapaleniu trzustki i zaostrzeniu przewlekłego bólu zlokalizowane są w lewej połowie nadbrzusza, mają charakter półpaśca, wywołany spożyciem jakiegokolwiek pokarmu. W wywiadzie - patologia układu żółciowego, nadużywanie alkoholu, długotrwałe stosowanie leków trzustkowych. Obiektywnie ujawniają utratę wagi, wielokałową, steatorrhea, twórcęrhea. Diagnozę potwierdzają wyniki biochemicznego badania krwi na enzymy trzustkowe, kał - na strawność, a także dane instrumentalne. Leczenie. Racjonalne leczenie wrzodów trawiennych powinno obejmować schemat leczenia, odpowiednie odżywianie, leczenie farmakologiczne, psychoterapię, metody leczenia fizykalnego i uzdrowiskowego. W okresie zaostrzenia choroby wrzodowej konieczne jest ścisłe przestrzeganie diety ułamkowej (od 4 do 6 razy dziennie przy niewielkiej objętości każdej porcji pokarmu przyjmowanej w określonych godzinach). Produkty spożywcze muszą charakteryzować się dobrymi właściwościami buforującymi i zawierać odpowiednią ilość białka (120-140 g). Psychoterapia jest niezbędna do zatrzymania lub zredukowania reakcji psychoneurotycznych wynikających z zespołu przewlekłego bólu i jego oczekiwania. Leki stosowane w leczeniu wrzodów trawiennych dzielą się na 5 grup: 1) leki wpływające na czynnik kwasowo-peptyczny (leki zobojętniające i H2blokery histaminy, inne środki przeciwwydzielnicze); 2) leki poprawiające barierę śluzówkową żołądka; 3) leki zwiększające syntezę endogennych prostaglandyn; 4) środki przeciwbakteryjne i antyseptyczne; 5) leki normalizujące zaburzenia motoryczno-ewakuacyjne żołądka i dwunastnicy. Leki zobojętniające: 1) rozpuszczalny (wchłanialny) - wodorowęglan sody, węglan wapnia (kreda) i tlenek magnezu (magnezja palona); 2) nierozpuszczalne (niewchłanialne): trójkrzemian magnezu i wodorotlenek glinu. Rozpuszczalne leki zobojętniające mają szybkie, energetyczne, ale krótkotrwałe działanie alkalizujące, ale często powodują działania niepożądane, dlatego nie stosuje się ich w leczeniu wrzodów trawiennych. Nierozpuszczalne leki zobojętniające na bazie wodorotlenku glinu i wodorotlenku magnezu (Almagel, Phosphalugel, Gelusillac, Topaal, Maalox itp.) zapewniają długotrwałą neutralizację kwasu solnego, otaczają błonę śluzową, chroniąc ją przed szkodliwym działaniem kwasu i żywności. Oprócz neutralizacji kwasu solnego, zmniejszają aktywność proteolityczną soku żołądkowego, wiążą lizolecytynę i kwasy żółciowe, mają uniwersalne działanie cytoprotekcyjne. Leki zobojętniające sok żołądkowy należy przyjmować 1-2 godziny po posiłku i wieczorem. Maalox jest przepisywany w postaci zawiesiny (15 ml 4 razy dziennie) lub tabletek (1-2 tabletki 4 razy dziennie), fosfalugel - w postaci żelu (16 g 3-4 razy dziennie). Jednym z głównych skutków ubocznych niewchłanialnych środków zobojętniających kwas jest zaburzenie stolca. Preparaty wodorotlenku glinu powodują zaparcia, a preparaty wodorotlenku magnezu (Maalox) mają zależne od dawki działanie przeczyszczające. Nowa era w leczeniu wrzodów trawiennych rozpoczęła się wraz z pojawieniem się H2- blokery histaminy. W warunkach fizjologicznych histamina pośredniczy w bodźcach nerwu pozażołądkowego i humoralnych, które powodują wytwarzanie kwasu. Stymulacja produkcji kwasu solnego przez histaminę spowodowana jest zwiększeniem aktywności cAMP, który oddziałuje na enzym adenylocyklazę zawarty w obszarze żołądka wytwarzającym kwas, który wzmaga sekrecję jonów wodorowych. Uzyskane dane były podstawą do syntezy leków przerywających udział histaminy w procesie wydzielania na poziomie komórkowym, takich jak cymetydyna, ranitydyna, famotydyna, nizatydyna itp. Ponadto antagoniści receptora H2Receptory histaminowe zapobiegają zaburzeniom mikrokrążenia w błonie śluzowej żołądka, a tym samym zapobiegają powstawaniu wrzodów. Ponadto zmniejszają produkcję pepsyny, zwiększają wydzielanie wodorowęglanów, normalizują motorykę żołądka i dwunastnicy, zwiększają liczbę komórek nabłonka syntetyzujących DNA, stymulując procesy naprawcze i przyspieszając gojenie przewlekłych wrzodów żołądka i dwunastnicy. Jednak leki I generacji (cymetydyna, cynamet, belomet, tagamet) mogą powodować zmiany w układzie nerwowym, toksyczne zapalenie wątroby, zaburzenia rytmu i przewodzenia w układzie sercowo-naczyniowym oraz zmiany w narządach krwiotwórczych. Blokery H2Kolejne generacje receptorów histaminowych - ranitydyna (zantak, ranisan, gistak), famotydyna (kvamatel, lecedil, gastrosidin), nizatydyna (roksatydyna) różnią się dobrą tolerancją od cymetydyny. Ranitydyna jest przepisywana w dawce 150 mg 2 razy dziennie, famotydyna - 20 mg 2 razy dziennie przez 4-6 tygodni. Aby zapobiec zespołowi odstawienia po wygojeniu wrzodów, zaleca się kontynuowanie przyjmowania ranitydyny (150 mg) lub famotydyny (20 mg) na noc przez 2-3 miesiące. W ostatnich latach pojawił się nowy lek przeciwwydzielniczy omeprazol (omenrol, omez, lozek), który należy do pochodnych benzimidazolu. Blokuje enzym H + -K + -ATPazę pompy protonowej komórki okładzinowej. Krótki okres półtrwania (około 1 godziny) i długi czas działania (18-24 godziny) umożliwiają jednorazowe zażycie tego leku. Omeprazol jest przepisywany w dawce 20 mg na noc 1 raz dziennie przez 2-3 tygodnie. Omeprazol zajmuje pierwsze miejsce pod względem nasilenia działania przeciwwydzielniczego wśród nowoczesnych leków przeciwwrzodowych.Skutki uboczne leku nie są bardzo wyraźne. Powszechne zastosowanie w leczeniu wrzodów trawiennych znalazła gastrocepina (nirenzepina, gastrozepina), która należy do leków antycholinergicznych. Lek selektywnie blokuje muskarynowe receptory acetylocholiny znajdujące się w komórkach błony śluzowej żołądka, które wytwarzają kwas solny i pepsynę. Gastrocepina działa hamująco na podstawowe i stymulowane wydzielanie żołądkowe, hamuje produkcję pepsyny, spowalnia opróżnianie żołądka, powoduje zahamowanie produkcji gastryny, obniża poziom polipeptydu trzustkowego, działa cytoochronnie poprzez zwiększenie produkcji glikoprotein śluzu żołądkowego , a także poprzez poprawę ukrwienia błony śluzowej żołądka i dwunastnicy . Przypisz go do 50 mg 2 razy dziennie 30 minut przed posiłkiem. Przebieg leczenia wynosi średnio 4 tygodnie. Do leków wzmacniających barierę śluzową żołądka zalicza się preparaty bizmutu koloidalnego (denol), który tworzy film ochronny na błonie śluzowej, zmniejsza aktywność trawienną żołądka, tworząc nierozpuszczalny związek z pepsyną, wzmaga tworzenie się śluzu, działa cytoprotekcyjnie działanie zwiększające zawartość prostaglandyn w ścianie żołądka. Denol ma zdolność hamowania aktywności HP w błonie śluzowej żołądka. Lek jest przepisywany 2 tabletki (240 mg) 2 razy dziennie na pół godziny przed posiłkiem lub 2 godziny po posiłku. Aby uniknąć gromadzenia się soli bizmutu w organizmie, nie zaleca się prowadzenia terapii tymi lekami dłużej niż 8 tygodni. W leczeniu przeciwbakteryjnym wrzodów żołądka i dwunastnicy stosuje się tetracyklinę, amoksycylinę i klarytromycynę. Stosuje się je w połączeniu z innymi lekami przeciwwrzodowymi. Zaproponowano kilka schematów terapii skojarzonej (dwu-, trzy-, czteroskładnikowej). Terapia dwuskładnikowa: amoksycylina 1000 mg 2 razy dziennie przez 2 tygodnie; omeprazol 40 mg dwa razy na dobę. Schemat trójskładnikowy obejmuje przygotowanie bizmutu koloidalnego 2 mg 120 razy dziennie; tetracyklina 4 mg 250 razy dziennie; metronidazol 4 mg 250 razy dziennie. Cykl terapii trwa 4 dni. Schemat czteroskładnikowy obejmuje 20 mg omeprazolu 2 razy dziennie od 1 do 10 dnia; de-nol 120 mg 4 razy dziennie od 4 do 10 dnia; tetracyklina 500 mg 4 razy dziennie od 4 do 10 dnia; metronidazol 500 mg 3 razy dziennie od 4 do 10 dnia. Czteroskładnikowy schemat leczenia wrzodu trawiennego żołądka i dwunastnicy jest uznawany za najbardziej skuteczny. Po 6 tygodniach wygojenie wady trawiennej obserwuje się u 93-96% pacjentów. Po bliznowaceniu wrzodu trawiennego żołądka i dwunastnicy tradycyjnie stosuje się dwa rodzaje leczenia. 1) Ciągłą terapię podtrzymującą prowadzi się lekami przeciwwydzielniczymi w połowie dziennej dawki przez okres do jednego roku. 2) Terapia „na żądanie”, polega na stosowaniu jednego ze środków przeciwwydzielniczych w połowie dziennej dawki przez dwa tygodnie, gdy pojawią się objawy wrzodu trawiennego. Rokowanie i zapobieganie. Nieskomplikowane formy choroby mają korzystne rokowanie w życiu i pracy. W przypadku powikłań choroby wrzodowej o rokowaniu decyduje terminowość leczenia operacyjnego. Zapobieganie nawrotom wrzodów trawiennych obejmuje monitorowanie dynamiczne z obowiązkowymi badaniami kontrolnymi przez lekarza 2 razy w roku. Badania powinny obejmować badanie kliniczne i endoskopowe oraz, w razie potrzeby, badanie morfologiczne. Jako środek zapobiegawczy zaleca się normalizację snu i odpoczynku, rezygnację ze złych nawyków, ograniczenie przyjmowania leków wrzodziejących, racjonalne pięć posiłków dziennie oraz stosowanie dwu- lub trzyskładnikowej terapii przez tydzień co 3 miesiące. WYKŁAD nr 12. Choroby przewodu pokarmowego. Choroby jelit. Choroby jelita cienkiego. Przewlekłe zapalenie jelit Przewlekłe zapalenie jelit to choroba jelita cienkiego, charakteryzująca się naruszeniem jego funkcji (trawienie i wchłanianie) na tle zmian dystroficznych i dysregeneracyjnych, których kulminacją jest rozwój stanu zapalnego, zanik i stwardnienie błony śluzowej jelita cienkiego. Etiologia i patogeneza. Jest to choroba polietiologiczna, która może być następstwem ostrego zapalenia jelita cienkiego lub pierwotnego procesu przewlekłego. W ostatnich latach duże znaczenie jako czynnik etiologiczny przewlekłego zapalenia jelit zyskały Yersinia, Helicobacteria, Proteus, Pseudomonas aeruginosa, rotawirusy, liczni przedstawiciele pierwotniaków i robaków pasożytniczych (giardia, ascaris, tasiemce, opistorchia, cryptosporidium). Duże znaczenie w występowaniu przewlekłego zapalenia jelit mają czynniki pokarmowe - przejadanie się, jedzenie suchej karmy, niezrównoważone, głównie węglowodanowe pokarmy, nadużywanie przypraw. Zapalenie jelit jest spowodowane promieniowaniem jonizującym, narażeniem na substancje toksyczne i leki. Wśród powszechnych mechanizmów patogenetycznych przewlekłych chorób jelita cienkiego występują zmiany w mikroflorze jelitowej na tle zmniejszenia odporności miejscowej i ogólnej. Zmiany stanu immunologicznego - zmniejszenie zawartości wydzielniczej IgA, wzrost poziomu IgE, zmniejszenie transformacji blastycznej limfocytów i zahamowanie migracji leukocytów - prowadzą do kolonizacji jelita cienkiego przez przedstawicieli mikroflory oportunistycznej i spadek normalnej flory beztlenowej. Kolonizacja bakteryjna jelita cienkiego wzmaga wydzielanie jelitowe dzięki aktywacji cAMP komórek nabłonka, co zwiększa przepuszczalność jelit, wzmaga produkcję elektrolitów i wody przez komórki. Wydzielanie wody i elektrolitów prowadzi do zaburzenia metabolizmu wody i soli. Pod wpływem flory bakteryjnej dochodzi do zaburzeń krążenia jelitowo-wątrobowego żółci. Kwasy tłuszczowe wiążą jony wapnia, tworząc trudno rozpuszczalne mydła, które są wydalane z kałem. Zaburzeniu metabolizmu wapnia sprzyjają zmiany w metabolizmie witaminy D, co zmniejsza wchłanianie wapnia. Pod wpływem zaburzeń metabolicznych witamin rozpuszczalnych w tłuszczach zmniejsza się zawartość mikroelementów we krwi. Przedłużająca się dysbioza sprzyja uczuleniu na antygeny drobnoustrojów i pokarmów, powoduje zapalenie immunologiczne błony śluzowej, co skutkuje powstawaniem antygenów tkankowych. Zwiększonej przepuszczalności bariery śluzowej towarzyszy resorpcja nierozszczepionych makrocząsteczek białkowych, które stają się alergenami i osłabiona jest reaktywność immunologiczna. W przypadku alergii uwalniane są substancje biologicznie czynne, które zwiększają przepuszczalność ściany jelita, zmieniają właściwości funkcjonalne enterocytów. Naruszenie mikrostruktury błony cytoplazmatycznej enterocytu prowadzi do zahamowania najpierw aktywności laktazy, a następnie maltazy i sacharazy. Przy dystroficznych, dysregeneracyjnych zmianach w nabłonkach zmniejsza się synteza enzymów i ich sorpcja na błonach nabłonka - disacharydazy, peptydazy, enterokinaza, fosfataza alkaliczna, co powoduje zaburzenia trawienia zarówno błony, jak i jamy. Wszystko to staje się podstawą zespołu złego wchłaniania. We wczesnych stadiach choroby rozwijają się zaburzenia metabolizmu lipidów na skutek zmniejszenia wchłaniania tłuszczu, jego utraty z kałem oraz zmian w fazie jelitowej jelitowo-wątrobowego krążenia żółciowego. Naruszenie metabolizmu żółci prowadzi z kolei do naruszenia metabolizmu lipidów, co wpływa na strukturę i funkcję błon komórkowych. W związku z niewystarczającym wchłanianiem tłuszczu dochodzi do naruszenia syntezy steroidów, co powoduje naruszenie funkcji gruczołów dokrewnych. Morfologicznie przewlekłe zapalenie jelit objawia się zmianami zapalnymi i dysregeneracyjnymi błony śluzowej jelita cienkiego. Jeśli proces postępuje, obserwuje się jego atrofię i stwardnienie. Klasyfikacja (Zlatkina A.R., Frolkis A.V., 1985). 1) Etiologia: infekcje jelitowe, inwazje robaków, czynniki pokarmowe, fizyczne i chemiczne, choroby żołądka, trzustki, dróg żółciowych. 2) Fazy choroby: zaostrzenie; umorzenie. 3) Stopień nasilenia: łagodny; umiarkowany; ciężki. 4) Prąd: monotonny; nawracający; stale powtarzające się; utajony. 5) Charakter zmian morfologicznych: zespół bez atrofii; zapalenie jelita grubego z umiarkowaną częściową atrofią kosmków; zapalenie jelit z częściowym zanikiem kosmków; jednostka z całkowitym zanikiem kosmków. 6) Charakter zaburzeń czynnościowych: zaburzenia trawienia błon (niedobór disacharydazy), zaburzenia wchłaniania wody, elektrolitów, pierwiastków śladowych, witamin, białek, tłuszczów, węglowodanów. 7) Powikłania: zapalenie słoneczne, niespecyficzne zapalenie mesadenu. Obraz kliniczny. Na obraz kliniczny przewlekłego zapalenia jelit składają się lokalne i ogólne zespoły jelitowe. Pierwszy jest spowodowany naruszeniem procesów trawienia ciemieniowego (błonowego) i jamy ustnej (złe trawienie). Pacjenci skarżą się na wzdęcia, bóle w okolicy pępkowej, wzdęcia w kształcie kapelusza, głośne dudnienie, biegunkę i rzadziej zaparcia. Palpacja ujawnia ból w śródbrzuszu, a także po lewej stronie i powyżej pępka (dodatni objaw Porgesa), pluskanie w okolicy jelita ślepego (objaw Obraztsova). Kał przybiera gliniasty wygląd i charakterystyczna jest materia polifekalna. Ogólny zespół jelitowy związany jest z zaburzeniami wchłaniania składników pokarmowych (złe wchłanianie), co skutkuje zaburzeniami wszystkich typów metabolizmu, zmianami homeostazy. Charakteryzuje się wieloaspektowymi zaburzeniami metabolicznymi, przede wszystkim białkowymi, co objawia się postępującą utratą masy ciała. Zmiany w metabolizmie węglowodanów są mniej wyraźne, co objawia się wzdęciami, dudnieniem w jamie brzusznej oraz nasiloną biegunką podczas przyjmowania nabiału. W dużej mierze niedobór masy ciała u pacjentów wynika nie tylko z braku białka, ale także z braku równowagi lipidowej. Zmiany w metabolizmie lipidów są ściśle związane z zaburzeniami metabolicznymi witamin rozpuszczalnych w tłuszczach i minerałów (wapń, magnez, fosfor). Charakterystyczne objawy niedoboru wapnia to pozytywny objaw wałka mięśniowego, drgawki, nawracające „niezmotywowane” złamania kości, osteoporoza, osteomalacja. Występują również obrzęki twarzy, sinica warg, zapalenie języka, drażliwość, zły sen. Naruszenie równowagi wodno-elektrolitowej objawia się ogólnym osłabieniem, brakiem aktywności fizycznej, niedociśnieniem mięśniowym, nudnościami, wymiotami i zmianami w ośrodkowym układzie nerwowym. Objawy polihipowitaminozy stają się typowe dla przewlekłego zapalenia jelit o umiarkowanym i ciężkim nasileniu. Hipowitaminoza C objawia się klinicznie krwawieniem z dziąseł, powtarzającym się krwawieniem z nosa, macicy, siniakami na skórze. Hipowitaminozie B towarzyszy bladość skóry, zapalenie języka, kątowe zapalenie jamy ustnej (cheilez). Oznaki niedoboru witamin rozpuszczalnych w tłuszczach (A, O, E, K): słabe widzenie o zmierzchu, suchość skóry i błon śluzowych, zwiększone krwawienie dziąseł. Ciężkie postacie przewlekłego zapalenia jelit występują z objawami zaburzeń endokrynologicznych (niewydolność opłucnej). Hipokortyka objawia się niedociśnieniem tętniczym, zaburzeniami rytmu serca, anoreksją i pigmentacją skóry. Spadkowi aktywności gonad towarzyszą zaburzenia czynności jajników, zaburzenia miesiączkowania, u mężczyzn impotencja, ginekomastia, wypadanie włosów. Dysfunkcja tarczycy charakteryzuje się ogólnym osłabieniem, suchością skóry, bradykardią, obniżoną wydajnością i zaburzeniami intelektualno-mnestycznymi. Diagnoza i diagnostyka różnicowa. Ogólne badanie krwi ujawnia niedokrwistość mikro- i makrocytarną, wzrost ESR, aw ciężkich przypadkach - limfo- i eozynopenię. Jeśli choroba ma podłoże pasożytnicze, we krwi można zaobserwować limfocytozę i eozynofilię. W badaniu skatologicznym stwierdza się jelitową biegunkę tłuszczową spowodowaną kwasami tłuszczowymi i mydłami, twórca, amylorrhea. Zwiększa się zawartość enterokinazy i fosfatazy alkalicznej w kale. Dzienna masa kału znacznie wzrasta. Analiza bakteriologiczna kału ujawnia dysbakteriozę w różnym stopniu. Występuje spadek lakto- i bifidobakterii, pojawiają się enterokoki, szczepy Escherichia coli o zmienionych właściwościach enzymatycznych. W ogólnej analizie moczu w ciężkiej postaci przewlekłego zapalenia jelit odnotowuje się mikroalbuminurię i migrohematurię. W biochemicznym badaniu krwi wykrywa się hipoproteinemię, hipoalbuminemię, hipoglobulinemię, hipokalcemię, obniżenie poziomu magnezu, fosforu i innych mikroelementów, zaburzenia metabolizmu elektrolitów w postaci obniżenia poziomu sodu i potasu. Zaburzeniom metabolizmu lipidów towarzyszą zmiany w spektrum lipidów: obniża się poziom cholesterolu, fosfolipidów, zmienia się także spektrum kwasów żółciowych, fosfolipidów i trójglicerydów. Wyniki badania rentgenowskiego pozwalają na wyjaśnienie funkcji motorycznej jelita cienkiego oraz odciążenie śluzówki, zmiany dystoniczne i dyskinetyczne w postaci spowolnienia lub przyspieszenia przejścia zawiesiny siarczanu baru przez jelito cienkie , a odciążenie błony śluzowej zmienia się w postaci nierównomiernego pogrubienia, deformacji i wygładzenia fałdów. Gastroduodenoskopia ujawnia zanikowe zapalenie żołądka i dwunastnicy. Obraz morfologiczny łagodnej postaci przewlekłego zapalenia jelit charakteryzuje się pogrubieniem kosmków, ich deformacją, zmniejszeniem głębokości nacięć, zmniejszeniem napięcia mięśni gładkich, obrzękiem podnabłonkowym, zmianami zwyrodnieniowymi powierzchni nabłonka , ścieńczenie rąbka szczoteczkowego komórek, zmniejszenie liczby komórek kubkowych w okolicy kosmków, zwiększenie liczby krypt, naciekanie błony śluzowej warstwy własnej elementami limfoplazmatycznymi, zmniejszenie liczby komórek Panetha w okolicy dna krypt. Dla postaci umiarkowanej typowe są częściowe zaniki kosmków, zmniejszenie liczby krypt, ścieńczenie błony śluzowej, zmniejszenie rąbka szczoteczkowego i naciek limfoplazmatyczny warstwy podśluzówkowej i mięśniowej. Ciężka postać choroby charakteryzuje się postępującym zanikiem kosmków, diagnozowanym na podstawie kryteriów histologicznych, histochemicznych i morfometrycznych. Proces proliferacji enterocytów przeważa nad ich różnicowaniem, pojawia się obfitość niedojrzałych, wadliwych komórek. Diagnostykę różnicową w przewlekłym zapaleniu jelit przeprowadza się z celiakią, chorobą Leśniowskiego-Crohna, chorobą Whipple'a, amyloidozą jelitową, chorobą uchyłkową, chłoniakiem, guzami jelita cienkiego. Wspólne dla wszystkich tych stanów są kliniczne zespoły niestrawności, wchłaniania i dysbakteriozy. Ostateczną diagnozę potwierdza badanie morfologiczne błony śluzowej jelita cienkiego. Tak więc w przypadku enteropatii celiakii typowe jest anamnestyczne wskazanie związku zaostrzeń choroby z użyciem produktów zawierających gliadynę. Klinika enteropatii trzewnej przypomina przewlekłe zapalenie jelit. Najczęściej dotyczy to górnych jelit i nie ma zmian w jelicie krętym. Optymalnym miejscem pobierania próbek biopsyjnych jest obszar błony śluzowej w pobliżu więzadła Treitza. Badanie morfologiczne ujawnia zmniejszenie liczby komórek kubkowych i wzrost liczby limfocytów międzynabłonkowych, subtotalny zanik kosmków i naciek komórek zapalnych własnej warstwy. W przypadku enteropatii trzewnej zmiany morfologiczne na tle diety bezglutenowej są odwracalne, w przeciwieństwie do banalnego przewlekłego zapalenia jelit, w którym zmiany morfologiczne są nieodwracalne. W chorobie Leśniowskiego-Crohna obserwuje się polimorfizm kliniczny ze względu na autoimmunologiczną genezę choroby i jej charakterystyczne objawy ogólnoustrojowe (takie jak autoimmunologiczne zapalenie tarczycy, zapalenie wielostawowe, zapalenie tęczówki, zapalenie wątroby, częste połączenie zapalenia jelit i dystalnego zapalenia jelita grubego). Badania endoskopowe i morfologiczne mają wysoką rozdzielczość w weryfikacji choroby Leśniowskiego-Crohna, ujawniając mozaikowatość zmiany jelitowej, typowe zmiany typu „kostka brukowa”, na przemian z obszarami nienaruszonej błony śluzowej. RTG, badanie endoskopowe może wykryć zwężenia jelit, czasami tworzą się przetoki jelitowe. Diagnostyka morfologiczna stwierdza naciek komórek zapalnych wszystkich warstw ściany jelita z maksymalnym uszkodzeniem warstwy podśluzówkowej i minimalnymi zmianami w błonie śluzowej. W warstwie podśluzówkowej stwierdza się patognomoniczne dla tej choroby ziarniniaki limfocytarne podobne do sarkoidozy. Choroba Whipple'a, oprócz objawów zapalenia jelit, charakteryzuje się objawami pozajelitowymi w postaci gorączki, zapalenia stawów, limfadenopatii, niedociśnienia tętniczego i pigmentacji skóry. Najbardziej pouczające kryteria morfologiczne choroby. Biopsje pobrane z jelita cienkiego ujawniają wewnątrzkomórkową i zewnątrzkomórkową akumulację tłuszczu w błonie śluzowej jelita cienkiego i węzłach chłonnych krezkowych; infiltracja własnej warstwy przez duże mikrofagi zawierające CHIC-dodatnie granulki beztłuszczowe oraz obecność prątków w błonie śluzowej. Leczenie. Leczenie przewlekłego zapalenia jelit powinno być kompleksowe i obejmować stosowanie środków wpływających na czynniki etiologiczne, mechanizmy patogenetyczne oraz lokalne i ogólne objawy choroby. Podstawą jest żywienie dietetyczne, które przyczynia się do obniżenia podwyższonego ciśnienia osmotycznego w jamie jelitowej, ogranicza wydzielanie oraz normalizuje pasaż treści jelitowej. Wykluczyć produkty zawierające grube włókno roślinne (surowe warzywa, owoce, chleb żytni, orzechy, ciasta, konserwy, przyprawy, dania pikantne, pełne mleko, piwo, kwas chlebowy, napoje gazowane i alkoholowe). Stosowanie soli kuchennej jest ograniczone. Potrzebne są posiłki ułamkowe, do 5-6 razy dziennie. W okresie remisji do diety wprowadza się niektóre warzywa i owoce, do 100-200 g dziennie. Przydziel sałatę, dojrzałe obrane pomidory, miękkie gruszki, słodkie jabłka, pomarańcze, mandarynki, maliny, truskawki, poziomki. Jedzenie powinno być gotowane lub gotowane na parze. Terapia lekowa powinna mieć charakter etiotropowy, patogenetyczny i objawowy. Leczenie etiotropowe: w przypadku dysbiozy stopnia II-IV przepisuje się leki przeciwbakteryjne: metronidazol (0,5 g 3 razy dziennie), klindamycynę (0,5 g 4 razy dziennie), cefaleksynę (0,5 g 2 razy dziennie) dzień), biseptol ( 0,48 g 2 razy dziennie), sulgina (1 g 3-4 razy dziennie), furazolidon (0,1 g 4 razy dziennie). Po zastosowaniu leków przeciwbakteryjnych przepisuje się eubiotyki - bifidumbakteryna lub bifikol 5 dawek 3 razy dziennie 30 minut przed posiłkiem, coli-bakteryna lub laktobakteryna 3 dawki 3 razy dziennie przed posiłkami, hilakforte 40 kropli 3 razy dziennie przed posiłkami. Leczenie preparatami bakteryjnymi prowadzi się przez długi czas: 3 kursy po 3 miesiące każdego roku. W przypadku dysbakteriozy gronkowcowej przepisywany jest bakteriofag antystafilokokowy (20 ml 3 razy dziennie przez 15-20 dni), w przypadku dysbakteriozy proteus - bakteriofag coliproteus doustnie, 20 ml 3 razy dziennie, przebieg leczenia wynosi 2-3 tygodnie. Jako środek przeciwbiegunkowy objawowy, imodium (loperamid) przepisuje się 1 kapsułkę 2-3 razy dziennie przed posiłkami przez 3-5 dni. W celu usprawnienia procesu trawienia zalecane są enzymy: pankreatyna, panzinorm forte, festal, trawienie, pankurmen, mezim forte, trienzym, których dawki dobierane są indywidualnie (od 1 tabletki 3 razy dziennie do 3-4 tabletek 4 razy dziennie ) i które są przepisywane bezpośrednio przed lub w trakcie posiłków przez 2-3 miesiące. W razie potrzeby enzymatyczną terapię zastępczą kontynuuje się przez dłuższy czas. Aby znormalizować ogólny stan pacjentów z zapaleniem jelit i wyeliminować zaburzenia metaboliczne, wskazana jest terapia substytucyjna. Aby zrekompensować niedobór witamin, witaminy B i B są przepisywane przez 4-5 tygodni.6 50 mg każdy, PP - 10-30 mg, C - 500 mg każdy. W stolcu tłuszczowym wskazane jest pozajelitowe podawanie witaminy B.2 (100-200 mcg) w połączeniu z witaminami rozpuszczalnymi w tłuszczach. Wewnątrz przepisuje się ryboflawina 0,02 g, kwas foliowy 0,003 g raz dziennie, witaminę E 3300 IU 2 razy dziennie. W przewlekłym zapaleniu jelit przebiegającym z ciężkim niedoborem białka, wraz z dietą, pozajelitowe podawanie osocza 150-200 ml hydrolizatów białkowych i mieszanin aminokwasów (aminopeptyd, alwezyna, poliamina, intrafuzyna, 250-500 ml dożylnie przez 20 dni) w połączenie z hormonami anabolicznymi (retabolil 2,0 ml 1 raz na 7-10 dni przez 3-4 tygodnie) i mieszaninami tłuszczowymi, np. intralipidem. Powołanie sterydów jest wskazane tylko przy znacznym niedoborze białka, hipoproteinemii, obecności niewydolności nadnerczy. Aby skorygować zaburzenia wodno-elektrolitowe, dożylne iniekcje pananginy 20-30 ml, glukonian wapnia 10% 10-20 ml w 200-400 ml roztworu izotonicznego lub roztworu glukozy, roztwory polijonowe „Disol”, „Trisol”, „Quartasol” są wskazane. Roztwory elektrolitów podaje się dożylnie przez 10-20 dni pod kontrolą stanu kwasowo-zasadowego i poziomu elektrolitów we krwi. Rokowanie i zapobieganie. Rokowania na całe życie i zdolność do pracy są w większości przypadków korzystne. Prognostycznie niekorzystnymi objawami są stale nawracający przebieg choroby, nagła znaczna utrata masy ciała, niedokrwistość, zespoły zaburzeń endokrynologicznych (obniżone libido, bolesne miesiączkowanie, niepłodność). Zapobieganie przewlekłemu zapaleniu jelit polega na szybkim leczeniu ostrych infekcji jelitowych i współistniejących chorób strefy żołądka i dwunastnicy, zgodnie z dietą, w profilaktycznym podawaniu preparatów bakteryjnych podczas prześwietlenia i radioterapii. WYKŁAD nr 13. Choroby przewodu pokarmowego. Choroby jelit. choroba Crohna Choroba Leśniowskiego-Crohna jest przewlekłą chorobą jelit z objawami ogólnoustrojowymi; którego podstawą morfologiczną jest ziarniniakowe autoimmunologiczne zapalenie przewodu pokarmowego. Etiologia i patogeneza. Etiologia i patogeneza choroby nie została dostatecznie poznana. Najpopularniejsze są zakaźne i immunologiczne koncepcje wystąpienia choroby. W ostatnich latach pojawiły się doniesienia na temat etiologicznej roli drobnoustrojów z rodzaju Yersinia. Trudno jednak określić, czy te drobnoustroje są patogenami, czy komensalami. Jednocześnie ważną rolę w patogenezie choroby odgrywają zmiany w mikroflorze jelitowej. Zazwyczaj zmniejszenie liczby bakterii typu bifidum z jednoczesnym wzrostem liczby enterobakterii z objawami patogenności. W rozwoju choroby rolę odgrywają mechanizmy autoimmunologiczne. W chorobie Leśniowskiego-Crohna pojawiają się autoprzeciwciała (IgC, IgM) przeciwko tkankom jelitowym. Podłożem morfologicznym choroby jest autoimmunologiczny proces zapalny, który początkowo występuje w warstwie podśluzówkowej, rozprzestrzenia się na całą grubość ściany jelita i charakteryzuje się obecnością nacieków ziarniniakowych, a następnie owrzodzeniem błony śluzowej, rozwojem ropni i przetoki gojące się z powstawaniem blizn i zwężeniem światła jelita. Wraz ze wzrostem czasu trwania choroby zwiększa się rozległość zmiany i pojawiają się objawy zaburzeń pozajelitowych. Klasyfikacja. Klasyfikacja (FI.I. Komarov, AI Kazanov, 1992). 1) Kurs: ostry; chroniczny. 2) Charakterystyka procesu: zmiana w jelicie cienkim; uszkodzenie w okolicy krętniczo-kątniczej; uszkodzenie w okrężnicy. 3) Powikłania: zwężenie jelita; toksyczne rozszerzenie okrężnicy; przetoki; amyloidoza; kamica nerkowa, kamica żółciowa; W12-niedokrwistość z niedoboru. Obraz kliniczny. Obraz kliniczny choroby Leśniowskiego-Crohna charakteryzuje się znaczną różnorodnością, o której decyduje lokalizacja i rozległość procesu patologicznego w jelicie, postać choroby oraz dodatek powikłań. Początek choroby może być ostry, gdy choroba postępuje od samego początku, i przewlekły, gdy choroba zaczyna się stopniowo. W pierwszym przypadku diagnozę często stawia się podczas laparotomii wykonywanej z powodu podejrzenia zapalenia wyrostka robaczkowego lub niedrożności jelit, która rozwinęła się bez wyraźnej przyczyny u młodych ludzi. Jednocześnie znajduje się przekrwiony obszar jelita cienkiego, powiększone węzły chłonne korzenia krezki, charakterystyczne dla choroby Leśniowskiego-Crohna. Pacjenci skarżą się na bóle brzucha bez określonej lokalizacji, rozluźnienie stolca bez widocznych patologicznych zanieczyszczeń, utratę masy ciała, niską temperaturę ciała. Obiektywne badanie zwraca uwagę na bladość skóry, która koreluje z nasileniem anemii, obrzękiem nóg z powodu upośledzenia wchłaniania i metabolizmu białek. Podczas badania dotykowego brzucha obserwuje się wzdęcia i dudnienie. Gdy proces zlokalizowany jest w jelicie grubym, występują na przemian zaparcia z biegunką, skurczowym bólem brzucha, płynnymi lub półuformowanymi stolcami zawierającymi domieszkę krwi. W przypadku zajęcia górnego odcinka przewodu pokarmowego pojawiają się objawy przypominające przewlekłe zapalenie przełyku, przewlekłe zapalenie żołądka i przewlekłe zapalenie dwunastnicy. Może wystąpić ból za mostkiem podczas przechodzenia pokarmu przez przełyk, nocny i „głodny” ból w nadbrzuszu, ból przy palpacji w strefie odźwiernikowo-dwunastniczej. W badaniu przedmiotowym pacjenta stwierdza się bladość skóry, stan podgorączkowy, niedobór masy ciała, pętle skurczowe jelit, ból w okolicy pępkowej, w prawym biodrowym odcinku. W chorobie Leśniowskiego-Crohna obserwuje się pozajelitowe objawy choroby: aftowe zapalenie jamy ustnej, ropowicę i przetoki jamy ustnej, zapalenie stawów, przypominające reumatoidalne zapalenie stawów w klinice, z charakterystycznymi objawami symetrycznych zmian drobnych stawów, sztywność rano. Typowe zmiany w oczach: zapalenie tęczówki, zapalenie tęczówki i ciała rzęskowego, makulopatia. Na skórze może pojawić się rumień guzowaty i ropne zapalenie zgorzelinowe. Biegunka charakteryzuje się wzrostem częstości stolca do 10 razy dziennie lub więcej, materii wielokałowej. Objętość stolca zależy od anatomicznej lokalizacji procesu: przy uszkodzeniu proksymalnego jelita cienkiego objętość kału jest znacznie większa niż przy uszkodzeniu części dystalnych. U wszystkich pacjentów obserwuje się utratę masy ciała. Diagnoza i diagnostyka różnicowa. Kliniczne badanie krwi podczas zaostrzenia ujawnia leukocytozę, niedokrwistość i wzrost ESR. Zmiany w ogólnej analizie moczu pojawiają się w ciężkich postaciach, charakteryzujących się dodatkiem amyloidozy nerek (białkomocz). Biochemiczne badanie krwi ujawnia hipoproteinemię, hipoalbuminemię, wzrost α-globulin, zmniejszenie zawartości żelaza, witaminy B12, kwas foliowy, cynk, magnez i potas. Dane z badania skatologicznego pozwalają pośrednio ocenić poziom zmiany. W koprogramie z lokalizacją procesu w jelicie cienkim stwierdza się materię wielokałową, stolce tłuszczowe, twórcę; w okrężnicy - domieszka śluzu, leukocytów, erytrocytów. Diagnostyka rentgenowska pozwala ustalić lokalizację i rozpowszechnienie procesu patologicznego w jelicie. Obszary zmienionego jelita przeplatają się z obszarami jelita niezmienionego. Zmienione pętle stają się sztywne, obraz jest mozaikowy z niewielkimi defektami wypełnienia oraz z przenikaniem kontrastu poza ścianę jelita w postaci kieszonek. Jelito w dotkniętym obszarze nabiera charakteru drobno frędzlowego, z utworzeniem pseudouchyłków. Zdolność skurczowa ściany jelita jest zmniejszona lub całkowicie utracona, ewakuacja baru spowalnia. Obserwuje się nierównomierne zwężenie światła jelita, w wyniku czego staje się ono tak wąskie, że przyjmuje formę koronki. Powyżej strefy zwężenia jelito rozszerza się. Diagnoza endoskopowa ma decydujące znaczenie w weryfikacji diagnozy. W przypadku choroby Leśniowskiego-Crohna najbardziej charakterystyczna jest zmiana w antrum żołądka i początkowej części dwunastnicy. Endoskopowo możliwe jest wykrycie kolistego zwężenia antrum, przypominającego zwężenie guza. Początkowy okres choroby Leśniowskiego-Crohna charakteryzuje się słabymi danymi endoskopowymi: matową błoną śluzową, na której widoczne są nadżerki typu aft, otoczone białawymi granulkami. Wzór naczyniowy jest nieobecny lub wygładzony. W świetle jelita i na jego ścianach określa się ropny śluz. W remisji klinicznej opisane zmiany mogą całkowicie zniknąć. W miarę postępu choroby błona śluzowa staje się nierównomiernie pogrubiona, ma białawy kolor i widoczne są duże powierzchowne lub głębokie owrzodzenia bruzd. Światło jelita zwęża się, co utrudnia prowadzenie kolonoskopu. Kolonoskopia umożliwia wykonanie celowanej biopsji błony śluzowej w dowolnej części okrężnicy oraz w końcowym odcinku jelita krętego. W chorobie Leśniowskiego-Crohna proces patologiczny zaczyna się w warstwie podśluzówkowej, dlatego biopsję należy wykonać w taki sposób, aby część warstwy podśluzówkowej dostała się do materiału biopsyjnego. W związku z powyższym w 54% przypadków nie wykryto morfologicznego podłoża choroby. Konieczne jest odróżnienie choroby Leśniowskiego-Crohna od nieswoistego wrzodziejącego zapalenia jelita grubego, gruźlicy przewodu pokarmowego, niedokrwiennego zapalenia jelita grubego, choroby Whipple'a, choroby uchyłkowej, rzekomobłoniastego zapalenia jelita grubego, limfogranulomatozy, pierwotnej skrobiawicy jelita cienkiego, przewlekłego zapalenia jelit. Wspólne dla wszystkich tych chorób jest zespół niestrawności jelitowej i niektóre zmiany ogólnoustrojowe. Jednak wrzodziejące zapalenie jelita grubego charakteryzuje się zmianą w dystalnych częściach okrężnicy z obowiązkowym udziałem w tym procesie odbytnicy i esicy. W nieswoistym wrzodziejącym zapaleniu jelita grubego nie ma segmentacji zmiany; rzadziej niż w chorobie Leśniowskiego-Crohna objawy ogólnoustrojowe są określane, a zespół złego wchłaniania jest mniej wyraźny. Jednak najdokładniejsze rozpoznanie choroby Leśniowskiego-Crohna potwierdza endoskopia z celowaną biopsją. Pokarmową postać gruźlicy odróżnia się od choroby Leśniowskiego-Crohna częstą lokalizacją w jelicie krętym, endoskopowymi ustaleniami pozwalającymi na wykrycie owrzodzeń o uniesionych, złuszczonych brzegach wypełnionych szarawą treścią. Takie wrzody goją się tworząc krótką bliznę, czego nie obserwuje się w chorobie Leśniowskiego-Crohna. U osób starszych istnieje potrzeba różnicowania choroby Leśniowskiego-Crohna i niedokrwiennego zapalenia jelita grubego. W przypadku tych ostatnich napady silnego bólu brzucha po jedzeniu są typowymi, wykrywalnymi irygoskopowo zmianami zapalenia okrężnicy w zagięciu śledzionowym, okrężnicy zstępującej i esicy. Najważniejszym objawem radiograficznym niedokrwiennego zapalenia jelita grubego jest objaw „odcisku kciuka”. Badanie endoskopowe i morfologiczne ujawnia typowe dla niedokrwiennego zapalenia jelita grubego komórki zawierające hemosyderynę oraz zwłóknienie w materiale biopsyjnym. Rozpoznanie limfogranulomatozy i pierwotnej amyloidozy jelitowej ustala się na podstawie badania histologicznego. W pierwszym przypadku komórki Bieriezowskiego-Sternberga znajdują się w biopsji z krezkowego węzła chłonnego, w drugim przypadku w błonie śluzowej odbytu znajdują się złogi amyloidu. Leczenie. Zaleca się dietę łagodną mechanicznie i chemicznie, o wysokiej zawartości białek, witamin, mikroelementów, z wyłączeniem mleka w przypadku jego nietolerancji i ograniczeniem grubego błonnika roślinnego. Wskazane jest stosowanie płynnych hydrolizatów dojelitowych. Salazopreparaty i kortykosteroidy stanowią podstawę farmakoterapii patogenetycznej. Dzienna dawka leków wynosi 3-6 g. Wraz z lokalizacją procesu patologicznego w jelicie grubym aktywność sulfasalazyny przewyższa aktywność prednizolonu. W przypadku braku efektu stosowania sulfasalazyny, ze zmianami głównie w jelicie cienkim i wyraźnymi objawami zapalenia immunologicznego, a także w obecności ogólnoustrojowych objawów choroby, wskazane jest stosowanie kortykosteroidów. Efekt ich stosowania odnotowuje się w ciągu pierwszych 8 tygodni od rozpoczęcia leczenia. Prednizolon jest przepisywany według następującego schematu: w szczycie zaostrzenia 60 mg na dobę, następnie dawkę stopniowo zmniejsza się i do 6-10 tygodnia dostosowuje się do dawki podtrzymującej 5-10 mg na dobę. Po osiągnięciu remisji klinicznej lek jest stopniowo anulowany. Jeśli remisja nie zostanie osiągnięta, leczenie prednizolonem jest kontynuowane w warunkach ambulatoryjnych do 52 tygodnia. W ciężkim przebiegu choroby, w przypadku powikłań pod postacią topiących się przetok odbytniczo-pochwowych, skórno-jelitowych, jelitowo-jelitowych, wskazane jest podawanie 6-merkaptopuryny doustnie w dawce 0,05 g 2-3 razy dziennie na 10-dniowe kursy z odstęp 3 dni do osiągnięcia remisji klinicznej . Następnie przestawiają się na przyjmowanie dawek podtrzymujących leku w ciągu roku. Dawka 6-merkaptopuryny w tym przypadku wynosi 75 mg na dobę. Efekt leczenia lekami immunosupresyjnymi można określić nie wcześniej niż po 3-4 miesiącach. Powszechne zastosowanie w leczeniu choroby Leśniowskiego-Crohna znalazł metronidazol, którego głównymi wskazaniami są przetoki i szczeliny okołoodbytnicze, brak działania salazopreparatów i glikokortykosteroidów, a także nawroty choroby po zabiegach protektomii. Lek jest przepisywany w dawce 500-1000 mg na dobę. Czas trwania kursu ciągłego nie powinien przekraczać 4 tygodni. Leczenie objawowe choroby Leśniowskiego-Crohna ogranicza się do wyznaczenia krótkich kursów (2-3 dni każdy) leków przeciwbiegunkowych (imodium, loperamid). Dawki dobierane są indywidualnie w zależności od efektu klinicznego. Nie przepisuj leków przeciwbiegunkowych przez długi czas (ponad 5 dni). W związku z występowaniem zespołu złego wchłaniania w chorobie Leśniowskiego-Crohna stosuje się preparaty enzymatyczne niezawierające kwasów żółciowych (pankreatyna, mesimforte, solizim, somilaza) w dawce od 2 do 6 tabletek do każdego posiłku. Zgodnie ze wskazaniami niedokrwistość i hipoalbuminemia są korygowane przez przepisywanie preparatów żelaza (pozajelitowo) i podawanie Alvezin, hydrolizerów białek, aminopeptydów, aminokrwi. Przypisz multiwitaminy w tabletkach, Essentiale w kapsułkach. Leczenie dysbakteriozy odbywa się zgodnie z ogólnymi zasadami. Rokowanie i zapobieganie. W przypadku choroby Leśniowskiego-Crohna rokowania na całe życie przy wczesnej diagnozie i skutecznych obserwacjach są korzystne, ale w przypadku pracy niepewne. U pacjentów z ciężką chorobą, w przypadku powikłań i objawów ogólnoustrojowych, ustala się I lub II grupę niepełnosprawności. Choroba Leśniowskiego-Crohna jest chorobą przednowotworową. Pacjenta należy szczegółowo zapoznać z cechami przebiegu choroby i ostrzec o możliwych powikłaniach, opisując ich objawy kliniczne w przystępnej formie. WYKŁAD nr 14. Choroby przewodu pokarmowego. Choroby okrężnicy. Nieswoiste wrzodziejące zapalenie jelita grubego Niespecyficzne wrzodziejące zapalenie jelita grubego jest chorobą zapalną, która atakuje błonę śluzową okrężnicy ze zmianami wrzodziejąco-destrukcyjnymi, która ma przewlekły, nawracający przebieg, któremu często towarzyszy rozwój powikłań zagrażających życiu. Etiologia i patogeneza. Nieswoiste wrzodziejące zapalenie jelita grubego jest chorobą idiopatyczną. Przyczyny jego wystąpienia nie są znane. Spośród wielu teorii wyjaśniających pochodzenie choroby (zakaźna, enzymatyczna, alergiczna, immunologiczna, neurogenna itp.) najbardziej interesująca jest teoria zakaźna, ale próby wyizolowania patogenu z treści okrężnicy zakończyły się niepowodzeniem. Proces patologiczny w przewlekłym wrzodziejącym zapaleniu jelita grubego rozpoczyna się w odbytnicy i rozprzestrzenia się w kierunku proksymalnym, obejmując leżące powyżej części okrężnicy. Zapalenie może być ograniczone do odbytnicy (zapalenie odbytnicy), odbytnicy i esicy (zapalenie odbytnicy), rozprzestrzenić się na cały lewy odcinek (zapalenie okrężnicy lewostronnej) lub obejmować całą okrężnicę (całkowite zapalenie okrężnicy). Pod względem funkcjonalnym długość okrężnicy w niespecyficznym zapaleniu okrężnicy jest skrócona o około 1/3. W badaniu materiału patologicznego stwierdzono rozlane zapalenie błony śluzowej okrężnicy (wyraźny obrzęk i nadmiar, pogrubienie fałdów). W błonie śluzowej powstają wrzody różnej wielkości, o nieregularnym kształcie, których dno znajduje się w błonie śluzowej, rzadziej w warstwie podśluzówkowej, w błonie mięśniowej i surowiczej. Morfologicznie w początkowym okresie określa się naciek w blaszce właściwej błony śluzowej, składający się z limfocytów z domieszką leukocytów wielojądrzastych, rozszerzeniem naczyń krwionośnych i obrzękiem śródbłonka tych naczyń. Naruszeniu mikrokrążenia towarzyszy rozwój niedotlenienia, który nasila naruszenia struktury i funkcji nabłonka błony śluzowej. Etapowi wyraźnych objawów klinicznych towarzyszy infiltracja leukocytów warstwy powierzchniowej nabłonka, rozwój zapalenia krypty, w którym w świetle krypt występuje nagromadzenie neutrofili. Dystalne części krypt ulegają zatarciu, pojawiają się ropnie krypt, w powstawaniu których ważną rolę odgrywa upośledzenie dojrzewania nabłonków. Wraz z martwicą nabłonka wyścielającego krypty otwierają się ropnie w kryptach, tworzą się wrzody. W okresie remisji błona śluzowa zostaje przywrócona, ale pozostaje jej zanik, deformacja krypt i nierównomierne pogrubienie blaszki właściwej. Klasyfikacja (Yu. V. Baltaitis i in., 1986). Charakterystyka kliniczna. 1. Forma kliniczna: 1) ostry; 2) przewlekłe. 2. Aktualne: 1) szybko postępujący; 2) ciągłe nawroty; 3) nawracające; 4) utajony. 3. Stopień aktywności: 1) zaostrzenie; 2) zaostrzenie zanikania; 3) umorzenie. 4. Dotkliwość: 1) światło; 2) umiarkowany; 3) ciężki. Charakterystyka anatomiczna. 1. Charakterystyka makroskopowa: 1) zapalenie odbytnicy: 2) zapalenie odbytnicy; 3) zmiana częściowa; 4) całkowita porażka. 2. Charakterystyka mikroskopowa: 1) przewaga procesów niszcząco-zapalnych; 2) redukcja procesów zapalnych z elementami naprawczymi; 3) konsekwencje procesu zapalnego Powikłania. 1. Lokalne: 1) krwawienie z jelit; 2) perforacja okrężnicy; 3) zwężenie okrężnicy; 4) pseudopolipowatość; 5) wtórne zakażenie jelitowe; 6) zanik błony śluzowej; 7) toksyczne rozszerzenie okrężnicy; 8) nowotwór złośliwy. 2. Ogólne: 1) czynnościowa hipokortyka; 2) sepsa; 3) objawy ogólnoustrojowe - zapalenie stawów, zapalenie stawów krzyżowo-biodrowych, zmiany skórne, zapalenie tęczówki, amyloidoza, zapalenie żył, stwardniające zapalenie dróg żółciowych, dystrofia wątroby. Obraz kliniczny. Obraz kliniczny wrzodziejącego zapalenia jelita grubego jest polimorficzny i zależy od ciężkości przebiegu i ciężkości procesu. Przebieg procesu zapalnego, często uważany za przewlekły, w niektórych przypadkach staje się ostry. Stopień uszkodzenia jelita grubego może się również różnić. Niespecyficzne wrzodziejące zapalenie jelita grubego charakteryzuje się 3 głównymi objawami: wypływem szkarłatnej krwi podczas wypróżnień, dysfunkcją jelit i bólem brzucha. Izolacja krwi (od smug na powierzchni kału do 300 ml lub więcej) podczas defekacji jest pierwszą oznaką choroby. W ostrej postaci choroby krew jest wydzielana przez strumień, co prowadzi do obniżenia ciśnienia krwi, aż do rozwoju zapaści i wstrząsu krwotocznego. Dysfunkcja jelit objawia się dolegliwościami powtarzających się niestabilnych stolców, co jest wynikiem rozległego uszkodzenia błony śluzowej oraz zmniejszenia wchłaniania wody i soli. Najczęściej biegunka występuje z ciężkim wrzodziejącym zapaleniem jelita grubego. Jednak biegunka nie jest wiarygodnym wskaźnikiem nasilenia procesu. Znaczenie ma nasilenie biegunki w połączeniu z obecnością czerwonej krwi w stolcu. U znacznej liczby pacjentów z wrzodziejącym zapaleniem jelita grubego na powierzchni powstałego kału okresowo znajdują się krew i śluz, co często błędnie uważa się za przejaw hemoroidów. Pacjenci skarżą się na ból w podbrzuszu o charakterze skurczowym lub stałym, który częściej zlokalizowany jest w podbrzuszu lub lewym biodrze, nasila się przed aktem defekacji i zanika po nim. Często odnotowuje się tenesmus. Kiedy w proces zaangażowane są warstwy podśluzówkowe, mięśniowe i surowicze jelita, ból wzrasta; palpacja brzucha pojawia się obrona mięśni przedniej ściany brzucha. Łagodny przebieg nieswoistego wrzodziejącego zapalenia jelita grubego charakteryzuje się zadowalającym stanem pacjentów. Ból brzucha jest umiarkowany i krótkotrwały. Krzesło jest dekorowane, przyspieszone, do 2-3 razy dziennie. W kale znajdują się krew i śluz. Proces zlokalizowany jest w odbytnicy i esicy. Przebieg kliniczny jest nawracający. Efekt leczenia salazopreparatami jest zadowalający. Nawroty występują nie więcej niż 2 razy w roku. Remisje mogą trwać długo (ponad 2-3 lata). Umiarkowany przebieg choroby rozpoznaje się, gdy pacjent ma biegunkę. Fotel jest częsty (do 6-8 razy dziennie), w każdej porcji widoczna domieszka krwi i śluzu. Bóle skurczowe brzucha są bardziej intensywne. Występuje przerywana gorączka ze wzrostem temperatury ciała do 38 ° C, intensywne ogólne osłabienie. Mogą również wystąpić pozajelitowe objawy choroby (zapalenie stawów, zapalenie błony naczyniowej oka, rumień guzowaty). Kurs jest stale nawracający, efekt salazopreparatów jest niestabilny, podczas zaostrzeń przepisywane są hormony. Ciężka postać choroby charakteryzuje się ostrym początkiem. Całkowite uszkodzenie jelita grubego szybko rozwija się wraz z rozprzestrzenianiem się procesu patologicznego w głąb ściany jelita. Stan pacjenta gwałtownie się pogarsza. Klinika charakteryzuje się nagłym początkiem, wysoką gorączką, obfitymi biegunkami do 24 razy na dobę, obfitymi krwawieniami jelitowymi oraz szybkim wzrostem odwodnienia. Pojawia się tachykardia, obniża się ciśnienie krwi, wzrastają pozajelitowe objawy niespecyficznego wrzodziejącego zapalenia jelita grubego. Leczenie zachowawcze nie zawsze jest skuteczne i często konieczna jest pilna operacja. Diagnoza i diagnostyka różnicowa. W klinicznych badaniach krwi w łagodnych postaciach choroby, niewielka leukocytoza neutrofilowa, wzrost ESR i liczba czerwonych krwinek nie ulegają zmianie. Wraz ze wzrostem nasilenia przebiegu i wydłużaniem się czasu trwania zaostrzenia pojawia się niedokrwistość pochodzenia mieszanego (B12-niedobór i niedobór żelaza), zwiększony ESR. W analizie biochemicznej krwi w postaciach umiarkowanych i ciężkich obserwuje się dysproteinemię, hipoalbuminemię, hipergammaglobulinemię, zaburzenia równowagi elektrolitowej i stan kwasowo-zasadowy. W ogólnej analizie moczu zmiany pojawiają się tylko wtedy, gdy powikłania pojawiają się w postaci zespołu nerczycowego na tle amyloidozy, gdy obserwuje się charakterystyczne zmiany w badaniach moczu - białkomocz, "martwy" osad moczu, występuje również wzrost krwi oraz poziom kreatyniny, mocznika. Główną rolę w diagnostyce odgrywa badanie endoskopowe z celowaną biopsją, ponieważ w nieswoistym wrzodziejącym zapaleniu jelita grubego głównie dotyczy to błony śluzowej jelita grubego. Odbytnica jest zawsze zaangażowana w proces patologiczny, tj. zmiany erozyjne i wrzodziejące są wykrywane podczas endoskopii bezpośrednio za zwieraczem odbytu podczas sigmoidoskopii. We wrzodziejącym zapaleniu jelita grubego nie zawsze jest możliwe pokonanie zgięcia odbytniczo-sigmoidalnego z powodu silnego skurczu. Próbie trzymania rurki proktoskopu towarzyszy silny ból. W tej sytuacji proktoskop należy wprowadzić na głębokość nie większą niż 12-15 cm. Kolonoskopia podczas ciężkiego zaostrzenia nieswoistego wrzodziejącego zapalenia jelita grubego nie jest bezpieczna do wykonania. Powinien być stosowany przy wysokim ryzyku nowotworu złośliwego. Należy zauważyć wysoką zawartość informacyjną sigmoidoskopii. Obraz endoskopowy zależy od postaci choroby. Przy łagodnej postaci widoczne są obrzęknięte, matowe błony śluzowe, gęste białawe naloty śluzu na ściankach jelita, lekkie krwawienie kontaktowe. Wzór naczyniowy warstwy podśluzówkowej nie jest określany wizualnie. W umiarkowanym przebiegu choroby ujawniają się przekrwienie i obrzęk błony śluzowej, silne krwawienia kontaktowe, krwotoki, nadżerki i owrzodzenia o nieregularnym kształcie, grube naloty śluzu na ściankach jelita. W ciężkim przebiegu choroby błona śluzowa okrężnicy ulega znacznemu zniszczeniu. Stwierdzono ziarnistą, krwawiącą powierzchnię wewnętrzną, rozległe obszary owrzodzenia ze złogami włóknikowatymi, pseudopolipy o różnych rozmiarach i kształtach, ropę i krew w świetle jelita. Przeciwwskazaniami do kolonoskopii i sigmoidoskopii są ciężkie postacie wrzodziejącego zapalenia jelita grubego w ostrym stadium choroby. Badanie rentgenowskie pozwala określić rozległość zmiany; wyjaśnić diagnozę w przypadku niewystarczająco przekonujących danych endoskopowych; diagnostyka różnicowa z chorobą Leśniowskiego-Crohna, chorobą uchyłkową, niedokrwiennym zapaleniem jelita grubego; w odpowiednim czasie wykryć oznaki złośliwości. Zwykłe zdjęcia rentgenowskie mogą ujawnić skrócenie jelita, brak haustacji, toksyczne rozszerzenie, wolny gaz pod kopułą przepony podczas perforacji. Irygoskopię należy wykonywać bardzo ostrożnie. Może wywołać pogorszenie stanu pacjenta. W niektórych przypadkach przygotowanie pacjenta do lewatywy z baru z lewatywami i środkami przeczyszczającymi należy zastąpić specjalną dietą przepisaną 2 dni przed badaniem. W niektórych przypadkach zastosowanie wlewu kontrastowego może przyspieszyć perforację lub spowodować toksyczne rozszerzenie okrężnicy. Dlatego irygoskopię wykonuje się po ustąpieniu ostrych zjawisk. Metoda ta ujawnia nierówności i „ziarnistość” błony śluzowej, pogrubienie ściany jelita, owrzodzenia, pseudopolipowatość, brak haustacji. Diagnostykę różnicową niespecyficznego wrzodziejącego zapalenia jelita grubego przeprowadza się przede wszystkim w przypadku ostrych infekcji jelitowych. W przypadku epidemii infekcji jelitowych diagnozę można łatwo ustalić. Ale nawet w przypadku sporadycznej zachorowalności w ostrych infekcjach jelitowych zespół zapalenia jelita grubego przebiega bez nawrotów, podczas gdy wrzodziejące zapalenie jelita grubego ma nawracający przebieg. Najdokładniejsze metody identyfikacji ostrej infekcji jelitowej obejmują bakteriologiczne i serologiczne. Często wrzodziejące zapalenie jelita grubego różni się od choroby Leśniowskiego-Crohna. W typowych przypadkach choroba Leśniowskiego-Crohna różni się od niespecyficznego zapalenia jelita grubego brakiem uszkodzenia odbytnicy, częstym zaangażowaniem jelita krętego w proces patologiczny i odcinkowym uszkodzeniem ściany jelita. Ostateczną diagnozę można postawić, wykrywając w próbkach biopsyjnych ziarniniaki limfoidalne specyficzne dla choroby Leśniowskiego-Crohna. W przypadku ziarniniakowego zapalenia jelita grubego częściej wykrywa się zapalenie przyodbytnicy i przetoki przyodbytnicze niż w przypadku niespecyficznego wrzodziejącego zapalenia jelita grubego. W niektórych przypadkach konieczne staje się rozróżnienie między wrzodziejącym zapaleniem jelita grubego a gruźlicą jelit. W przypadku gruźlicy jelit charakterystyczna jest pewna lokalizacja procesu (jelito kręte, okolica krętniczo-kątnicza), segmentowe uszkodzenie jelit. Ale czasami w przypadku gruźlicy jelit dotyczy to odbytnicy i całego jelita grubego. Obraz kolonoskopowy gruźlicy jelit charakteryzuje się obecnością owrzodzeń o uniesionych krawędziach wypełnionych szarawą treścią. Wrzody gruźlicze mają tendencję do rozprzestrzeniania się w kierunku poprzecznym i pozostawiania krótkich blizn, w których owrzodzenia pojawiają się ponownie. W przypadku nieswoistego wrzodziejącego zapalenia jelita grubego blizny nie tworzą się w miejscu dawnych owrzodzeń. U pacjentów w podeszłym wieku i w podeszłym wieku wrzodziejące zapalenie jelita grubego należy odróżnić od niedokrwiennego zapalenia jelita grubego. Ten ostatni charakteryzuje się intensywnym, napadowym bólem brzucha w 20-30 minut po jedzeniu, natomiast we wrzodziejącym zapaleniu jelita grubego ból występuje przed wypróżnieniem. Najważniejszym objawem radiologicznym jest objaw „odcisku kciuka”. Obraz endoskopowy niedokrwiennego zapalenia jelita grubego charakteryzuje się ostro określonymi granicami zmiany, krwotokami podśluzówkowymi, sinicowymi pseudopolipowatymi formami wystającymi do światła jelita. Badanie histologiczne ujawnia komórki zawierające hemosyderynę i zwłóknienie. Brak krwawienia kontaktowego w czasie biopsji również bardziej wskazuje na niedokrwienne zapalenie jelita grubego. Leczenie. Brak jednego czynnika etiologicznego oraz złożoność patogenezy nieswoistego wrzodziejącego zapalenia jelita grubego utrudniają leczenie tej choroby. Stosuje się leki o działaniu przeciwzapalnym i przeciwbakteryjnym: salazopirydazyna, sulfasalazyna, salazodimetoksyna, salofalk. Sulfasalazyna przyjmowana doustnie przy udziale mikroflory jelitowej rozkłada się na kwas 5-aminosalicylowy i sulfapirydynę. Niewchłonięta sulfapirydyna hamuje rozwój mikroflory beztlenowej w jelicie, w tym Clostridia i bakteriody. A dzięki kwasowi 5-aminosalicylowemu lek nie tylko powoduje zmiany w mikroflorze jelitowej, ale także moduluje reakcje immunologiczne i blokuje mediatory procesu zapalnego. Lek jest przepisywany w dawce 2-6 g na dzień przez cały okres aktywnego stanu zapalnego. Po ustąpieniu zespołu jelita grubego dawkę sulfasalazyny zmniejsza się stopniowo, doprowadzając ją do utrzymania (średnio 1-1,5 tabletki dziennie). Powołanie pochodnych kwasu 5-aminosalicylowego (salofalk, mesacol, salosan, tidikol) jest podstawową metodą i może być stosowane jako monoterapia w łagodnych i umiarkowanych postaciach wrzodziejącego zapalenia jelita grubego. Zabieg przeprowadza się na tle terapii dietetycznej z wyjątkiem produktów mlecznych, w obecności zrównoważonej zawartości białek, tłuszczów, węglowodanów i witamin w diecie. Wskazane jest wykluczenie świeżych owoców, warzyw, konserw. Żywność powinna być delikatna mechanicznie i chemicznie. Karm ułamkowe 4-5 razy dziennie. Brak równowagi witaminowej zakłóca proces wchłaniania mikroelementów i jest kompensowany przez wyznaczenie złożonych preparatów w tabletkach ("Duovit", "Oligovit", "Unicap"). W ciężkim zespole biegunkowym u osób z łagodną lub umiarkowaną chorobą wskazane jest wyznaczenie sandostatyny, która hamuje syntezę hormonów żołądkowo-jelitowych i amin biogennych (wazoaktywny peptyd jelitowy, gastryna, serotonina), których wytwarzanie jest znacznie zwiększone w wrzodziejącym zapaleniu jelita grubego i Choroba Crohna. A także lek zmniejsza wydzielanie i poprawia wchłanianie w jelicie, hamuje trzewny przepływ krwi i zmniejsza ruchliwość. Przy stosowaniu sandostatyny (w ciągu 7 dni w dawce 0,1 mg 2 razy, podskórnie) zmniejsza się biegunka, praktycznie zanika parcie i zmniejsza się wydalanie krwi z kałem. W ciężkiej postaci niespecyficznego wrzodziejącego zapalenia jelita grubego leczenie prowadzi się na tle żywienia pozajelitowego. Zawartość białka w tych preparatach powinna wynosić około 1,5-2,0 g/kg masy ciała. Kortykosteroidy, które są podawane pozajelitowo, są patogenetycznym leczeniem ciężkiej postaci choroby: w pierwszym dniu prednizon podaje się dożylnie w odstępach 12 godzin (90-120 mg lub więcej), w ciągu następnych 5 dni - domięśniowo, stopniowo zmniejszając dawkę. Z pozytywnym efektem przechodzą na leki doustne (prednizolon 40 mg dziennie). Długotrwałe podawanie hormonów w okresie stabilnej remisji jest niepraktyczne. U pacjentów z ciężkim przebiegiem choroby odnotowano pozytywny efekt hiperbarii tlenowej (HBO). Zastosowanie kursu HBO (7-10 zabiegów) w okresie remisji może zmniejszyć częstotliwość nawrotów. Wskazania do pilnego leczenia chirurgicznego: perforacja jelit, toksyczne rozszerzenie, obfite krwawienie jelitowe, nowotwór złośliwy. W umiarkowanej postaci przebiegu niespecyficznego wrzodu wrzodowego wymagana jest ścisła dieta z ograniczeniem błonnika, produktów mlecznych i wysokiej zawartości białka. Prednizolon jest przepisywany doustnie w początkowej dawce 20-40 mg na dobę. Leczenie można uzupełnić sulfasalazyną i jej analogami, które przyjmuje się doustnie lub podaje do odbytnicy w mikroklisterach i czopkach. Początkowa dawka sulfasalazyny wynosi 1 g dziennie, następnie zwiększa się ją do 4-6 g. Jako pomocniczą metodę leczenia można stosować wywary z ziół o działaniu przeciwzapalnym i hemostatycznym (korzeń czarniaka, liść pokrzywy, porosty, szyszki olchy szarej, korzeń lukrecji), ziołolecznictwo często pozwala zmniejszyć dawkę salazopreparatów, przedłużyć umorzenie. Rokowanie i zapobieganie. W ciężkich przypadkach i przy obecności powikłań ogólnoustrojowych i miejscowych rokowanie jest poważne. Pacjenci są całkowicie niezdolni do pracy. W łagodnych i umiarkowanych postaciach choroby rokowanie na całe życie jest korzystne. Pacjentów należy przenieść do lekkiej pracy. W okresie remisji zaleca się leczenie podtrzymujące salazopreparatami, środkami bakteryjnymi, psychoterapię i dietoterapię. Pacjenci cierpiący na nieswoiste wrzodziejące zapalenie jelita grubego od dłuższego czasu (powyżej 5-7 lat) powinni być przypisani do grupy ryzyka wystąpienia raka jelita i umieszczani w dokumentacji przychodni. Pacjenci ci są pokazywani raz w roku kolonoskopią z celowaną biopsją. WYKŁAD nr 15. Choroby nerek. Ostre kłębuszkowe zapalenie nerek Ostre kłębuszkowe zapalenie nerek (AGN) to ostra rozlana choroba nerek o charakterze zakaźno-alergicznym, zlokalizowana w kłębuszkach nerkowych. AGN może być chorobą niezależną (pierwotną) lub wtórną jako część innej choroby, komplikując obraz kliniczny i diagnozę tej ostatniej. AGN zwykle dotyka mężczyzn młodych i w średnim wieku. Etiologia. AGN występuje najczęściej po zakażeniu kokosem (grypa, ostre zapalenie migdałków, zapalenie gardła wywołane przez tzw. nefrytogenne szczepy mikroorganizmów). U 60-80% pacjentów wykryto paciorkowce β-hemolizujące grupy A, w 1/3 przypadków nie można ustalić etiologii AGN. Długotrwała hipotermia, szczególnie w warunkach wysokiej wilgotności, przyczynia się do rozwoju AGN. Szczepienie jest również czynnikiem początku choroby, aw 75% przypadków nerki są zaatakowane po drugim lub trzecim wstrzyknięciu. Patogeneza. Patogeneza choroby ma mechanizm immunologiczny: kiedy antygeny (paciorkowcowe, lecznicze, obce białka) dostają się do organizmu, w odpowiedzi powstają przeciwciała, które wiążą te antygeny i wraz z trzecią frakcją dopełniacza tworzą kompleksy immunologiczne krążące w naczyniach łóżko. Kompleksy mają zdolność odkładania się na zewnętrznej stronie błony podstawnej naczyń włosowatych kłębuszków, powodując ich uszkodzenie poprzez uwolnienie produktów rozpadu dopełniacza, które zwiększają przepuszczalność naczyń włosowatych i powodują w nich miejscowe zmiany. Neutrofile pędzą do miejsc odkładania się kompleksów immunologicznych, których enzymy lizosomalne pogłębiają uszkodzenia śródbłonka i błony podstawnej, oddzielając je od siebie. Degranulacja płytek krwi powoduje uwolnienie serotoniny, co prowadzi do hemokoagulacji i odkładania się fibryny na błonie podstawnej. Eliminację kompleksów immunologicznych z organizmu ułatwia reakcja makrofagów w postaci proliferacji komórek mezangialnych i śródbłonka, przy skuteczności tego procesu następuje powrót do zdrowia. Obraz kliniczny. Obraz kliniczny choroby składa się z następujących zespołów. zespół moczowy. 1. Proteinuria ze względu na przechodzenie cząsteczek białka przez przestrzenie ściany naczyń włosowatych kłębuszków nerkowych, powstałe podczas osadzania się na nich kompleksów immunologicznych. Proteinuria ma charakter selektywny, w którym przez „filtr kłębuszkowy” przechodzą głównie albuminy. 2. Krwiomocz z powodu zaangażowania w patologiczny proces mezangium włośniczkowego i tkanki śródmiąższowej. Erytrocyty przenikają przez najmniejsze szczeliny w błonie podstawnej, zmieniając swój kształt. 3. Cylindruria - wydalanie z moczem cylindrycznych komórek kanalików. Podczas procesów dystroficznych w kanalikach rozpadających się komórek nabłonka nerek powstają ziarniste cylindry składające się z gęstej ziarnistej masy; woskowe cylindry mają ostre kontury i jednorodną strukturę; szkliste odlewy to formacje białkowe. Zespół nadciśnieniowy obserwuje się z powodu: 1) retencja sodu i wody; 2) aktywacja układu renina-angiotensyna-aldosteron i współczulno-nadnerczowa; 3) zmniejszenie funkcji układu depresyjnego nerek. Zespół obrzęku wiąże się z następującymi czynnikami: 1) spadek filtracji kłębuszkowej z powodu ich porażki; 2) zmniejszenie ładunku filtracyjnego sodu i wzrost jego reabsorpcji; 3) retencja wody spowodowana zatrzymaniem sodu w organizmie; 4) wzrost BCC; 5) wtórny hiperaldosteronizm; 6) wzrost wydzielania ADH i wzrost wrażliwości na nie dystalnego nefronu, co prowadzi do zatrzymania płynów; 7) wzrost przepuszczalności ścian naczyń włosowatych i uwalnianie osocza do tkanek; 8) spadek ciśnienia onkotycznego osocza z masywnym białkomoczem. Skargi przedstawione w AGN nie są specyficzne i występują w różnych schorzeniach. Bardzo ważne jest, aby w wywiadzie wskazać niedawny ból gardła, zaostrzenie przewlekłego zapalenia migdałków, hipotermię itp. Niektórzy pacjenci odnotowują rano zmniejszenie ilości wydalanego moczu połączone z obrzękiem (ciastami) twarzy. U 1/3-3/4 pacjentów w pierwszych dniach choroby występują niezbyt silne bóle w okolicy lędźwiowej związane ze zwiększeniem wielkości nerek. Występują również zwiększone zmęczenie, ból głowy, duszność podczas wysiłku fizycznego, krótkotrwały wzrost temperatury ciała do stanu podgorączkowego. Nadciśnienie tętnicze, wykryte tylko u połowy pacjentów, charakteryzuje się wzrostem liczebności do 140-160/85-90 mm Hg. Sztuka. (rzadko - do 180/100 mm Hg. Art.). diagnostyka. W 100% przypadków w badaniu moczu stwierdza się białkomocz o różnym nasileniu, cylindrurię oraz, co najważniejsze dla rozpoznania, krwiomocz o różnym nasileniu – od mikrohematurii (do 10 czerwonych krwinek w polu widzenia) po makrohematurię (choć dość rzadką). ). Jeśli jednak podejrzewa się AGN, konieczne jest wykonanie serii powtarzanych badań moczu lub wykonanie testu Nechiporenko (określenie liczby powstałych pierwiastków w 1 μl), ponieważ w pojedynczej porcji moczu mogą nie zostać wykryte czerwone krwinki. Podczas badania krwi wykrywane są wskaźniki ostrej fazy (wzrost zawartości fibrynogenu i α2-globulina, białko C-reaktywne, przyspieszenie ESR), liczba leukocytów zmienia się nieznacznie, umiarkowana niedokrwistość. Przy nieskomplikowanym przebiegu AGN zawartość substancji azotowych (kreatyniny, indican, mocznika) we krwi nie zmienia się. W początkowej fazie choroby obserwuje się zmianę w teście Reberga - spadek filtracji kłębuszkowej i wzrost reabsorpcji kanalikowej, która normalizuje się wraz z powrotem do zdrowia. Badanie rentgenowskie u pacjentów z ciężkim nadciśnieniem tętniczym może wykazać umiarkowany wzrost lewej komory, która przybiera takie same rozmiary, jak pacjent wraca do zdrowia. Istnieją 3 kliniczne warianty AGN. 1) Wariant monosymptomatyczny: drobne dolegliwości, brak obrzęku i nadciśnienia tętniczego, występuje tylko zespół moczowy; najczęstszy wariant przebiegu choroby (86% przypadków). 2) Wariant nerczycowy: wyraźny obrzęk, skąpomocz, możliwe jest zwiększenie ciśnienia krwi do stosunkowo niskich wartości, wykrywa się go u 8% pacjentów. 3) Wersja rozszerzona: nadciśnienie tętnicze, osiągające wysokie wartości (180/100 mm Hg), umiarkowanie nasilony obrzęk, niewydolność krążenia występuje w 6% przypadków. Diagnostyka różnicowa. AGN należy odróżnić od przewlekłego kłębuszkowego zapalenia nerek, co nie jest trudne przy ostrym początku AGN i późniejszym całkowitym ustąpieniu objawów. Jednak w przypadku braku ostrego początku, a także długotrwałego utrzymywania się pewnych objawów choroby, diagnoza staje się znacznie bardziej skomplikowana. Jeśli różnicowanie jest trudne, stosuje się biopsję nerki. Trudno odróżnić AGN od odmiedniczkowego zapalenia nerek ze względu na obecność leukocyturii w obu chorobach. Jednak AGN towarzyszy bardziej masywna białkomocz, aw niektórych przypadkach obrzęk. W diagnostyce różnicowej pomagają również objawy kliniczne odmiedniczkowego zapalenia nerek w postaci silniejszego bólu w dolnej części pleców, któremu towarzyszy gorączka i zaburzenia dyzuryczne. Wartość diagnostyczną ma również definicja bakteriomoczu w odmiedniczkowym zapaleniu nerek, identyfikacja „aktywnych” leukocytów, a także badania rentgenowskie (deformacja miseczek) i izotopowo-renograficzne (asymetria czynności nerek). AGN jako niezależną chorobę należy odróżnić od przewlekłych rozlanych chorób tkanki łącznej, w których AGN jest jednym z objawów choroby. Taka sytuacja występuje zwykle przy nasileniu zespołów moczowych, nadciśnieniowych i obrzękowych oraz niedostatecznej jasności innych objawów choroby, częściej z SLE (toczeń rumieniowaty układowy). Prawidłową diagnozę w SLE można postawić biorąc pod uwagę zespół stawowy, uszkodzenie skóry i innych narządów (serca), wyraźne zmiany immunologiczne (wykrycie przeciwciał przeciwnarządowych w wysokim mianie, komórki tocznia rumieniowatego, przeciwciała przeciwko DNA i RNA ), a także monitorowanie dynamiki obrazu klinicznego. Leczenie. Leczenie AGN jest złożone i obejmuje następujące środki. 1. Tryb. W przypadku podejrzenia AGN lub natychmiast po ustaleniu diagnozy pacjent powinien być natychmiast hospitalizowany. Ścisły leżenie w łóżku należy obserwować przez około 2-4 tygodnie, aż do ustąpienia obrzęku i normalizacji ciśnienia krwi. Przebywanie w łóżku zapewnia równomierne rozgrzanie organizmu, co prowadzi do zmniejszenia skurczu naczyń (a tym samym do obniżenia ciśnienia krwi) oraz do wzrostu filtracji kłębuszkowej i diurezy. Po wypisaniu ze szpitala wskazane jest leczenie domowe przez okres do 4 miesięcy od dnia wystąpienia choroby, co stanowi najlepszą prewencję przejścia AGN do stadium przewlekłego. 2. Dieta. W zależności od nasilenia objawów klinicznych bardzo ważne jest ograniczenie płynów i chlorku sodu. Przy postaci rozszerzonej i nerczycowej zaleca się całkowity post przez 1-2 dni z przyjmowaniem płynów w ilości równej diurezie. W 2-3 dniu pokazano spożycie żywności bogatej w sole potasu (owsianka ryżowa, ziemniaki). Całkowita ilość wypijanej wody dziennie powinna być równa objętości moczu przeznaczonej na dzień poprzedni plus 300-500 ml. Po 3-4 dniach pacjent przechodzi na dietę z ograniczeniem białka (do 60 g dziennie), a całkowita ilość soli nie przekracza 3-5 g / dzień. Taka dieta jest zalecana do ustąpienia wszelkich objawów pozanerkowych i gwałtownej poprawy osadu moczowego. 3. Farmakoterapia obejmuje przede wszystkim terapię przeciwbakteryjną, która jednak powinna być prowadzona tylko wtedy, gdy zakaźny charakter AGN jest wiarygodnie ustalony (patogen został wyizolowany i minęły nie więcej niż 3 tygodnie od początku choroba). Zwykle przepisywana penicylina lub jej półsyntetyczne analogi w konwencjonalnych dawkach. Obecność wyraźnych ognisk przewlekłej infekcji (zapalenie migdałków, zapalenie zatok itp.) jest również bezpośrednim wskazaniem do antybiotykoterapii. Diuretyki w leczeniu AGN są wskazane tylko przy zatrzymaniu płynów, podwyższonym ciśnieniu krwi i pojawieniu się niewydolności serca. Najskuteczniejszy furosemid (40-80 mg), stosowany do czasu eliminacji obrzęków i nadciśnienia. Nie ma potrzeby długoterminowego przepisywania tych leków, wystarczą 3-4 dawki. W przypadku braku obrzęku, ale utrzymującego się nadciśnienia lub niedostatecznego działania przeciwnadciśnieniowego saluretyków, leki przeciwnadciśnieniowe (klofelina, dopegyt) są przepisywane z czasem podawania zależnym od utrzymywania się nadciśnienia tętniczego. W nerczycowej postaci AGN zalecana jest terapia immunosupresyjna (kortykosteroidy - prednizolon 60-120 mg na dobę, a następnie stopniowe zmniejszanie dawki, czas stosowania przez 4-8 tygodni). W przypadku AGN z silnym obrzękiem i znacznym spadkiem diurezy heparynę podaje się w dawce 20 000-30 000 IU dziennie przez 4-6 tygodni, osiągając 2-3-krotny wzrost czasu krzepnięcia krwi. W przypadku długotrwałego białkomoczu indometacynę lub woltaren przepisuje się w dawce 75-150 mg na dobę (przy braku nadciśnienia i skąpomoczu). Rokowanie jest korzystne, jednak przy długotrwałych formach istnieje możliwość, że proces stanie się przewlekły. Zapobieganie AGN sprowadza się do skutecznego leczenia infekcji ogniskowej, racjonalnego stwardnienia. Aby w porę wykryć początek choroby po szczepieniu, przeniesiony SARS u wszystkich pacjentów, konieczne jest zbadanie moczu. WYKŁAD nr 16. Choroby nerek. Odmiedniczkowe zapalenie nerek Odmiedniczkowe zapalenie nerek jest chorobą zakaźną, w której w proces zaangażowana jest miedniczka nerkowa, jej kielichy i substancja nerkowa, z dominującą zmianą tkanki śródmiąższowej. Pod tym względem odmiedniczkowe zapalenie nerek jest śródmiąższowym (śródmiąższowym) zapaleniem nerek. Jest to pojęcie szersze niż odmiedniczkowe zapalenie nerek. Oznacza, po pierwsze, rodzaj zapalenia nerek o dowolnej etiologii z przewagą tkanki śródmiąższowej, a po drugie, szczególną chorobę, w której to zapalenie jest jedynym i głównym wyrazem. W pobliżu śródmiąższowego zapalenia nerek znajduje się tak zwane cewkowo-śródmiąższowe zapalenie nerek, w którym występuje przyjazne uszkodzenie kanalików i zrębu nerek. Klasyfikacja. Na podstawie danych klinicznych i morfologicznych wyróżnia się ostre i przewlekłe odmiedniczkowe zapalenie nerek, które zwykle ma przebieg nawracający w postaci napadów ostrego odmiedniczkowego zapalenia nerek. Również odmiedniczkowe zapalenie nerek może być jedno- i dwustronne. Zgodnie z formą kursu (dla przewlekłego odmiedniczkowego zapalenia nerek): postać nawracająca, utajone przewlekłe odmiedniczkowe zapalenie nerek, odmiedniczkowa pomarszczona nerka. Etiologia i patogeneza. Odmiedniczkowe zapalenie nerek jest chorobą zakaźną. Jego czynnikami sprawczymi są czynniki zakaźne o niespecyficznym charakterze: E. coli, enterokoki, gronkowce i inne bakterie, ale w większości przypadków mówimy o E. coli (40%) i florze mieszanej (38%). Zwraca się uwagę na formy L bakterii, protoplasty (ciała bakterii pozbawione błon podtrzymujących infekcję), candida, które mogą powodować przewlekłe odmiedniczkowe zapalenie nerek. Źródłem infekcji mogą być migdałki, choroby narządów płciowych i jelita grubego, tzn. czynniki zakaźne mogą przenikać do nerek, w tym do miednicy, wraz z krwią (krwiopochodne zstępujące odmiedniczkowe zapalenie nerek), które obserwuje się w wielu chorobach zakaźnych (dur brzuszny, grypa , dusznica bolesna, posocznica). Częściej drobnoustroje są wprowadzane do nerek w sposób wstępujący z moczowodów, pęcherza moczowego, cewki moczowej (urogeniczne wstępujące odmiedniczkowe zapalenie nerek), czemu sprzyja dyskineza moczowodów i miednicy, zwiększone ciśnienie śródmiedniczkowe (odpływ pęcherzowo-nerkowy i odmiedniczkowy), a także reabsorpcja zawartości miednicy do żył rdzenia nerkowego ( refluks odmiedniczkowy). Wstępujące odmiedniczkowe zapalenie nerek z reguły komplikuje te choroby układu moczowo-płciowego, w których odpływ moczu jest utrudniony (kamienie i zwężenia moczowodów, zwężenia cewki moczowej, guzy układu moczowo-płciowego), dlatego często rozwija się w czasie ciąży. Możliwe jest również zakażenie limfogenne nerek (limfogenne odmiedniczkowe zapalenie nerek), gdy źródłem zakażenia są okrężnica i narządy płciowe. Dla rozwoju odmiedniczkowego zapalenia nerek, oprócz wnikania infekcji do nerek, duże znaczenie ma reaktywność organizmu i szereg lokalnych przyczyn, które powodują naruszenie odpływu moczu i zastój moczu. Te same powody wyjaśniają możliwość nawrotu przewlekłego przebiegu choroby. Zakażone drobnoustroje ze zmianami czynnościowymi i morfologicznymi w drogach moczowych prowadzącymi do zastoju moczu, upośledzonego odpływu żylnego i limfatycznego z nerki, przyczyniającego się do utrwalenia infekcji w nerkach, powodują ogniskowe i polimorficzne strefy nacieków zapalnych i ropienie śródmiąższowe jednego lub obie nerki. Dotknięta jest tkanka śródmiąższowa kanalików, a następnie nefron. Występuje produktywne zapalenie wsierdzia, przerost środkowej powłoki naczyń, zjawisko hialinozy, miażdżyca tętnic aż do wtórnej pomarszczonej nerki. W ostatnich latach pewną rolę w rozwoju przewlekłego odmiedniczkowego zapalenia nerek przypisuje się reakcjom autoimmunologicznym: pod wpływem antygenów bakteryjnych immunoglobulina G i dopełniacz odkładają się na błonie podstawnej naczyń włosowatych kłębuszków, powodując jej uszkodzenie. Przejście ostrego odmiedniczkowego zapalenia nerek w przewlekłe ułatwia: spóźnione rozpoznanie ostrego odmiedniczkowego zapalenia nerek, przedwczesna hospitalizacja, obecność przewlekłych infekcji, cukrzyca, dna moczanowa, nadużywanie leków przeciwbólowych - fenacetyna. Przewlekłe odmiedniczkowe zapalenie nerek występuje częściej u kobiet (50%), czemu sprzyjają ciąże, zwłaszcza powtarzające się (estrogeny powodują atonię mięśni gładkich dróg moczowych), w dzieciństwie u dziewcząt, co jest związane z budową dróg moczowych , ich anomalie. Obraz kliniczny. Jak wspomniano powyżej, możliwy jest zarówno ostry, jak i przewlekły przebieg odmiedniczkowego zapalenia nerek. Obraz kliniczny ostrej fazy choroby charakteryzuje się nagłym, gwałtownym wzrostem temperatury ciała do 39-40 ° C, może wystąpić osłabienie, ból głowy, dreszcze w połączeniu z obfitym poceniem się, nudnościami i wymiotami. Wraz ze wzrostem temperatury ciała pojawiają się bóle w okolicy lędźwiowej, które z reguły występują po jednej stronie. Charakter bólu jest tępy, ich intensywność jest inna. W przypadku rozwoju choroby na tle kamicy moczowej atak odmiedniczkowego zapalenia nerek poprzedza atak kolki nerkowej. W przypadku braku odpowiedniej terapii choroba może stać się przewlekła lub prowadzi to do rozwoju procesów ropnych w nerkach, które klinicznie objawiają się pogorszeniem ogólnego stanu pacjenta i nagłymi wahaniami temperatury (od 35-36 ° C rano do 40-41°C wieczorem). Przewlekłe odmiedniczkowe zapalenie nerek jest z reguły konsekwencją niedoleczonego ostrego odmiedniczkowego zapalenia nerek, kiedy można było usunąć ostry stan zapalny, ale nie było możliwe radykalne zniszczenie wszystkich patogenów w nerce lub przywrócenie fizjologicznego odpływu moczu z nerki. Przewlekłe odmiedniczkowe zapalenie nerek martwi się ciągłymi tępymi bólami w okolicy lędźwiowej, pogarszającymi się w wilgotnej zimnej pogodzie. Ponadto przewlekłe odmiedniczkowe zapalenie nerek jest podatne na okresowe zaostrzenia, gdy pacjent ma wszystkie objawy ostrego procesu. diagnostyka. Problem w rozpoznaniu choroby wynika z faktu, że objawy odmiedniczkowego zapalenia nerek są podobne do objawów innych chorób wynikających ze stanu zapalnego dróg moczowych. Plan badań diagnostycznych obejmuje badania krwi, badania moczu, a także badania pokazujące stan układu moczowego: USG nerek, badania rentgenowskie, analizę PCR na czynnik zakaźny. Aby zweryfikować rodzaj czynnika zakaźnego, konieczne jest przeprowadzenie hodowli bakteriologicznej próbki moczu, a metoda tomografii komputerowej służy do wykluczenia procesów nowotworowych. Tak więc laboratoryjne i specjalne metody badawcze mają ogromne znaczenie dla rozpoznania choroby. A w przewlekłym odmiedniczkowym zapaleniu nerek decydującymi, a czasem jedynymi objawami są zmiany w moczu, krwi i drogach moczowych. Niezbędne jest dynamiczne monitorowanie ciśnienia krwi i masy ciała pacjenta. We krwi leukocytoza, zwiększona ESR, przesunięcie neutrofilowe, wzrost poziomu azotu resztkowego (norma 20-40 mg), mocznik (norma 40-60 mg), kreatynina (norma 53-106 μmol / l), indican (norma 1,41-3,76 µmol/l), cholesterol (norma 180-200 mg), chlorki krwi (norma 83 mmol/l). Ważne dla diagnozy zmian w moczu: zmniejszenie ciężaru właściwego, białkomocz (w tym dobowy), krwiomocz i cylindrycznuria. Coraz większe znaczenie diagnostyczne zyskują jednak metody ilościowego oznaczania powstałych elementów osadu moczu: Kakovsky-Addis (normalne leukocyty do 4 milionów czerwonych krwinek - do 1 miliona, cylindry - do 2 tysięcy w ciągu 24 godzin), Amburger (normalne leukocyty do 2000 , erytrocyty - do 1400, cylindry - do 20 na 1 min), Nechiporenko (normalnie leukocyty do 2500, erytrocyty - do 1000, cylindry - do 20 w 1 ml świeżo wydanego moczu) . Stosunek bezwzględnej liczby erytrocytów i leukocytów w osadzie moczu w odmiedniczkowym zapaleniu nerek zmienia się dramatycznie w kierunku znaczącej przewagi leukocytów 10-20 razy. W przewlekłym odmiedniczkowym zapaleniu nerek w moczu pojawiają się komórki Stenheimera-Malbina: duże leukocyty, z ruchami Browna ziarnistości cytoplazmatycznych, pojawiającymi się ze spadkiem właściwości osmotycznych moczu (ciężar właściwy poniżej 10-14), zabarwione na niebiesko fioletem goryczki i safroniną, „aktywne” leukocyty: zmienione leukocyty, wykazujące ruchy Browna protoplazmy, widoczne po wybarwieniu 1% wodnym roztworem błękitu metylenowego z dodatkiem wody destylowanej. Wartość diagnostyczna wzrostu liczby „aktywnych” leukocytów i komórek Stenheimera-Malbina (do 40%), bakteriomocz (liczba drobnoustrojów ponad 100 tys. na 1 ml moczu), test azotynowy (z liczbą drobnoustrojów większą powyżej 100 tysięcy U, drobnoustroje rozkładają azotyny w moczu) po dodaniu kwasu sulfanilowego i L-naftyloaminy pojawia się czerwony kolor), kolorymetryczny test TTX (pod wpływem dehydrogenaz mikrobiologicznych chlorek trifenylotetrazolitu zostaje zredukowany do czerwonego nierozpuszczalnego trifenyloformazan w ciągu 4-10 godzin w temperaturze -37 ° C), prowokacyjny test prednizolonu (pacjent zbiera się w sterylnym naczyniu, środkowa porcja moczu jest kontrolną, następnie 30 mg prednizolonu w 10 ml soli fizjologicznej jest powoli wstrzykuje się do żyły, a środkową porcję moczu zbiera się trzy razy w odstępach godzinnych i po 24 godzinach, w przewlekłym odmiedniczkowym zapaleniu nerek liczba leukocytów, bakterii podwaja się, pojawiają się „aktywne” leukocyty, przynajmniej w jednej porcji), antybiogramy. Szczególną uwagę należy zwrócić na mikroskopię gruźlicy nerek (mikroskopia rozmazów barwionych według Tsil, wysiew moczu na specjalnych podłożach - metoda Preis i Shkolnikova, metoda biologiczna). W przypadku podejrzenia jednostronnego procesu konieczne jest przeprowadzenie badania moczu, osobno pobranego z każdej nerki specjalnymi cewnikami. Ważną rolę w diagnostyce przewlekłego odmiedniczkowego zapalenia nerek odgrywają radiologiczne metody badawcze: radiografia przeglądowa i tomografia (charakteryzują położenie, wielkość i kształt nerek), pielografia wydalnicza i wsteczna (zmniejszenie koncentracji i zdolności wydalniczej nerek, skurcze , anomalie, deformacje miednicy, kielichy), pneumopielografia (do rozpoznawania kamieni niekontrastowych), angiografia nerek (ujawnia naruszenie architektury naczyniowej - tętnice i żyły). W celu określenia bezpieczeństwa funkcji i miąższu nerek, zwłaszcza przy jednostronnym procesie, stosuje się metody radiosygnalizacyjne - renografię (jod hippuranu 131) i skanografię (przy użyciu neowodorku Hg 203). Biopsja punkcji w przypadku odmiedniczkowego zapalenia nerek z powodu ognisk procesu może nie dostarczyć informacji. Chromocystoskopia może wskazywać na uszkodzenie nerek. Leczenie. Najczęściej leczenie odmiedniczkowego zapalenia nerek jest zachowawcze, jednak jeśli ostre odmiedniczkowe zapalenie nerek ma charakter ropny, może być konieczna interwencja chirurgiczna. Leczenie zachowawcze obejmuje schemat, dietę, stosowanie antybiotyków, a także różne leki stabilizujące czynność nerek i organizmu pacjenta jako całości. W ostrym odmiedniczkowym zapaleniu nerek wskazany jest ścisły odpoczynek w łóżku. Pokarm należy spożywać pokarmy zawierające optymalną ilość białek, tłuszczów i węglowodanów. W ostrym okresie konieczne jest zastępowanie pokarmów białkowych i roślinnych. Przy silnym zatruciu musisz pić dużo wody. Leczenie przewlekłego odmiedniczkowego zapalenia nerek polega na wpływie na infekcję (etiotropową) w pierwotnym odmiedniczkowym zapaleniu nerek i wyeliminowaniu tej lub innej przyczyny w wtórnym odmiedniczkowym zapaleniu nerek, mechanizmach patogenetycznych i leczeniu powikłań. Najskuteczniejsze leczenie następuje po określeniu antybiogramu. Prowadzone jest ciągłe (co najmniej 2 miesiące) leczenie lekami przeciwbakteryjnymi. Natychmiast po przyjęciu przepisuje się antybiotyk, sulfanilamid lub nitrofuran. Po 1-10 dniach zmienia się leki, leczenie prowadzi się do trwałego zaniku leukocyturii i bakteriomoczu. Po wyeliminowaniu zaostrzenia, przerywane leczenie jednym ze środków przeciwbakteryjnych prowadzi się przez 4-5 miesięcy: lek podaje się przez 7 dni, następnie przerwę na 8-10 dni lub podaje się na 10 dni w odstępie 15-20 dni lub lek podaje się przez 15 dni, odstęp wynosi 15 dni, następnie ponownie przepisuje się terapię przeciwdrobnoustrojową. Czas trwania leczenia i odstępy są określane na podstawie objawów klinicznych i kontroli laboratoryjnej. Należy podkreślić, że w przypadku odmiedniczkowego zapalenia nerek, które rozwinęło się u chorego z przewlekłym zapaleniem migdałków, najskuteczniejsze są antybiotyki z serii penicylin, w przypadku infekcji narządów płciowych u mężczyzn i kobiet stosuje się antybiotyki o szerokim spektrum działania (tab. 12). . W obecności flory gram-ujemnej leczenie kwasem nalidyksowym daje dobre wyniki (czarne, ievigramon - 1,0 g 4 razy dziennie przez 7 dni, ale jego preparaty należy przepisywać rzadziej niż inne leki (2 razy)). Z preparatów sulfanilamidowych stosuje się etazol (1,0 g 4 razy - 10 dni), solafur (0,1 g 3 razy), długo działające sulfonamidy. Również kursy są leczone furazolidonem, furadoniną, furaginą (0,1 g 4 razy dziennie). Należy podkreślić, że czynność nerek należy określić przed rozpoczęciem leczenia. Długotrwałą antybiotykoterapię należy prowadzić przy szybkości filtracji kłębuszkowej co najmniej 30 ml/min lub przy resztkowej zawartości azotu w surowicy krwi nie większej niż 70 mg. Wskaźnikiem skuteczności leku po tygodniu leczenia jest zmniejszenie liczby drobnoustrojów do 10 000 w 1 ml moczu. Możliwe jest zmniejszenie zjadliwości mikroflory i zwiększenie skuteczności środków przeciwbakteryjnych poprzez zmianę odczynu moczu co 10-14 dni. Pokarm alkalizujący, cytrynian sodu (10 g dziennie), alkaliczne wody mineralne pomagają zmniejszyć odczyn pH. Pewne działanie przeciwbakteryjne ma benzoesan sodu (4-6 g dziennie), którego obficie występuje w żurawinie i mącznicy lekarskiej. Terapia patogenetyczna powinna mieć na celu zwiększenie reaktywności organizmu, poprawę odpływu moczu i normalizację ciśnienia krwi. Aby aktywować reaktywność immunobiologiczną, stosuje się α-globulinę, autohemoterapię, transfuzję krwi, terapię szczepionką (leczenie autoszczepionką prowadzi się przez 30-40 dni, 0,1 ml podskórnie lub 0,2-0,3 ml co 2 dni), toksoid gronkowcowy (0,1-0,3- 0,5-0,7-1,0-1,2-1,7-2,0 ml co 3 dni). Zioła moczopędne (mącznica lekarska, jagody jałowca, skrzyp polny, liść ortosyfonu - herbata nerkowa, liść borówki brusznicy), przeciwskurczowe (papaweryna, no-shpa, itp.) pomagają w normalizacji odpływu moczu. W przypadku utrudnienia przepływu moczu wskazane jest leczenie chirurgiczne. Przy współistniejącym nadciśnieniu wskazane są preparaty rauwolfia - izobaryna, dopegyt, hemiton, saluretyki, antagoniści aldosteronu. Profilaktyka i rokowanie. Zapobieganie odmiedniczkowemu zapaleniu nerek składa się ze środków pierwotnych i wtórnych. Profilaktyka pierwotna obejmuje przede wszystkim leczenie chorób, które mogą prowadzić do rozwoju odmiedniczkowego zapalenia nerek: zakażenia ogniskowe, choroby urologiczne (takie jak kamica moczowa, gruczolak prostaty, a także wszelkie choroby, którym towarzyszy naruszenie odpływu moczu z nerek), zajęcia rekreacyjne. Tabela 12 Porównawcza skuteczność leków przeciwbakteryjnych w odmiedniczkowym zapaleniu nerek
Profilaktyka wtórna obejmuje wykrycie bakteriomoczu podczas badań profilaktycznych (na przykład kobiety w ciąży powinny przeprowadzać analizę bakteriologiczną moczu co najmniej raz w miesiącu), wyznaczenie leczenia przeciw nawrotom: pierwszy tydzień każdego miesiąca - przerwa w leczeniu: wywar z dzikiej róży, drugi, trzeci tydzień - ziołowe leki moczopędne i antyseptyczne, czwarty tydzień - środki przeciwbakteryjne (nitrofurany, antybiotyki, antyseptyki, raz w roku - nevigramon 1 g 1 razy w tygodniu i 1,0 g - w drugim tygodniu lub 4 -NOC 2-5 mg 100 razy dziennie 150-4 dni). Leczenie przeciw nawrotom prowadzi się przez 2-3 lata. Badania lekarskie z leczeniem należy przeprowadzać 3-4 razy w roku lub 4-6 razy. Prognoza. Rokowanie zależy od stadium choroby. Leczenie sanatoryjne. Leczenie sanatoryjne jest wskazane w okresie remisji, zwłaszcza u pacjentów z wtórnym odmiedniczkowym zapaleniem nerek po operacjach urologicznych (wody mineralne Truskawiec, Sairme, Żeleznowodsk, Bieriezowski), gdzie pacjenci przyjmują wody niskozmineralizowane. Leczenie sanatoryjno-uzdrowiskowe jest przeciwwskazane w przypadku wysokiego nadciśnienia, ciężkiej anemii i oczywistej niewydolności nerek. Powikłania odmiedniczkowego zapalenia nerek są zróżnicowane. W ostrym odmiedniczkowym zapaleniu nerek progresja procesu ropnego prowadzi do zespolenia dużych ropni i powstania karbunkułu nerki, połączenia ropnych jam z miednicą (roponercze), przejścia procesu do włóknistej torebki (zapalenie krocza ) i tkanki okołonerkowej (zapalenie paranerkowe). Ostre odmiedniczkowe zapalenie nerek może być powikłane martwicą brodawek piramid (papillonekrosis), która rozwija się w wyniku bezpośredniego toksycznego działania bakterii w warunkach zastoju moczu. To powikłanie odmiedniczkowego zapalenia nerek występuje w większości przypadków u pacjentów z cukrzycą. Rzadko odmiedniczkowe zapalenie nerek staje się źródłem sepsy. Przy ograniczeniu procesu ropnego w okresie bliznowacenia mogą powstawać ropnie otoczone błoną ropotwórczą (przewlekły ropień nerki). W przewlekłym odmiedniczkowym zapaleniu nerek, zwłaszcza jednostronnym, możliwe jest wystąpienie nadciśnienia nerkowego i miażdżycy w drugiej (nienaruszonej) nerce. Obustronne odmiedniczkowe zmarszczki nerek prowadzą do przewlekłej niewydolności nerek. Skutkiem ostrego odmiedniczkowego zapalenia nerek jest zwykle wyzdrowienie, ale w wyniku powikłań (roponercze, posocznica, papilonekroza) może dojść do śmierci. Przewlekłe odmiedniczkowe zapalenie nerek ze zmarszczkami nerek często kończy się mocznicą azotemią. Wraz z rozwojem nadciśnienia tętniczego pochodzenia nerkowego, śmiertelny wynik w przewlekłym odmiedniczkowym zapaleniu nerek jest czasami związany z powikłaniami występującymi w nadciśnieniu (krwotok mózgowy, zawał mięśnia sercowego itp.). Autor: Mostovaya OS
▪ Metody nauczania psychologii. Notatki do wykładów ▪ Prawo procesowe cywilne. Kołyska
Otwarto najwyższe obserwatorium astronomiczne na świecie
04.05.2024 Sterowanie obiektami za pomocą prądów powietrza
04.05.2024 Psy rasowe chorują nie częściej niż psy rasowe
03.05.2024
▪ Nadprzewodnikowy silnik elektryczny Toshiba ▪ Laser może zajrzeć przez dziurkę od klucza ▪ Stały Internet w samochodzie ▪ Procesory Imagination Catapult RISC-V ▪ Sterownik wyświetlacza LED MAX6957
▪ część witryny Materiały referencyjne. Wybór artykułu ▪ artykuł Bezpieczeństwo i higiena przemysłowa. Informator ▪ artykuł Ogólne środki zapewnienia bezpieczeństwa przemysłowego ▪ artykuł Lampa już nie migocze. Encyklopedia elektroniki radiowej i elektrotechniki
Strona główna | biblioteka | Artykuły | Mapa stony | Recenzje witryn www.diagram.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese








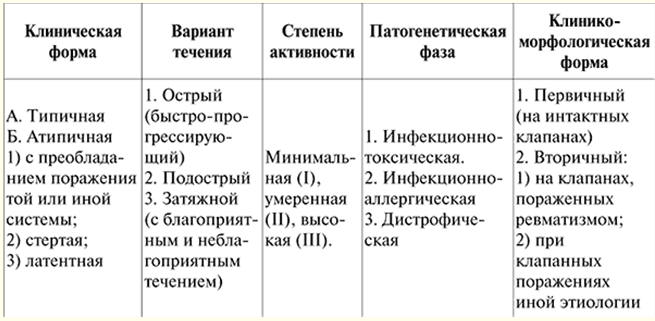








 Zobacz inne artykuły Sekcja
Zobacz inne artykuły Sekcja 