
|
Notatki z wykładów, ściągawki
Anestezjologia i resuscytacja. Ściągawka: krótko, najważniejsza
Katalog / Notatki z wykładów, ściągawki Spis treści
1. Pojęcie resuscytacji Resuscytacja to dział medycyny klinicznej zajmujący się problematyką rewitalizacji organizmu, opracowując zasady profilaktyki stanów terminalnych, metody resuscytacji i intensywnej terapii. Praktyczne metody rewitalizacji ciała łączy koncepcja „resuscytacji”. Resuscytacja (z łac. „odrodzenie” lub „animacja”) to system środków mających na celu przywrócenie poważnie uszkodzonych lub utraconych funkcji życiowych organizmu i wyprowadzenie go ze stanu terminalnego i śmierci klinicznej. Skuteczne środki resuscytacyjne to pośredni masaż serca i sztuczna wentylacja płuc. Jeśli nie będą skuteczne w ciągu 30 minut, stwierdza się śmierć biologiczną. Intensywna terapia to zestaw środków stosowanych w leczeniu ciężkich, zagrażających życiu stanów i obejmuje stosowanie, zgodnie ze wskazaniami, szerokiej gamy środków terapeutycznych, w tym wlewów dożylnych, przedłużonej wentylacji mechanicznej, stymulacji elektrycznej, metod dializy itp. Stanem krytycznym jest niemożność utrzymania integralności funkcji organizmu w wyniku ostrej dysfunkcji narządu lub układu, wymagającej wymiany leku lub sprzętu-instrumentu. Stan terminalny to stan graniczny między życiem a śmiercią, odwracalne wygaśnięcie funkcji organizmu, w tym etapy preagony, agonii i śmierci klinicznej. Śmierć kliniczna jest stanem końcowym, w którym nie ma krążenia krwi i oddychania, aktywność kory mózgowej ustaje, ale procesy metaboliczne są zachowane. W przypadku śmierci klinicznej pozostaje możliwość skutecznej resuscytacji. Czas trwania śmierci klinicznej wynosi od 5 do 6 minut. Śmierć biologiczna to nieodwracalne zatrzymanie procesów fizjologicznych w narządach i tkankach, w których resuscytacja jest niemożliwa. Ustala się go przez kombinację szeregu objawów: brak spontanicznych ruchów, skurcze serca i tętna w dużych tętnicach, oddychanie, reakcje na bolesne bodźce, odruch rogówkowy, maksymalne rozszerzenie źrenic i brak ich reakcji na światło. Wiarygodne oznaki początku śmierci to spadek temperatury ciała do 20 C, pojawienie się plam zwłok i stwardnienie mięśni pośmiertnych. 2. Podstawowe manipulacje na oddziale intensywnej terapii Przezskórne nakłucie i cewnikowanie żyły głównej (podobojczykowej). Wskazania: duże objętości terapii wlewowo-transfuzyjnej, żywienie pozajelitowe, terapia detoksykacyjna, antybiotykoterapia dożylna, sondowanie i kontrastowanie serca, pomiar CVP, wszczepienie rozrusznika serca, niemożność cewnikowania żył obwodowych. Przeciwwskazania: naruszenie układu krzepnięcia krwi, proces zapalny i ropny w miejscu nakłucia i cewnikowania, uraz obojczyka, zespół żyły głównej górnej, zespół Pageta-Schrettera. Oprzyrządowanie i akcesoria do nakłuwania i cewnikowania: igła do punkcji, komplet plastikowych cewników, komplet przewodników, strzykawka 10 ml do iniekcji domięśniowych, nożyczki, igła igła, igła chirurgiczna i ligatura jedwabna, plaster samoprzylepny. Technika: cewnikowanie przeprowadza się zgodnie z zasadami aseptyki i antyseptyki, leczenia rąk operatora, pola operacyjnego i owinięcia sterylnym materiałem. Pacjent jest ułożony poziomo na plecach z rękoma przyłożonymi do ciała i klapą głowy w przeciwnym kierunku. Stosuje się znieczulenie miejscowe - 0,5-1% roztwór nowokainy. Nakłucie najlepiej wykonać po prawej stronie, ponieważ przy nakłuciu lewej żyły podobojczykowej istnieje niebezpieczeństwo uszkodzenia piersiowego przewodu limfatycznego. Punkt nakłucia - na granicy wewnętrznej i środkowej trzeciej części obojczyka 2 cm poniżej. Igłę wprowadza się powoli pod kątem 45 do obojczyka i 30-40 do powierzchni klatki piersiowej między obojczykiem a I żebrem w kierunku górnej krawędzi stawu mostkowo-obojczykowego. Trzymając igłę, tłok strzykawki jest okresowo dokręcany, aby określić, czy wchodzi do żyły, a wzdłuż igły wstrzykuje się nowokainę. Podczas przekłuwania żyły czasami pojawia się uczucie porażki. Po wejściu do żyły strzykawkę odłącza się od igły, a kaniulę zamyka się palcem. Następnie przez igłę wprowadza się przewodnik na długość 15-20 cm i igłę usuwa się. Przez przewodnik przepuszcza się cewnik o odpowiedniej średnicy i wraz z przewodem wprowadza się do żyły na 6-8 cm, po czym przewodnik jest ostrożnie usuwany. Aby sprawdzić prawidłowe położenie cewnika, podłącza się do niego strzykawkę i pobiera do niego 2-3 ml krwi, po czym zakłada się zatyczkę lub rozpoczyna terapię infuzyjną. Cewnik mocowany jest do skóry jedwabną ligaturą. Aby to zrobić, na cewniku 3-5 mm od skóry wykonuje się rękaw z plastra samoprzylepnego, na którym zawiązuje się jedwab, a następnie przepuszcza przez uszy cewnika i ponownie zawiązuje. Po zamocowaniu cewnika miejsce nakłucia zamyka się aseptyczną naklejką. Powikłania: nakłucie tętnicy podobojczykowej, zator powietrzny, nakłucie jamy opłucnej, uszkodzenie splotu ramiennego, uszkodzenie piersiowego przewodu limfatycznego, uszkodzenie tchawicy, wola i tarczycy, ropienie w miejscu nakłucia. 3. Tracheostomia. Konikostomia Tracheostomia Wskazania: niedrożność krtani i górnej tchawicy spowodowana niedrożnością guza lub ciała obcego, porażenie i skurcz strun głosowych, ciężki obrzęk krtani, ostra niewydolność oddechowa, aspiracja wymiocin, zapobieganie zamartwicy w ciężkich urazach klatki piersiowej. Narzędzia: 2 skalpele, 2 pęsety anatomiczne i chirurgiczne, kilka kleszczy hemostatycznych, podnośnik, sonda ryflowana, 2 tępe i 1 jednozębny ostry haczyk, rozszerzacz Trousseau lub Deschamps, igły chirurgiczne z uchwytem na igłę. Technika. Pacjent leży na plecach, wałek pod ramionami, głowa jest odrzucona do tyłu. Jeśli pacjent jest w stanie asfiksji, wałek zakłada się dopiero w ostatniej chwili, przed otwarciem tchawicy. Miejscowe znieczulenie infiltracyjne wykonuje się 0,5-1% roztworem nowokainy z dodatkiem adrenaliny. W ostrej asfiksji można operować bez znieczulenia. Punkty identyfikacji: kąt chrząstki tarczycy i guzek łuku chrząstki pierścieniowatej. Cięcie skóry, tkanki podskórnej i powierzchownej powięzi wykonuje się od dolnej krawędzi chrząstki tarczycy do wcięcia szyjnego ściśle wzdłuż linii środkowej szyi. Żyła środkowa szyi jest cofana lub podwiązywana, znajdując białą linię, wzdłuż której mięśnie są rozpychane tępo i odsłania się przesmyk tarczycy. Krawędzie nacięcia rozsuwa się za pomocą rozszerzacza Trousseau, na brzeg rany zakłada się ligatury i ostrożnie wprowadza się rurkę tracheostomijną, upewniając się, że jej koniec wchodzi do światła tchawicy. Rana chirurgiczna zostaje zszyta. Rurka mocowana jest na szyi pacjenta za pomocą szyny z gazy, uprzednio przywiązanej do osłony tuby. Włóż dętkę do dętki. Konikostomia Pacjent kładzie się na plecach za pomocą poprzecznego wałka na wysokości łopatek. Głowa pacjenta jest odchylona do tyłu. Krtań mocuje się palcami na bocznych powierzchniach chrząstki tarczycy i wyczuwa się szczelinę między tarczycą a chrząstką pierścieniowatą, gdzie znajduje się więzadło w kształcie stożka. W znieczuleniu miejscowym nasiękowym spiczastym skalpelem wykonuje się poprzeczne nacięcie skóry o długości około 2 cm, wyczuwa się więzadło stożkowe i rozcina lub perforuje. Kaniulę tracheostomijną o odpowiedniej średnicy wprowadza się do utworzonego otworu i mocuje paskiem z gazy wokół szyi. W przypadku braku kaniuli można ją zastąpić kawałkiem gumowej lub plastikowej rurki o odpowiedniej średnicy i długości. Aby zapobiec ześlizgnięciu się tej rurki do tchawicy, jej zewnętrzny koniec przekłuwa się poprzecznie w odległości 2 cm od krawędzi i mocuje paskiem z gazy. Conicotome to metalowa kaniula tracheostomijna o małej średnicy z umieszczonym wewnątrz trzpieniem przebijającym. Po wypreparowaniu skóry nad więzadłem stożkowym przekłuwa się ją konikotomem, usuwa mandrynę, kaniulę umieszcza się w pozycji zapewniającej swobodny przepływ powietrza do tchawicy i mocuje. 4. Intubacja tchawicy Wskazania: zwężenie krtani, patologiczny oddech, ostra niewydolność oddechowa, śpiączka II i III stopnia, wysokie ryzyko aspiracji podczas zabiegów chirurgicznych na narządach klatki piersiowej i jamy brzusznej, głowy i szyi, w chorobach gardła, krtani i tchawicy (ostre stany zapalne, nowotwory, gruźlica itp.). Do intubacji używa się laryngoskopu. Składa się z rękojeści i ostrza. Najczęściej używane zakrzywione ostrza, ponieważ są bardziej fizjologiczne. Proste ostrza są używane z długą szyją. Przygotowanie do intubacji obejmuje sprawdzenie sprzętu i prawidłowe ustawienie pacjenta. Należy sprawdzić rurkę dotchawiczą. Mankiet jest testowany poprzez napompowanie go strzykawką o pojemności 10 ml. Sprawdź kontakt ostrza z rękojeścią laryngoskopu i żarówką. Konieczne jest upewnienie się, że odsysanie jest gotowe w przypadku nagłego wydzieliny plwociny, krwawienia lub wymiotów. Pomyślna intubacja zależy od prawidłowej pozycji pacjenta. Głowa pacjenta powinna znajdować się na poziomie wyrostka mieczykowatego intubatora. Umiarkowane uniesienie głowy z jednoczesnym wyprostem w stawie szczytowo-potylicznym stwarza lepszą pozycję do intubacji. Przygotowanie do intubacji obejmuje również obowiązkową preoksygenację. Laryngoskop jest trzymany w ręce niedominującej (dla większości osób jest to lewa), a drugą ręką szeroko otwiera się usta pacjenta. Ostrze jest wprowadzane wzdłuż prawej strony części ustnej gardła, aby uniknąć uszkodzenia zębów. Język jest przesunięty w lewo, a ostrze uniesione do łuku gardła. Czubek zakrzywionego ostrza wprowadza się do doliny (dołek znajdujący się na przedniej powierzchni nagłośni), podczas gdy czubek ostrza prostego powinien bezpośrednio unosić nagłośnię. Rękojeść laryngoskopu unosi się do góry i do przodu prostopadle do żuchwy, aż do ukazania się strun głosowych. Należy unikać polegania na zębach. Rurka dotchawicza jest pobierana w prawą rękę i przepuszczana przez otwartą głośnię pod kontrolą wzroku. Mankiet powinien być umieszczony w górnej tchawicy, ale poniżej krtani. Laryngoskop jest usuwany z jamy ustnej, ponownie unikając uszkodzenia zębów. Bezpośrednio po intubacji wykonuje się osłuchiwanie płuc po obu stronach (ponieważ można wprowadzić rurkę do jednego oskrzela) oraz w nadbrzuszu (w celu wykluczenia intubacji przełyku). Jeśli rurka znajduje się w tchawicy, mocuje się ją wstążkami, a mankiet jest napompowany. Mankiet powinien być umieszczony powyżej poziomu chrząstki pierścieniowatej, ponieważ długie przebywanie w krtani może prowadzić do chrypki w okresie pooperacyjnym. Powikłania: intubacja przełyku, oskrzeli, umiejscowienie mankietu w krtani, uszkodzenie zębów, zwichnięcie żuchwy, skurcz krtani, zaburzenia odruchowe (nadciśnienie, tachykardia, podwyższone ciśnienie śródczaszkowe), urazy dróg oddechowych, stany zapalne itp. 5. Nakłucie i cewnikowanie przestrzeni zewnątrzoponowej Wskazania: zespół silnego bólu, interwencje chirurgiczne, zapewnienie analgezji pooperacyjnej. Poziom ustawienia blokady zewnątrzoponowej zależy od tego, który narząd wymaga znieczulenia. Poziomy kręgosłupa i „narządów docelowych” w znieczuleniu zewnątrzoponowym
Oprzyrządowanie: igły do znieczulenia, specjalna igła do nakłuwania przestrzeni zewnątrzoponowej, strzykawka do próbek, cewnik, korek, kulki filtracyjne, serwetki, taśma klejąca i sterylne rękawiczki. Pozycja pacjenta siedzi lub leży na boku. W takim przypadku kolana i podbródek powinny znajdować się jak najbliżej klatki piersiowej. W ten sposób powstaje maksymalne zgięcie kręgosłupa, przy którym zwiększa się kąt między wyrostkami kolczystymi sąsiednich kręgów i ułatwia dostęp do więzadła żółtego. W warunkach aseptycznych i w znieczuleniu miejscowym 0,5% roztworem nowokainy wykonuje się nakłucie przestrzeni nadtwardówkowej. Igła jest wstrzykiwana ściśle prostopadle, ale w przypadku osteochondrozy możliwy jest kąt nachylenia lub podczas nakłucia w okolicy środkowej klatki piersiowej. Gdy igła wejdzie w grubość więzadeł, usuwa się z niej mandrynę i dołącza się strzykawkę z płynem. Dalsze przesuwanie igły odbywa się powoli i płynnie z naciskiem na tłok strzykawki. Ze względu na znaczny opór więzadeł płyn nie może opuścić strzykawki. Strzykawka jest odłączona, a cewnik włożony na 5-7 cm, nie powinno być żadnego oporu. Igłę usuwa się, a prowadnik mocuje się z tyłu za pomocą plastra samoprzylepnego, doprowadzając go do przedniej powierzchni klatki piersiowej. Wtyczka z filtrem jest przymocowana do przewodu. Wstrzykuje się środek znieczulający. Następnie określa się poziom znieczulenia skóry. Powikłania: zaburzenia oddechowe i hemodynamiczne, zatrucie, uszkodzenie opony twardej, powikłania neurologiczne, zapalenie okołotwardówkowe. 6. Ostre zaburzenia świadomości Świadomość jest najwyższą formą odbicia rzeczywistości, która jest zbiorem procesów psychicznych, które pozwalają człowiekowi poruszać się w otaczającym go świecie, czasie, własnej osobowości, która zapewnia jego zachowanie. Upośledzenie świadomości to ogólna nazwa zaburzeń integralnej aktywności mózgu, wyrażających się naruszeniem zdolności do odpowiedniego postrzegania, rozumienia i reagowania na otoczenie, poruszania się po nim, zapamiętywania bieżących wydarzeń, nawiązywania kontaktu głosowego i wykonywania arbitralnych środków akty behawioralne. Istnieją różne opcje depresji świadomości (otępienie, otępienie, śpiączka o różnej głębokości), a także ostre splątanie (stan delirium lub encefalopatia metaboliczna). Stopień upośledzonej świadomości waha się od lekkiego splątania do śpiączki i nie ma wyraźnych przejść między tymi stanami. W praktyce stopień upośledzenia świadomości zależy od reakcji pacjenta na bodźce. Otępienie to forma zaburzonej świadomości, charakteryzująca się letargiem, spowolnieniem i trudnościami w przebiegu procesów psychicznych, szybkim wyczerpaniem uwagi, podwyższeniem progu percepcji bodźców zewnętrznych, ale przy zachowaniu ograniczonego kontaktu werbalnego. Ogłupienie polega na naruszeniu uwagi, tj. umiejętności wybierania niezbędnych informacji i koordynowania reakcji w taki sposób, aby nie naruszać logicznej sekwencji myśli i działań. Najczęstszymi przyczynami otępienia są zaburzenia metaboliczne i toksyczne, ale czasami obserwuje się je również w zmianach ogniskowych kory, zwłaszcza prawego płata ciemieniowego. U takich pacjentów możliwe jest uzyskanie odpowiedzi jednosylabowej lub wykonanie najprostszych instrukcji tylko po uporczywych apelach lub dodatkowej stymulacji. Wraz z dalszym uciskiem świadomości traci się możliwość kontaktu głosowego i rozwija się sopor. Sopor to stan głębokiej depresji świadomości z utratą możliwości kontaktu z pacjentem, ale zachowaniem skoordynowanych reakcji obronnych i otwarciem oczu pacjenta w odpowiedzi na ból, dźwięk lub inne bodźce. Pacjenta nie można w pełni wybudzić nawet przy pomocy bolesnych bodźców, leży z zamkniętymi oczami. Reakcja na instrukcje słowne jest słaba lub całkowicie nieobecna, nie można uzyskać od pacjenta słowa odpowiedzi lub dźwięku. Wraz z dalszym uciskiem świadomości rozwija się śpiączka. Śpiączka to stan nieświadomości charakteryzujący się niewrażliwością na bodźce zewnętrzne. Jest to zagrażający życiu stan depresji funkcji ośrodkowego układu nerwowego i zaburzeń regulacji funkcji życiowych. Śpiączka może być spowodowana wieloma różnymi zaburzeniami metabolicznymi i uszkodzeniami strukturalnymi. 7. Badanie pacjenta ze śpiączką Plan badania pacjenta jest następujący. 1. Ocena stanu funkcjonalnego układu oddechowego i sercowo-naczyniowego. 2. Ogólne badania kliniczne z uwzględnieniem danych laboratoryjnych, pozwalające na ocenę patologii pozaczaszkowej. 3. Badanie neurologiczne. Badania laboratoryjne: ogólne kliniczne badanie krwi (objawy infekcji bakteryjnej lub wirusowej); biochemiczne badanie krwi: glukoza, czynniki krzepnięcia (czas krzepnięcia, protrombina, fibrynogen, APTT, antytrombina III, testy parakoagulacyjne, liczba płytek), mocznik, kreatynina, bilirubina, ALT, AST, osmolarność, elektrolity (K, Na, Mg , Ca) ; badanie toksykologiczne krwi, moczu, treści żołądkowej. Badania instrumentalne: radiografia czaszki i kręgosłupa szyjnego. Konsultacja neuropatologa (neurochirurga) wyznacza dalszy kierunek poszukiwań diagnostycznych: rezonans komputerowy lub rezonans magnetyczny; EEG; dopplerografia ultradźwiękowa. Nakłucie lędźwiowe z analizą płynu mózgowo-rdzeniowego jest obowiązkowe po: 1) konsultacja okulisty i wykluczenie oznak zwiększonego ciśnienia śródczaszkowego - obrzęk i uniesienie tarczy wzrokowych; 2) wykluczenie oznak przepukliny mózgu. Wyróżnia się następujące lokalizacje przepukliny mózgu. Przepuklina międzymózgowia, która występuje, gdy uszkodzona jest przyśrodkowa lokalizacja nadnamiotowa i polega na przemieszczeniu międzymózgowia przez wycięcie ścięgna móżdżku. Ten proces wywołuje: 1) oddychanie Cheyne-Stokesa; 2) zwężenie źrenic przy zachowaniu ich reakcji na światło; 3) paraliż spojrzenia w górę; 4) zmiany stanu psychicznego. Przepuklina przyśrodkowych części płata skroniowego, która występuje, gdy dotknięta jest boczna lokalizacja nadnamiotowa, polega na przemieszczeniu przyśrodkowych części płata skroniowego przez wycięcie czopu móżdżku. Powstały nacisk na struktury śródmózgowia objawia się: 1) upośledzona świadomość; 2) powiększoną, niereaktywną źrenicę po stronie przepukliny, co wiąże się z uciskiem nerwu czaszkowego III; 3) niedowład połowiczy po przeciwnej stronie. Ruchy gałek ocznych nie zawsze są zaburzone. Przepuklina migdałków móżdżku, która jest spowodowana naciskiem przepychającym dolną część móżdżku przez otwór wielki, co prowadzi do ucisku rdzenia przedłużonego. Wywołuje: 1) upośledzona świadomość; 2) naruszenia rytmu oddychania lub bezdechu. 8. Leczenie śpiączki Leczenie powinno być jak najbardziej agresywne i ukierunkowane przede wszystkim na zapewnienie odpowiedniego dotlenienia i stabilizacji hemodynamiki ośrodkowej. W przypadku podtrzymania oddychania spontanicznego zaleca się wdmuchiwanie nawilżonego tlenu przez maskę lub cewnik nosowy. W przypadku braku oddychania spontanicznego lub w obecności oddychania patologicznego wykonuje się intubację tchawicy i pacjenta przenosi się do sztucznej wentylacji płuc. Przy pobudzeniu psychoruchowym i reakcji na wentylację mechaniczną konieczne jest stosowanie środków uspokajających (benzodiazepiny, butyrofenony). Stabilizacja centralnej hemodynamiki to normalizacja ciśnienia krwi. W stanie nadciśnienia ciśnienie krwi musi zostać obniżone, ale nie więcej niż 10% pierwotnego na godzinę. Dobrym efektem jest zastosowanie nitroprusydku sodu lub siarczanu magnezu. W przypadku niedociśnienia stosuje się dopaminę, dopaminę, dobutreks i leki hormonalne. W przypadku braku danych anamnestycznych i niejasnej diagnozy przeprowadza się terapię eksjuwantybusem (pozytywna odpowiedź na ekspozycję na lek z jednej strony daje klucz do diagnozy, z drugiej pozwala kupić czas, aby uniknąć nieodwracalnych zmian) : 1) tiamina - 100 mg dożylnie, następnie - 100 mg domięśniowo (szczególnie w przypadku alkoholizmu w wywiadzie, przy określaniu wysokich stężeń etanolu we krwi); 2) glukoza - dożylnie 40% roztwór 60 ml (o nieznanym poziomie glukozy w osoczu lub na poziomie poniżej 3 mmol / l); 3) nalokson - 0,4-1,2 mg dożylnie, frakcyjnie, wielokrotnie, zwłaszcza w obecności "objawów opiatowych" (ślady wstrzyknięć dożylnych, wąskie źrenice, zaburzenia ośrodkowego układu oddechowego); 4) anexat (flumazenil) - 0,2 mg przez 30 sekund, w ciągu kolejnej minuty dodać kolejne 0,3 mg, co minutę - 0,5 mg do łącznej dawki 3 mg. W przypadku braku efektu można założyć, że jest mało prawdopodobne, aby śpiączka była spowodowana lekami benzodiazepinowymi; 5) w przypadku zatrucia lub przedawkowania znanym lekiem lub substancją należy podać odpowiednie antidotum (jeśli istnieje możliwość leczenia antidotum). Zabieg przeprowadza się: 1) kontrola zespołu konwulsyjnego; 2) utrzymanie normotermii; 3) zapobieganie aspiracji treści żołądkowej; 4) leczenie urologiczne; 5) spadek ciśnienia śródczaszkowego. 9. Resuscytacja krążeniowo-oddechowa Resuscytacja krążeniowo-oddechowa (RKO) to zespół zabiegów chirurgicznych i terapeutycznych wykonywanych przy braku urazów zagrażających życiu, mających na celu przywrócenie i wspomaganie funkcji układu sercowo-oddechowego. Wskazania do resuscytacji krążeniowo-oddechowej: wykonywana u pacjentów z brakiem efektywnego tętna na tętnicach szyjnych lub nitkowatym, słabym tętnem, którzy są nieprzytomni i (lub) przy braku efektywnych ruchów oddechowych. Najczęstsze przypadki pierwotnego zatrzymania krążenia, a także pierwotnej niewydolności oddechowej. Przeciwwskazania: uraz niezgodny z życiem, terminalne stadia nieuleczalnych chorób i śmierć biologiczna. Podstawowe zasady Podstawowe wysiłki w resuscytacji krążeniowo-oddechowej mają na celu: 1) kompresja klatki piersiowej; 2) wdmuchiwanie powietrza do płuc i wentylację; 3) przygotowanie i podawanie leków; 4) instalacja i konserwacja dostępu dożylnego; 5) czynności specjalistyczne (defibrylacja, instalacja rozrusznika, intubacja tchawicy). Do realizacji pełnego zakresu działań potrzebne są więc 4 osoby oraz lider zespołu. Jedna osoba powinna być odpowiedzialna za resuscytację krążeniowo-oddechową. Osoba ta powinna zintegrować wszystkie dostępne informacje i nadać priorytet wpływowi. Musi monitorować monitor EKG, stosowanie leków i upewnić się, że działania innych członków zespołu są korygowane. Powinien zostać usunięty z wykonywania procedur, które umniejszają rolę lidera. Od ponad 40 lat alfabet resuscytacji Safar jest używany do resuscytacji krążeniowo-oddechowej. W tym kompleksie zachowana jest sekwencja działań resuscytatora, zgodnie z ich angielską nazwą są one oznaczone odpowiednimi literami. A - Drogi oddechowe - zapewnienie drożności dróg oddechowych. B - Oddychanie - sztuczna wentylacja płuc (ALV) w przystępny sposób, np. podczas oddychania „usta-usta”. C - Krążenie - zapewniające hemokrążenie - pośredni masaż serca. D - Narkotyki - wprowadzenie narkotyków. E - Elektrokardiografia - rejestracja EKG. F - Fibrylacja - przeprowadzanie w razie potrzeby defibrylacji elektrycznej (kardiowersji). G - Gauging - ocena wyników pierwotnych. H - Hipotermia - chłodzenie głowy. I - Intensywna terapia - intensywna terapia zespołów poresuscytacyjnych. 10. Zapewnienie drożności dróg oddechowych. IVL A - Drogi oddechowe - zarządzanie drogami oddechowymi Pacjent kładzie się poziomo na plecach. Głowa jest odrzucona tak bardzo, jak to możliwe. Jeśli pacjent z obniżonym napięciem mięśniowym leży na plecach, jego język może zapadać się, jakby ugniatał gardło. W tym samym czasie nagłośnia opada, dodatkowo blokując drogi oddechowe. Pojawiają się: dźwięczny oddech, a następnie naruszenia rytmu oddechowego aż do całkowitego zatrzymania. Takie zjawiska rozwijają się szczególnie szybko u pacjentów nieprzytomnych. Aby zapobiec i wyeliminować cofanie języka, należy wysunąć żuchwę do przodu i jednocześnie wykonać przeprost w stawie potyliczno-szyjnej. Aby to zrobić, z naciskiem kciuków na brodę dolną szczękę pacjenta przesuwa się w dół, a następnie palcami umieszczonymi w rogach szczęki popychają ją do przodu, uzupełniając tę technikę przeprostem głowy wstecz (technika potrójnego Safar). Przy prawidłowym i terminowym przeprowadzeniu tych manipulacji drożność dróg oddechowych na poziomie gardła zostaje szybko przywrócona. Przyczyną niedrożności dróg oddechowych mogą być ciała obce. Są szybko usuwane za pomocą improwizowanych materiałów (serwetek). Głowa pacjenta powinna być zwrócona na bok ze względu na niebezpieczeństwo aspiracji. Przywrócenie drożności górnych dróg oddechowych ułatwia zastosowanie różnych kanałów powietrznych. Najbardziej celowe jest zastosowanie kanału powietrznego w kształcie litery S. W celu jego wprowadzenia otwiera się usta pacjenta skrzyżowanymi palcami II i I, a rurkę przesuwa się do nasady języka tak, aby jej otwór „przesuwał się” wzdłuż podniebienia. Należy zadbać o to, aby kanał powietrzny nie poruszał się podczas transportu. Jeśli wszystkie opisane procedury nie są skuteczne, możemy założyć obecność obturacji dróg oddechowych w leżących poniżej odcinkach. W takich przypadkach wymagana jest bezpośrednia laryngoskopia i aktywna aspiracja patologicznej wydzieliny, a następnie intubacja tchawicy przez 10-15 sekund. Wskazane jest wykonanie konikotomii i tracheostomii. B - Oddychanie - sztuczna wentylacja płuc (ALV) w przystępny sposób Najprostszą i najskuteczniejszą metodą sztucznego oddychania podczas resuscytacji jest metoda usta-usta. Po 2-3 napełnieniach płuc określa się obecność tętna na tętnicy szyjnej, jeśli nie zostanie wykryty, wówczas przystępują do sztucznego przywrócenia krążenia krwi. Wentylację ręczną stosuje się za pomocą samorozprężnego worka typu Ambu. Podczas korzystania z respiratora częstość oddechów wynosi 12-15 na minutę, objętość wdechowa wynosi 0,5-1,0 litra. W szpitalu wykonuje się intubację tchawicy, a pacjenta przenosi się do respiratora. 11. Pośredni masaż serca C-Circulation - zapewnienie hemocyrkulacji - uciśnięcia klatki piersiowej Masaż przy zamkniętym sercu to najprostszy i najskuteczniejszy sposób awaryjnego wspomagania krążenia. Zamknięty masaż serca należy rozpocząć natychmiast po rozpoznaniu ostrego zatrzymania krążenia, nie wyjaśniając jego przyczyn i mechanizmów. W przypadku nieskutecznych skurczów serca nie należy czekać na całkowite zatrzymanie akcji serca lub samodzielne przywrócenie prawidłowej czynności serca. Podstawowe zasady masażu zamkniętego serca. 1. Pacjent powinien znajdować się w pozycji poziomej na solidnym podłożu (podłoga lub niska kanapa), aby zapobiec możliwości przemieszczenia się jego ciała pod wpływem wzmocnienia rąk masujących. 2. Strefa stosowania siły rąk resuscytatora znajduje się w dolnej jednej trzeciej mostka, ściśle wzdłuż linii środkowej; resuscytator może znajdować się po obu stronach pacjenta. 3. Do masażu kładzie się jedną dłoń na drugiej i naciska się na mostek w obszarze położonym 3-4 poprzeczne palce powyżej miejsca przywiązania do mostka wyrostka mieczykowatego; ręce masażera, wyprostowane w stawach łokciowych, są ustawione tak, że tylko nadgarstek wytwarza ucisk. 4. Kompresja klatki piersiowej poszkodowanego wykonywana jest ze względu na siłę ciężkości tułowia lekarza. Przemieszczenie mostka w kierunku kręgosłupa (tj. głębokość ugięcia klatki piersiowej) powinno wynosić 4-6 cm. 5. Czas trwania jednego uciśnięcia klatki piersiowej wynosi 0,5 s, odstęp między poszczególnymi uciśnięciami wynosi 0,5-1 s. Tempo masażu - 60 ruchów masujących na minutę. W odstępach ręce nie są usuwane z mostka, palce pozostają uniesione, ramiona są całkowicie wyprostowane w stawach łokciowych. Gdy resuscytację prowadzi jedna osoba, po dwóch szybkich wstrzyknięciach powietrza do płuc pacjenta wykonuje się 15 uciśnięć klatki piersiowej, czyli stosunek „wentylacja:masaż” wynosi 2:15. stosunek ten wynosi 2:1, co oznacza 5 uciśnięć klatki piersiowej na oddech. Warunkiem wstępnym masażu serca jest stałe monitorowanie jego skuteczności. Kryteria skuteczności masażu należy rozpatrywać w następujący sposób. 1. Zmiana koloru skóry: staje się mniej blada, szara, sinicza. 2. Zwężenie źrenic, jeśli były rozszerzone, z pojawieniem się reakcji na światło. 3. Pojawienie się impulsu tętna na tętnicach szyjnych i udowych, a czasem na tętnicy promieniowej. 4. Oznaczanie ciśnienia krwi na poziomie 60-70 mm Hg. Sztuka. mierzona na ramieniu. 5. Czasami pojawienie się niezależnych ruchów oddechowych. 12. Wprowadzenie leków. Rejestracja EKG D - Narkotyki - wprowadzenie narkotyków. W przypadku ostrego ustania krążenia krwi wprowadzenie środków stymulujących czynność serca należy rozpocząć tak szybko, jak to możliwe, w razie potrzeby powtórzyć podczas resuscytacji. Po rozpoczęciu masażu serca należy jak najszybciej podać 0,5-1 ml adrenaliny (dożylnie lub dotchawiczo). Jego wielokrotne wprowadzenie jest możliwe po 2-5 minutach (łącznie do 5-6 ml). Przy asystolii adrenalina tonizuje mięsień sercowy i pomaga „uruchomić” serce, przy migotaniu komór przyczynia się do przejścia z migotania małych fal w duże, co znacznie ułatwia defibrylację. Adrenalina ułatwia wieńcowy przepływ krwi i zwiększa kurczliwość mięśnia sercowego. Zamiast epinefryny można zastosować izodrynę, która jest 3 razy skuteczniejsza od adrenaliny pod względem skuteczności działania na mięsień sercowy. Dawka początkowa wynosi 1-2 ml we wstrzyknięciu dożylnym, a kolejne 1-2 ml w 250 ml 5% roztworu glukozy. W warunkach upośledzonego krążenia krwi kwasica metaboliczna stopniowo wzrasta, dlatego bezpośrednio po wlewie adrenaliny podaje się dożylnie 4-5% roztwór wodorowęglanu sodu w ilości 3 ml/kg masy ciała pacjenta. W procesie umierania ton przywspółczulnego układu nerwowego znacznie wzrasta, mózg jest wyczerpany, dlatego stosuje się M-cholinolityki. W asystolii i bradykardii atropinę podaje się dożylnie w 0,1% roztworze - 0,5-1 ml, do maksymalnej dawki 3-4 ml. Aby zwiększyć napięcie mięśnia sercowego i zmniejszyć efekt hiperkaliemii, zaleca się dożylne podanie 5 ml 10% roztworu chlorku wapnia. Adrenalinę, atropinę i chlorek wapnia można podawać razem w tej samej strzykawce. W przypadku ciężkiej tachykardii, a zwłaszcza z rozwojem migotania, wskazane jest stosowanie lidokainy w dawce 60-80 mg, ale ponieważ jest ona krótkodziałająca, podaje się ją w infuzji z szybkością 2 mg / min. Wskazane jest również stosowanie glikokortykoidów, które poprzez zwiększenie wrażliwości adrenoreaktywnych struktur mięśnia sercowego na katecholaminy oraz normalizację przepuszczalności błon komórkowych przyczyniają się do przywrócenia prawidłowej czynności serca. E - Elektrokardiografia - rejestracja EKG Za pomocą badania EKG określa się charakter naruszenia czynności serca. Najczęściej może to być asystolia - całkowite ustanie skurczów serca, migotanie - chaotyczny nieskoordynowany skurcz włókien mięśnia sercowego z częstotliwością 400-500 uderzeń / min, w którym pojemność minutowa serca praktycznie się zatrzymuje. Początkowo obserwuje się migotanie dużych fal, które w ciągu 1-2 minut przechodzi w migotanie małych fal, a następnie asystolię. Obecność jakiegokolwiek rytmu w EKG jest lepsza niż całkowity brak aktywności elektrycznej mięśnia sercowego. Dlatego kluczowym zadaniem RKO jest pobudzenie aktywności elektrycznej mięśnia sercowego, a następnie przekształcenie jej w efektywny (obecność pulsu) rytm. 13. Defibrylacja elektryczna F - Fibrylacja - przeprowadzenie w razie potrzeby defibrylacji elektrycznej (kardiowersji) Migotanie serca można wyeliminować za pomocą defibrylacji elektrycznej. Konieczne jest ścisłe przyłożenie elektrod do klatki piersiowej (w pozycji przednio-bocznej jedna elektroda znajduje się w okolicy wierzchołka serca, druga w okolicy podobojczykowej po prawej stronie mostka), co zwiększa siłę nacisku rozładowanie i, odpowiednio, skuteczność defibrylacji. U wielu pacjentów bardziej skuteczne jest przednio-tylne (wierzchołek serca - przestrzeń międzyłopatkowa) elektrod. Nie nakładaj elektrod na nakładki monitora EKG. Należy zauważyć, że defibrylacja elektryczna jest skuteczna tylko wtedy, gdy w EKG rejestrowane są oscylacje wielkofalowe o amplitudzie od 0,5 do 1 mV lub większej. Ten rodzaj migotania mięśnia sercowego wskazuje na bezpieczeństwo jego zasobów energetycznych i możliwość przywrócenia odpowiedniej czynności serca. Jeśli oscylacje są niskie, arytmiczne i polimorficzne, co obserwuje się w ciężkim niedotlenieniu mięśnia sercowego, wówczas możliwość przywrócenia czynności serca po defibrylacji jest minimalna. W tym przypadku za pomocą masażu serca, wentylacji mechanicznej, dożylnego podawania adrenaliny, atropiny, chlorku wapnia konieczne jest osiągnięcie przejścia migotania na fale wielkofalowe, a dopiero po tym należy wykonać defibrylację. Pierwsza próba defibrylacji wykonywana jest przy wyładowaniu 200 J, przy kolejnych próbach ładunek wzrasta do 360 J. Elektrody należy zwilżyć i mocno docisnąć do powierzchni klatki piersiowej. Do najczęstszych błędów podczas defibrylacji, które powodują nieskuteczność tej ostatniej, należą: 1. Długie przerwy w masażu serca lub całkowity brak resuscytacji podczas przygotowania defibrylatora do wyładowania. 2. Luźny docisk lub niedostateczne zwilżenie elektrod. 3. Zastosowanie wyładowania na tle migotania o niskiej długości fali bez podejmowania działań zwiększających zasoby energetyczne mięśnia sercowego. 4. Zastosowanie wyładowania o niskim lub zbyt wysokim napięciu. Należy zauważyć, że defibrylacja elektryczna serca jest skuteczną metodą korygowania takich zaburzeń rytmu serca jak napadowy częstoskurcz komorowy, trzepotanie przedsionków, częstoskurcz węzłowy i nadkomorowy, migotanie przedsionków. Wskazaniem do defibrylacji elektrycznej na etapie przedszpitalnym jest najczęściej napadowy częstoskurcz komorowy. Cechą defibrylacji w tych warunkach jest obecność świadomości pacjenta i konieczność wyeliminowania reakcji na ból podczas stosowania wyładowania elektrycznego. 14. Intensywna opieka nad zespołami poresuscytacyjnymi I-Intensywna terapia – intensywna opieka w zespołach poresuscytacyjnych 1. Korekta CBS i równowagi wodno-elektrolitowej. Często po RKO rozwija się zasadowica metaboliczna, hipokaliemia, hipochloremia i inne zaburzenia elektrolitowe. Następuje zmiana pH do środowiska kwaśnego lub zasadowego. Kluczem do korekcji pH jest odpowiednia wentylacja. Stosowanie wodorowęglanu powinno odbywać się pod kontrolą składu gazu we krwi. Z reguły nie ma potrzeby wprowadzania HCO3 z szybkim przywróceniem krążenia krwi i oddychania. Przy sprawnym sercu poziom pH ~7,15 jest odpowiedni dla funkcjonowania układu sercowo-naczyniowego. 2. Normalizacja systemu obrony antyoksydacyjnej. Intensywna terapia obejmuje kompleks leków przeciwutleniających o wielokierunkowym działaniu - mafusol, unitiol, witamina C, multibiont, tokoferol, probucol itp. 3. Stosowanie antyoksydantów przyczynia się do zmniejszenia intensywności procesów metabolicznych, a co za tym idzie, zmniejszenia zapotrzebowania na tlen i energię, a także maksymalnego wykorzystania zmniejszonej ilości tlenu dostępnego podczas hipoksji. Osiąga się to poprzez stosowanie leków neurowegetatywnych i przeciw niedotlenieniu (seduxen, droperydol, blokery zwojów, meksamina, oksymaślan sodu, cytochrom, gutimina itp.). 4. Zwiększenie zasobów energetycznych zapewnia dożylne podawanie stężonych roztworów glukozy z insuliną i głównymi koenzymami zaangażowanymi w wykorzystanie energii (witamina B6, kokarboksylaza, ATP, ryboksyna itp.). 5. Stymulacja syntezy białek i kwasów nukleinowych - substratów absolutnie niezbędnych do prawidłowego funkcjonowania komórek, syntezy enzymów, immunoglobulin i innych, odbywa się przy użyciu hormonów anabolicznych (retabolil, nerabolil, insulina, retinol ), kwas foliowy, a także wprowadzenie roztworów aminokwasów. 6. Aktywacja metabolizmu tlenowego osiągana jest poprzez wprowadzenie wystarczającej ilości substratów utleniania (glukozy), a także zastosowanie hiperbolicznego natleniania (HBO) - ta metoda zapewnia dostarczenie wymaganej ilości tlenu nawet w warunkach ostrych naruszeń jego dostarczania . 7. Usprawnienie procesów redoks (kwas bursztynowy, ryboksyna, tokoferol itp.). 8. Aktywna terapia detoksykacyjna przyczynia się do normalizacji procesów metabolicznych. W tym celu stosuje się różne metody terapii infuzyjnej (żelatynol, albumina, osocze), wymuszoną diurezę itp. W ciężkich przypadkach stosuje się pozaustrojowe metody detoksykacji (hemosorpcja, hemodializa, plazmafereza). 9. Eliminacja naruszeń procesów mikrokrążenia. W tym celu wykonuje się terapię heparyną. 15. Skurcz krtani Skurcz krtani to zamknięcie prawdziwych i fałszywych strun głosowych. W obu przypadkach koniecznie stosuje się środki kontrolne (eufillin). Jeśli to nie pomaga, należy wprowadzić krótko działające środki zwiotczające mięśnie, zaintubować i przenieść pacjenta na wentylację mechaniczną. Środki zwiotczające mięśnie powodują niewydolność oddechową w okresie pooperacyjnym, jeśli nie zostanie wykonana wystarczająca dekuraryzacja. Jest zwykle wytwarzany przez leki antycholinesterazowe (prozerin). Do czasu ekstubacji należy upewnić się, że siła i napięcie mięśniowe powróciły (poproś o podniesienie ręki, ściśnięcie ręki, podniesienie głowy). Przy wielu złamaniach żeber część klatki piersiowej zapada się podczas wdechu, rozwija się tak zwany oddech paradoksalny, dlatego konieczne jest przywrócenie klatki piersiowej. U tego pacjenta konieczna jest intubacja, po wprowadzeniu środków zwiotczających, z dalszym przejściem na wentylację mechaniczną (do przywrócenia integralności klatki piersiowej). Do zmniejszenia czynności miąższu płucnego prowadzą: niedodma, zapaść płuca, zapalenie płuc, następstwa operacji, odma płucna, hemoroidalna, ropotokowa. Różnice między niedodmą a zapaścią: niedodma jest przeszkodą w stanie wyprostowanym. Ten stan charakteryzuje się obecnością niewentylowanego płuca, przez które przepływa połowa krwi krążącej, ta ostatnia nie jest natleniona. W rezultacie rozwija się ostra niewydolność oddechowa. Kiedy płuco zapada się, jest ono ściskane przez powietrze lub płyn w jamie opłucnej. W tym samym czasie krążenie krwi w skompresowanym płucu gwałtownie spada, a krążenie krwi w zdrowym płucu wzrasta. Dlatego zapaść nie jest tak groźnym powikłaniem w zakresie rozwoju ostrej niewydolności oddechowej jak niedodma. Przed zabiegiem należy ocenić funkcję nienaruszonego płuca (oddzielna spirografia). Zgodnie z etapem rozwoju ostrą niewydolność oddechową dzieli się na: 1) dysfunkcja; 2) niewydolność; 3) brak funkcji protetycznej. Zgodnie z tempem rozwoju ostrą niewydolność oddechową dzieli się na: 1) błyskawicznie (rozwija się w ciągu minuty); 2) ostry (rozwija się w ciągu kilku godzin); 3) podostry (rozwija się w ciągu kilku dni); 4) przewlekły (trwa latami). Główne elementy intensywnej terapii w ostrej niewydolności oddechowej: tlenoterapia, drenaż pacjenta, fibrobronchoskopia, tracheostomia, intubacja i wentylacja mechaniczna, rozszerzenie oskrzeli, terapia hormonalna, HBO. 16. Zator płucny Zatorowość płucna (ZP) to zablokowanie głównego lub środkowego tułowia, małych pni naczyniowych tętnicy płucnej, prowadzące do wzrostu ciśnienia w krążeniu płucnym, niewydolności prawej komory. Kliniczna klasyfikacja PE Forma: ciężka, średnia i lekka. Downstream: piorunujący, ostry, nawracający. W zależności od stopnia uszkodzenia tętnicy płucnej: pień lub główne gałęzie, gałęzie płatowe (odcinkowe), małe gałęzie. Przebieg kliniczny PE jest dość zmienny. Najczęstsze objawy to nagły początek duszności (RR waha się od 30 do ponad 50 na minutę), przyspieszony oddech, bladość, częściej sinica, obrzęk żył szyjnych, tachykardia, niedociśnienie tętnicze (do wstrząsu), zamostkowa ból, kaszel i krwioplucie. Osłuchiwanie często warunkuje wzmocnienie tonu II nad tętnicą płucną. Objawy rentgenowskie - wzrost wielkości proksymalnej tętnicy płucnej, wyczerpanie wzoru obwodowego, a także podniesienie kopuły przepony. EKG może ujawnić przeciążenie prawych oddziałów (cor pulmonale): 1) pojawienie się fal Q z jednoczesnym wzrostem amplitudy fal R i S (zespół QS); 2) obrót serca wokół osi podłużnej z prawą komorą do przodu (przesunięcie strefy przejściowej do lewych odprowadzeń klatki piersiowej); 3) uniesienie odcinka ST z ujemną falą w odprowadzeniach III, aUR, V1-V3; 4) pojawienie się lub zwiększenie stopnia blokady prawej nogi wiązki Jego; 5) wysoki spiczasty „płucny” ząb P z odchyleniem jego osi elektrycznej w prawo; 6) częstoskurcz zatokowy lub częstoskurczowa postać migotania przedsionków. Echokardiografia pozwala na wykrycie ostrego serca płucnego, określenie stopnia zaawansowania nadciśnienia w krążeniu płucnym, ocenę stanu strukturalnego i funkcjonalnego prawej komory, wykrycie zatorowości w jamach serca i głównych tętnicach płucnych, uwidocznienie otwartego otworu owalnego, który może nasilenia zaburzeń hemodynamicznych i być przyczyną zatorowości paradoksalnej. Jednak ujemny wynik badania echokardiograficznego w żadnym wypadku nie wyklucza rozpoznania zatorowości płucnej. Najbardziej informacyjną metodą diagnostyczną jest angiografia tętnic płucnych. Leczenie 1. Terapia przeciwzakrzepowa. 2. Terapia trombolityczna. 3. Leczenie chirurgiczne. 17. Leczenie doraźne stanu astmatycznego Terapia tlenowa. Zwilżony tlen jest wdychany2przez cewniki donosowe lub przez maskę z szybkością 1-2 l / min. Adrenalina pobudza α1-, β., - i β2-receptory adrenergiczne, rozszerzają oskrzela i zmniejszają opór dróg oddechowych. Eufillin hamuje fosfodiesterazę, która przyczynia się do akumulacji cyklicznego AMP i usuwania skurczu oskrzeli. Przepisując aminofilinę, należy wziąć pod uwagę przeciwwskazania, w tym palenie i dzieciństwo, niewydolność serca i ostry zespół wieńcowy, przewlekłe choroby płuc, wątroby i nerek. W przypadku AS dawka nasycająca aminofiliny wynosi 3-6 mg/kg, podaje się ją dożylnie w ciągu 20 minut. Następnie przeprowadzić konserwację wlewu kroplowego leku. Efekt terapii kortykosteroidami związany jest z tłumieniem zapalenia dróg oddechowych i zwiększoną wrażliwością na leki β-adrenergiczne. Im cięższy AS, tym większe wskazanie do natychmiastowej terapii kortykosteroidami. Początkowo należy podać dużą dawkę kortykosteroidów. Jeśli terapia jest nieskuteczna, dawkę zwiększa się. Przynajmniej co 6 godzin podaje się odpowiednie równoważne dawki tych leków. Większości pacjentów pokazano terapię inhalacyjną za pomocą b - adrenomimetyków; (fenoterol, alupent, salbutamol). Wyjątkiem są przypadki przedawkowania leków sympatykomimetyków. Jeżeli trwająca terapia nie daje efektu, wskazane jest dożylne podanie agonistów β-adrenergicznych, takich jak izoproterenol, rozcieńczony w 5% roztworze glukozy. Przeciwwskazaniami są choroby serca (miażdżyca naczyń wieńcowych, zawał mięśnia sercowego), ciężki tachykardia i objawy tachyfilaksji, podeszły wiek. Szybkość podawania izoproterenolu wynosi 0,1 μg / kg na 1 min do początku tachykardii (HR 130 na 1 min lub więcej). Terapia infuzyjna jest najważniejszym elementem leczenia AS, mającym na celu uzupełnienie niedoboru płynów i wyeliminowanie hipowolemii, całkowita objętość terapii infuzyjnej wynosi 3-5 litrów na dobę. Hydratację przeprowadza się poprzez wprowadzenie roztworów zawierających wystarczającą ilość wolnej wody (roztwory glukozy), a także hipo- i izotonicznych roztworów elektrolitów zawierających sód i chlor. Wskaźnikami odpowiedniego nawodnienia są ustanie pragnienia, mokry język, przywrócenie prawidłowej diurezy, lepsze opróżnianie plwociny i spadek hematokrytu do 0,30-0,40. Znieczulenie halotanem może być stosowane w leczeniu ciężkiego ataku astmy, który nie jest podatny na konwencjonalną terapię. Sztuczna wentylacja płuc. Wskazania do przeniesienia chorych z AS do wentylacji mechanicznej powinny być bardzo surowe, gdyż w tym stanie często powoduje powikłania i charakteryzuje się dużą śmiertelnością. Jednocześnie wentylacja mechaniczna, prowadzona według ścisłych wskazań, jest jedyną metodą, która może zapobiec dalszemu postępowi hipoksji i hiperkapnii. 18. Zawał mięśnia sercowego Zawał mięśnia sercowego to rozbieżność między zapotrzebowaniem mięśnia sercowego na tlen a jego dostarczaniem, skutkująca ograniczoną martwicą mięśnia sercowego. Najczęstszą przyczyną jest zakrzep, rzadziej zator, rzadziej skurcz tętnic wieńcowych. Zakrzepicę najczęściej obserwuje się na tle miażdżycowego uszkodzenia tętnic wieńcowych. Klasycznie zawał mięśnia sercowego zaczyna się od narastającego bólu za mostkiem, który z natury jest palący i uciskający. Charakteryzuje się rozległym napromieniowaniem bólu ramion (najczęściej po lewej), pleców, brzucha, głowy, pod lewą łopatką, w lewej żuchwie itp. Pacjenci są niespokojni, niespokojni, czasami zauważają uczucie lęku przed śmierć. Występują oznaki niewydolności serca i naczyń - zimne kończyny, lepki pot itp. Zespół bólowy jest przedłużony i nie ustępuje pod wpływem nitrogliceryny przez 30 minut lub dłużej. Występują różne zaburzenia rytmu serca, spadek ciśnienia krwi lub jego wzrost. Pacjenci subiektywnie odnotowują uczucie braku powietrza. Powyższe objawy są typowe dla okresu I - bolesnego lub niedokrwiennego, których czas trwania waha się od kilku godzin do 2 dni. Obiektywnie wzrost ciśnienia krwi (wtedy spadek); zwiększona częstość akcji serca lub zaburzenia rytmu; podczas osłuchiwania słychać nieprawidłowy ton IV; dźwięki serca są stłumione; na akcent aorty II ton; praktycznie nie ma zmian biochemicznych we krwi, charakterystycznych znaków na EKG. Drugi okres jest ostry (gorączkowy, zapalny), charakteryzujący się występowaniem martwicy mięśnia sercowego w miejscu niedokrwienia. Ból zwykle ustępuje. Czas trwania ostrego okresu wynosi do 2 tygodni. Stan pacjenta stopniowo się poprawia, ale utrzymuje się ogólne osłabienie, złe samopoczucie i tachykardia. Dźwięki serca są stłumione. Podwyższenie temperatury ciała spowodowane procesem zapalnym mięśnia sercowego, zwykle niewielkie, do 38°C, pojawia się zwykle w 3. dniu choroby. Pod koniec pierwszego tygodnia temperatura zwykle wraca do normy. Trzeci okres (podostry lub bliznowacenie) trwa 4-6 tygodni. Charakterystyczne dla niego jest normalizacja parametrów krwi (enzymów), normalizuje się temperatura ciała, znikają wszystkie inne oznaki ostrego procesu: zmiany EKG, blizna tkanki łącznej rozwija się w miejscu martwicy. Czwarty okres (okres rehabilitacji, rekonwalescencji) trwa od 6 miesięcy do 1 roku. Brak objawów klinicznych. W tym okresie dochodzi do kompensacyjnego przerostu nienaruszonych włókien mięśnia sercowego i rozwijają się inne mechanizmy kompensacyjne. Następuje stopniowe przywracanie funkcji mięśnia sercowego. Ale patologiczna fala Q utrzymuje się na EKG. Leczenie ma na celu zapobieganie powikłaniom, ograniczenie strefy zawałowej, łagodzenie bólu i korekcję niedotlenienia. 19. Wstrząs kardiogenny Wstrząs kardiogenny jest krytycznym zaburzeniem krążenia z niedociśnieniem tętniczym i objawami ostrego pogorszenia krążenia krwi w narządach i tkankach. Głównym objawem diagnostycznym jest znaczne obniżenie skurczowego ciśnienia krwi, które wynosi poniżej 90 mm Hg. Sztuka. Różnica między ciśnieniem skurczowym i rozkurczowym (ciśnienie tętna) wynosi 20 mm Hg. Sztuka. lub jeszcze mniejsze. Ponadto rozwija się klinika gwałtownego pogorszenia perfuzji narządów i tkanek: 1) zaburzenia świadomości od łagodnego letargu do psychozy lub śpiączki, mogą pojawić się ogniskowe objawy neurologiczne; 2) diureza poniżej 20 ml/h. Objawy pogorszenia krążenia obwodowego: blada sinica, marmurkowata, ceglasta, wilgotna skóra; zapadnięte żyły obwodowe, gwałtowny spadek temperatury skóry dłoni i stóp; zmniejszenie przepływu krwi. Wartość CVP może być różna. Normalne wskaźniki CVP to 5-8 cm wody. Sztuka.; wskaźnik poniżej 5 cm wody. Sztuka. wskazuje na hipowolemię i niskie ciśnienie krwi oraz powyżej 8 cm wody. Sztuka. wskazuje na niewydolność prawej komory. Leczenie Wskazana jest terapia tlenowa nawilżonym tlenem przez maskę lub cewniki donosowe. Bolesne podawanie leków przeciwzakrzepowych w dawce 10 000 IU, a następnie dożylny infusomat 1000 IU na godzinę. Konieczne jest podanie leków przeciwbólowych: morfina 1% 1,0 ml podskórnie lub dożylnie w bolusie; analgin 50% 2 ml domięśniowo, dożylnie. Toniki naczyniowe: Cordiamin 1-4 ml dożylnie; mezaton 1% 1,0 g podskórnie, dożylnie, w soli fizjologicznej; norepinefryna 0,2% 1,0 g dożylnie. Prawdziwy wstrząs kardiogenny jest traktowany w następujący sposób. W celu zwiększenia aktywności skurczowej mięśnia sercowego stosuje się: strofantynę 0,05% 0,5-0,75 g dożylnie powoli na 20,0 roztwór izotoniczny, korglukon 0,01 g dożylnie, również w roztworze izotonicznym lub mieszaninie polaryzacyjnej, glukagon 2-4 mg dożylnie kroplówka na roztwór polaryzacyjny. Normalizacja ciśnienia krwi: norepinefryna 0,2% 2-4 ml na 1 litr 5% roztworu glukozy lub roztworu izotonicznego. Ciśnienie krwi utrzymuje się na poziomie 100 mm Hg. Art., mezaton 1% 1,0 g dożylnie; kordiamina 2-4 ml, dopamina 200 mg w 400 ml reopolyglucyny lub 5% glukozy. Przy niestabilnym działaniu powyższych leków stosuje się hydrokortyzon 200 mg, prednizolon 90-120 mg. Normalizacja właściwości reologicznych krwi. Eliminacja hipowolemii, ponieważ występuje pocenie się płynnej części krwi: reopoliglyukin, polyglukin - w objętości do 100 ml z szybkością 50,0 ml na minutę. Korekta równowagi kwasowo-zasadowej (zwalczanie kwasicy): wodorowęglan sodu 5% do 200,0 ml. Ponowne wprowadzenie środków przeciwbólowych. Przywracanie zaburzeń rytmu i przewodzenia. 20. Kryzys nadciśnieniowy Przełom nadciśnieniowy to nagły wzrost ciśnienia krwi do poziomu, który zwykle nie jest charakterystyczny dla tego pacjenta, prowadzący do ostrych regionalnych zaburzeń krążenia i uszkodzenia narządów docelowych (serca, mózgu, nerek, jelit). Czynnikami zewnętrznymi wywołującymi kryzys mogą być: 1) stres psychoemocjonalny; 2) wpływy meteorologiczne; 3) nadmierne spożycie soli kuchennej. Objawy kliniczne kryzysu objawiają się hałasem w uszach migające muchy przed oczami, pękający ból głowy w okolicy potylicznej, pogarszany przez pochylanie się, napinanie, kaszel, nudności, wymioty, zaburzenia rytmu serca. Podczas kryzysu dochodzi do niebezpiecznych naruszeń wieńcowych mózgu, rzadziej krążenia nerkowego i brzusznego, co prowadzi do udaru, zawału mięśnia sercowego i innych poważnych powikłań. EKG ujawnia przerost lewej komory. RTG klatki piersiowej pokazuje powiększenie serca, deformację aorty w postaci cyfry „3”, lichwę żeber w wyniku zwiększonego pobocznego przepływu krwi przez tętnice międzyżebrowe. Aortografia potwierdza diagnozę. Postać neurowegetatywna kryzysu charakteryzuje się nagłym początkiem, pobudzeniem, przekrwieniem i wilgocią skóry, tachykardią, częstym obfitym oddawaniem moczu, dominującym wzrostem ciśnienia skurczowego ze wzrostem amplitudy tętna. Takie kryzysy są inaczej nazywane kryzysami nadnerczy lub kryzysami typu I. Kryzysy typu I mają zwykle stosunkowo łagodny przebieg, chociaż mogą prowadzić do napadowych zaburzeń rytmu serca lub dusznicy bolesnej, aw ciężkich przypadkach do zawału mięśnia sercowego. W przypadku kryzysu w postaci soli wodno-solnej stan pogarsza się stopniowo, obserwuje się senność, osłabienie, letarg, dezorientację, bladość i obrzęk twarzy oraz obrzęk. Ciśnienie skurczowe i rozkurczowe wzrasta równomiernie lub z przewagą tego ostatniego i spadkiem ciśnienia tętna. Takie kryzysy nazywane są kryzysami typu II. Kryzysy typu II są z reguły ciężkie i mogą być powikłane zawałem mięśnia sercowego, udarem mózgu, ostrą niewydolnością lewej komory. Konieczne jest podkreślenie kryzysów nadciśnieniowych, które powstają w wyniku nagłego zaprzestania trwałej terapii hipotensyjnej, w szczególności przyjmowania β-blokerów, nifedypiny, leków sympatykolitycznych, a zwłaszcza klonidyny. Leczenie przełomu nadciśnieniowego polega na nagłym obniżeniu ciśnienia krwi do normalnego poziomu, niezbędnym do zapobiegania lub ograniczania uszkodzeń narządów docelowych w nadciśnieniu, w celu zapobiegania powikłaniom aż do śmierci w najcięższych przypadkach lub trwałej niepełnosprawności w rozwoju udaru mózgu , zawał mięśnia sercowego. 21. Arytmia. Paroksyzm migotania przedsionków Arytmia to rytm serca inny niż zatokowy. Klasyfikacja arytmii 1. Naruszenie powstawania impulsów: 1) w węźle zatokowym: a) częstoskurcz zatokowy; b) bradykardia zatokowa; c) arytmia zatokowa; d) zespół chorej zatoki (SSS); 2) ektopowe arytmie: a) ekstrasystolia; b) częstoskurcz napadowy; c) migotanie i trzepotanie przedsionków; d) migotanie i trzepotanie komór. 2. Naruszenie przewodzenia impulsów: 1) dodatkowe ścieżki (pakiety Kent); 2) blok serca: a) przedsionkowy (wewnątrzprzedsionkowy); b) przedsionkowo-komorowy; c) dokomorowe. Mechanizmy występowania arytmii Spadek potencjału spoczynkowego, próg pobudliwości występuje tylko na podstawie niedoboru komórkowego potasu, stosunek „osocze – komórka” (normalnie 80 meq potasu znajduje się w komórce i 5 meq w osoczu). Asymetria ogniska elektrofizjologiczno-metabolicznego mięśnia sercowego z powodu niedokrwienia, zapalenia, reperfuzji podczas trombolizy. Osłabienie elektrofizjologiczne stymulatora górnego. Wrodzone dodatkowe ścieżki przewodzenia. Napadowy częstoskurcz nadkomorowy to nagły atak bicia serca z częstotliwością 150-250 uderzeń na minutę. Istnieją 3 formy: 1) przedsionkowy; 2) węzłowy; 3) komorowy. Etiologia częstoskurczu napadowego nadkomorowego jest częściej związana ze wzrostem aktywności współczulnego układu nerwowego. Klinicznie objawia się nagłym atakiem bicia serca, naczynia szyi pulsują, czynność serca przechodzi w inny rytm. Czas trwania ataku wynosi od kilku minut do kilku dni. Liczba uderzeń serca w postaci komorowej mieści się zwykle w zakresie 150-180 uderzeń na minutę, przy formach nadkomorowych - 180-240 uderzeń na minutę. Podczas ataku rytm wahadłowy jest charakterystyczny osłuchowo, nie ma różnicy między tonem I i II. Zwiększa zapotrzebowanie mięśnia sercowego na tlen i może wywołać atak ostrej niewydolności wieńcowej. Znaki EKG 1. Zespoły QRS nie ulegają zmianie. 2. W formie nadkomorowej fala P łączy się z T. 22. Dodatkowy skurcz komorowy. Zaburzenia przewodzenia AV Ekstrasystolia komorowa to wystąpienie niezwykle szerokiego zdeformowanego zespołu QRS, niezgodności przesunięcia odcinka ST i T, pełna pauza kompensacyjna (odstęp między przed- i po ekstrasystolicznym załamku P jest równy dwukrotności normalnego odstępu RR). Lekem z wyboru jest lidokaina, którą podaje się zgodnie z powyższym schematem. Być może zastosowanie cordaronu w dawce 300-450 mg dożylnie w kroplówce. Naruszenie przewodzenia AV wraz z rozwojem omdleń (zespół Morgagni-Adams-Stokes) Gdy przewodnictwo jest zaburzone, dochodzi do różnego rodzaju blokad serca, następuje spowolnienie lub całkowite ustanie przewodzenia impulsu przez układ przewodzący serca. Blokada zatokowo-uszna charakteryzuje się dysfunkcją limfocytów T i upośledzeniem przewodzenia impulsów z węzła zatokowego do przedsionków. Istnieją 3 stopnie. I stopień - spowolnienie impulsu. Na EKG - wydłużenie odstępu PQ o ponad 0,20 s. Wypadanie zespołu QRS. Odstęp RR jest stabilny. II stopień - utrata części impulsów, niepełne przewodzenie. Mobitz typu I - w miarę przechodzenia impulsów odstęp PQ stopniowo wydłuża się aż do całkowitego zaniku fali tętna. QRS nie ulega zmianie. W miejscu wypadnięcia zespołu QRS największa odległość to RR. Prognostycznie ten typ jest stosunkowo korzystny. Mobitz typu II ze stałym odstępem PQ i niezmienionym zespołem QRS. Jednocześnie nie wszystkie impulsy docierają do komór - w niektórych przypadkach realizowany jest co drugi impuls, w innych - co trzeci itd., czyli występuje okresowe wypadanie zespołu QRS 3:2, 4:3 , 5:6 itd. re. III stopień - całkowita blokada przewodzenia. Jednocześnie przewodzenie impulsów do komór zostaje całkowicie zatrzymane, aw komorach rodzi się heterotopowe ognisko rytmu idiokomorowego, a im niższy automatyzm, tym trudniejsza klinika. Obserwuje się całkowitą dysocjację: rytm przedsionkowy jest zbliżony do normalnego, a komory mają własną częstotliwość - 40 uderzeń na minutę lub mniej. Ta ostatnia zależy od poziomu uszkodzenia: jeśli cierpi węzeł AV, 40-50 uderzeń na 1 minutę, jeśli odnoga wiązki Jego - 20 uderzeń na 1 minutę lub mniej. Na poziom uszkodzenia wskazuje również stopień deformacji zespołu QRS. Dźwięki serca są osłabione, okresowo pojawia się ton "armaty", gdy skurcz przedsionków i komór prawie pokrywa się w czasie. Może być III dodatkowym tonem. U podstawy serca mogą pojawić się skurczowe szmery wyrzutowe. Często występuje pulsacja żył związana ze skurczem przedsionków, szczególnie wyraźna przy tonie działa Strazhesko. Klinika Awaria serca, jeśli jeden impuls wypadnie. Zawroty głowy, jeśli wypadnie kilka impulsów. Zespół Morgagni-Adams-Stokes (utrata przytomności), jeśli wypadnie 6-8 kompleksów. Leczenie Aby przywrócić odpowiedni rytm, atropinę podaje się w dawce od 0,5-1 mg do 3 mg. Co 3 minuty 1 mg do całkowitej dawki 0,4 mg/kg. Antagoniści wapnia - izoptyna 0,04 mg/kg. Przy częstej utracie przytomności pacjent zostaje przeniesiony na stałą terapię elektropulsową. Częściej jednak stymulacja musi odbywać się „na żądanie”. 23. Przyczyny ostrej niewydolności nerek Ostra niewydolność nerek (ARF) jest powikłaniem szeregu chorób nerek i pozanerkowych, charakteryzujących się ostrym pogorszeniem lub ustaniem czynności nerek i objawiającymi się następującym zespołem objawów: oligonuria, azotemia, przewodnienie, upośledzenie CBS i równowagi wodno-elektrolitowej. Formy OOP obejmują: 1) przednerkowe (hemodynamiczne); 2) nerkowy (miąższowy); 3) zanerkowe (obturacyjne); 4) arena. Przyczyny rozwoju przednerkowej ostrej niewydolności nerek. 1. Zmniejszona pojemność minutowa serca (wstrząs kardiogenny, napadowe zaburzenia rytmu serca, tamponada serca, zator tętnicy płucnej, zastoinowa niewydolność serca). 2. Zmniejszone napięcie naczyniowe (posocznica, wstrząs toksyczny zakaźny, wstrząs anafilaktyczny, przedawkowanie leków hipotensyjnych). 3. Zmniejszona efektywna objętość wewnątrznaczyniowa (utrata krwi, utrata osocza, odwodnienie – utrata 7-10% masy ciała). 4. Naruszenie hemodynamiki wewnątrznerkowej (przyjmowanie NLPZ, inhibitorów ACE, leków nieprzepuszczających promieniowania, sandimmunizacyjnych). 5. Zatrucie wodne - przewodnienie (niekontrolowane wytwarzanie ADH w nowotworach złośliwych, choroby zapalne ośrodkowego układu nerwowego, przedawkowanie leków - leki, barbiturany, przeciwcukrzycowe leki sulfanilamidowe, indometacyna, amitryptylina, cyklofosfamid). Przyczyny rozwoju ostrej niewydolności nerek. 1. Niedokrwienie nerki. 2. Nefrotoksyczne uszkodzenie spowodowane narażeniem na: 1) leki (aminoglikozydy, NLPZ, leki nieprzepuszczające promieniowania itp.); 2) nefrotoksyny przemysłowe (sole metali ciężkich); 3) nefrotoksyny domowe (glikol etylenowy, alkohol metylowy, dichloroetan, czterochlorek węgla). 3. Niedrożność wewnątrzkanalikowa przez pigmenty: 1) hemoglobina; 2) moczan; 3) mioglobina; 4) procesy zapalne; 5) martwicze zapalenie brodawek (cukrzyca, nefropatia alkoholowa, przeciwbólowa); 6) patologia naczyniowa. Przyczyny rozwoju ostrej pozanerkowej niewydolności nerek. 1. Patologia moczowodów: 1) przeszkoda; 2) kompresja. 2. Patologia pęcherza. 3. Zwężenie cewki moczowej. 24. Klinika i leczenie ostrej niewydolności nerek W przebiegu klinicznym ostrej niewydolności nerek występuje pięć etapów. Etap I ostrej niewydolności nerek jest początkowy, trwa od momentu wystąpienia czynnika etiologicznego do pojawienia się pierwszych objawów. Na tym etapie taktyki terapeutyczne mają na celu wyeliminowanie lub złagodzenie wpływu czynnika etiologicznego: terapię przeciwwstrząsową, uzupełnienie BCC, zwalczanie niewydolności serca, terapię alkalizującą hemolizy wewnątrznaczyniowej, zwalczanie bólu, leczenie stanów septycznych itp. Wraz z etiologicznymi terapia, skurcz naczyń nerkowych jest eliminowany pod kontrolą diurezy godzinowej. Im wcześniej rozpocznie się stymulacja diurezy, tym korzystniejsze rokowanie. II stopień ostrej niewydolności nerek, czyli oligoanurii, charakteryzuje się dysfunkcją 70% nefronów. Wydalanie moczu mniejsze niż 500 ml na dzień wskazuje na rozwój skąpomoczu, a zmniejszenie do 50 ml na dzień lub mniej wskazuje na bezmocz. Oprócz upośledzonej zdolności nerek do wydalania wody, ucierpią także funkcje koncentracji i wydalania azotu. Ilość elektrolitów i azotu w moczu gwałtownie spada. Na tym etapie zachodzą najbardziej wyraźne zmiany w hemostazie. Leczenie powinno mieć na celu stałość środowiska wewnętrznego, aby zapewnić czas i możliwość regeneracji nabłonka nerek. Na skutek utraty elektrolitów podczas wymiotów i biegunki rozwija się stan przewodnienia. Dlatego konieczne jest stymulowanie diurezy, ale tylko pod kontrolą CVP. Popraw przepływ krwi przez nerki. Ponieważ konieczna jest ścisła kontrola diurezy, wykonuje się cewnikowanie pęcherza. Naruszenie funkcji nerek wydalania azotu prowadzi do azotemii, dlatego aby zmaksymalizować zapobieganie rozpadowi białek w organizmie, konieczne jest wprowadzenie wystarczającej ilości węglowodanów. Jeśli przebieg jest ciężki i nieuleczalny, wykonuje się sesje hemodializy. Jeśli czynnik etiologiczny zostanie usunięty, to po 5-7 dniach leczenia diureza zaczyna się zwiększać. Maksymalny czas trwania tego etapu to do 2 tygodni. III etap ostrej niewydolności nerek - wczesna wielomocz. Charakteryzuje się postępującym wzrostem diurezy (o 200-300 ml dziennie) do 3 litrów. Funkcje wydalania i koncentracji azotu w nerkach nie zostały jeszcze w pełni odzyskane, ale stężenie potasu, magnezu i fosforanów stopniowo się normalizuje. Intensywna terapia we wczesnej fazie wielomoczowej powinna obejmować te same środki, co w poprzedniej, z wyjątkiem stymulacji diurezy. Często wymagana jest hemodializa. Istnieje wysokie ryzyko odwodnienia. IV etap ostrej niewydolności nerek - późny wielomocz. Dzienny wzrost moczu sięga 500-1000 ml, a diureza może osiągnąć 8-10 litrów dziennie lub więcej. W nerkach zaczynają się regenerować procesy wymiany jonowej. Utrata potasu, magnezu, fosforu i innych elektrolitów gwałtownie wzrasta, pacjenci są narażeni na odwodnienie i demineralizację. Dlatego na tym etapie dożylnie podaje się elektrolity i płyny. Etap V OPN lub etap odzyskiwania. Funkcja koncentracji nerek zostaje przywrócona. Diureza zaczyna stopniowo spadać do normy (2-3 litry dziennie), a gęstość moczu wzrasta (1008-1028). 25. Ostra niewydolność wątroby Ostra niewydolność wątroby to zespół objawów charakteryzujący się naruszeniem jednej lub więcej funkcji wątroby z powodu ostrego lub przewlekłego uszkodzenia jej miąższu. Objawy kliniczne ARF są następujące. 1. Koagulopatia jest spowodowana niedoborem czynników krzepnięcia i wzrostem aktywności fibrynolitycznej. Predysponuje do samoistnych krwawień z błon śluzowych: można zaobserwować krwawienie z przewodu pokarmowego, macicy, nosa. Możliwe są krwotoki mózgowe. Aby ocenić stan układu hemostazy, określa się czas protrombinowy. 2. Hipoglikemia charakteryzuje się wysokim poziomem insuliny w osoczu, co wynika ze zmniejszenia jej wychwytu przez wątrobę. Prowadzi to do szybkiego pogorszenia stanu neurologicznego i śmierci pacjentów. 3. Naruszenia równowagi wodno-elektrolitowej i kwasowo-zasadowej. Schyłkowa ostra niewydolność nerek charakteryzuje się hiponatremią, hipofosfatemią, hipokalcemią i hipomagnezemią. Zmiana stanu kwasowo-zasadowego nie ma jednoznacznego kierunku. Zasadowicę oddechową związaną ze stymulacją ośrodka oddechowego substancjami toksycznymi można zastąpić kwasicą oddechową z powodu podwyższonego ciśnienia śródczaszkowego i zahamowania czynności oddechowej. W rozwoju śpiączki wątrobowej jako ciężkiego przebiegu choroby wyróżnia się stadia przedśpiączkowe, śpiączkę zagrażającą i śpiączkę właściwą. Występuje również śpiączka wątrobowokomórkowa (endogenna), będąca wynikiem masywnej martwicy miąższu, portokawalu (bypass, przeciek, egzogenna), z powodu znacznego wykluczenia wątroby z procesów metabolicznych z powodu obecności wyraźnych zespoleń portokawalnych, i śpiączka mieszana, występująca głównie w marskości wątroby. W okresie przedśpiączkowym rozwija się postępująca anoreksja, nudności, zmniejszenie wielkości wątroby, wzrost żółtaczki, hiperbilirubinemia i wzrost zawartości kwasów żółciowych we krwi. W przyszłości nasilają się zaburzenia neuropsychiczne, spowolnienie myślenia, depresja, a czasem euforia. Charakteryzuje się niestabilnością nastroju, drażliwością, zaburzenia pamięci, zaburzenia snu. Odruchy ścięgniste są zwiększone, charakterystyczne jest niewielkie drżenie kończyn. Rozwija się Azotemia. Dzięki szybkiej terapii pacjenci mogą wyjść z tego stanu, ale częściej przy ciężkich nieodwracalnych zmianach w wątrobie pojawia się śpiączka. W okresie śpiączki możliwe jest pobudzenie, które następnie zostaje zastąpione depresją (otępieniem) i postępującym upośledzeniem świadomości aż do jej całkowitej utraty. Rozwijają się zjawiska oponowe, odruchy patologiczne, niepokój ruchowy, drgawki. Oddychanie jest zaburzone (takie jak Kussmaul, Cheyne-Stokes); puls jest mały, arytmiczny; jest hipotermia. Twarz pacjenta jest wychudzona, kończyny zimne, z ust i skóry wydobywa się charakterystyczny słodki zapach wątroby, nasilają się zjawiska krwotoczne (krwotoki skórne, krwawienia z nosa, dziąseł, żylaki przełyku itp.). 26. Leczenie ostrej niewydolności wątroby Wczesne wsparcie inotropowe jest niezbędnym elementem intensywnej pielęgnacji. Zapobieganie powikłaniom infekcyjnym - wyznaczenie antybiotyków cefalosporynowych w połączeniu z lekami przeciwgrzybiczymi (amfoterycyna-B). Hepatoprotektory i leki stabilizujące błony: prednizolon do 300 mg, witamina C 500 mg, troxevasin 5 ml, etamsylan sodu 750 mg, Essentiale 30 ml, tokoferol 4 ml domięśniowo, cytomak 35 mg, kokarboksylaza 300 mg, kwas nikotynowy 30-40 mg, com-plamin 900 mg, sirepar 5-10 ml, kwas glutaminowy 1% 400 ml, vikasol 10 ml dożylnie, witaminy z grupy B. Inhibitory proteazy, które zawierają korowe 100 tys. szt., trasylol 400 tys. szt., antagonzan, go-dox. Stymulacja diurezy: reogluman 400 ml, mannitol, lasix do 200 mg dożylnie, eufillin 240 mg. W celu skorygowania koagulopatii stosuje się dożylne podawanie witaminy K (10 mg dziennie przez 3 dni). Efekt pojawia się po 3 h. W tym przypadku eliminacja hipoprotrombinemii związanej z zaburzeniami wchłaniania witaminy K, wynikającymi z niedoboru kwasów żółciowych. W przypadku krwawienia lub podejrzenia zabiegów inwazyjnych (cewnikowanie naczyń, dializa otrzewnowa) podaje się dożylnie masę płytkową lub świeżo mrożone osocze. Obrzęk mózgu jest częstą przyczyną śmierci. Mannitol podaje się w ilości 1 g/kg masy ciała. U pacjentów z niewydolnością nerek mannitol jest przepisywany w połączeniu z ultrafiltracją, aby uniknąć hiperosmolarności i przewodnienia. Wraz z rozwojem śpiączki wątrobowej przepisuje się chlorek potasu (0,4-0,5% roztwór w 5% roztworze glukozy o objętości 500 ml dożylnie) lub roztwór wodorowęglanu sodu (z kwasicą metaboliczną); Pacjenci oddychają nawilżonym tlenem przez cewnik donosowy. Wraz ze spadkiem ciśnienia tętniczego i żylnego poliglucynę i albuminę podaje się dożylnie. W przypadku wystąpienia masywnych krwawień podejmuje się odpowiednie środki, aby je zatrzymać, przetacza się krew jednej grupy i podaje leki zawierające czynniki krzepnięcia krwi. Przy znaczących objawach rozsianego wykrzepiania wewnątrznaczyniowego heparynę podaje się dożylnie w dawce bolusowej 10 000-15 000 IU. W przypadku niewydolności nerek wykonuje się hemodializę otrzewnową i plazmaferezę, które dają dobry wynik, ale wprowadzenie heparyny jest przeciwwskazane przed tymi manipulacjami. Aby zatrzymać pobudzenie psychomotoryczne i drgawki, przepisuje się diprazynę, haloperidol, oksymaślan sodu. W ciężkich przypadkach należy zastosować intubację i wentylację mechaniczną. Ważne jest, aby pamiętać, że ryzyko krwawienia jest wysokie, dlatego wszystkie manipulacje należy wykonywać z najwyższą ostrożnością. Przy usuwaniu pacjenta ze śpiączki kolejnym krokiem jest przeprowadzenie intensywnej terapii choroby podstawowej. 27. Szok Wstrząs jest formą krytycznego stanu organizmu, objawiającego się dysfunkcją wielonarządową, która kaskaduje na zasadzie uogólnionego kryzysu krążenia i z reguły kończy się śmiercią bez leczenia. Czynnikiem szokowym jest każdy wpływ na organizm, który przekracza siły adaptacyjne. W szoku zmieniają się funkcje oddychania, układu sercowo-naczyniowego i nerek, zaburzone są procesy mikrokrążenia narządów i tkanek oraz procesy metaboliczne. Wstrząs to choroba o charakterze polietiologicznym. W zależności od etiologii wystąpienia, rodzaje wstrząsu mogą być różne. 1. Szok traumatyczny: 1) z urazami mechanicznymi - złamania kości, rany, ucisk tkanek miękkich itp.; 2) z oparzeniami (oparzenia termiczne i chemiczne); 3) pod wpływem niskiej temperatury - szok zimny; 4) w przypadku urazów elektrycznych - porażenie prądem. 2. Wstrząs krwotoczny lub hipowolemiczny: 1) rozwija się w wyniku krwawienia, ostrej utraty krwi; 2) w wyniku ostrego naruszenia bilansu wodnego dochodzi do odwodnienia organizmu. 3. Wstrząs septyczny (toksyczny dla bakterii) (uogólnione procesy ropne wywołane przez mikroflorę Gram-ujemną lub Gram-dodatnią). 4. Wstrząs anafilaktyczny. 5. Wstrząs kardiogenny (zawał mięśnia sercowego, ostra niewydolność serca). Rozważane w dziale stany nagłe w kardiologii. We wszystkich rodzajach wstrząsu głównym mechanizmem rozwoju jest rozszerzenie naczyń krwionośnych, w wyniku czego zwiększa się pojemność łożyska naczyniowego, hipowolemia - zmniejsza się objętość krwi krążącej (BCC), ponieważ istnieją różne czynniki: utrata krwi, redystrybucja płyn między krwią a tkankami lub niedopasowanie normalnej objętości krwi zwiększające pojemność naczyń. Wynikająca z tego rozbieżność między BCC a pojemnością łożyska naczyniowego jest przyczyną zmniejszenia pojemności minutowej serca i zaburzeń mikrokrążenia. Ta ostatnia prowadzi do poważnych zmian w ciele, ponieważ tutaj odbywa się główna funkcja krążenia krwi - wymiana substancji i tlenu między komórką a krwią. Następuje pogrubienie krwi, wzrost jej lepkości i mikrozakrzepica wewnątrzkapilarna. Następnie funkcje komórek ulegają zakłóceniu aż do ich śmierci. W tkankach zaczynają dominować procesy beztlenowe nad tlenowymi, co prowadzi do rozwoju kwasicy metabolicznej. Nagromadzenie produktów przemiany materii, głównie kwasu mlekowego, zwiększa kwasicę. 28. Wstrząs anafilaktyczny Wstrząs anafilaktyczny to zespół różnych reakcji alergicznych typu natychmiastowego, osiągających ekstremalny stopień nasilenia. Istnieją następujące formy wstrząsu anafilaktycznego: 1) postać sercowo-naczyniowa, w której rozwija się ostra niewydolność krążenia, objawiająca się tachykardią, często z zaburzeniami rytmu serca, migotaniem komór i przedsionków oraz spadkiem ciśnienia krwi; 2) postać oddechowa, której towarzyszy ostra niewydolność oddechowa: duszność, sinica, stridor, bulgotanie oddechu, wilgotne rzęski w płucach. Wynika to z naruszenia krążenia kapilarnego, obrzęku tkanki płucnej, krtani, nagłośni; 3) forma mózgowa spowodowana niedotlenieniem, upośledzeniem mikrokrążenia i obrzękiem mózgu. W zależności od ciężkości przebiegu rozróżnia się 4 stopnie wstrząsu anafilaktycznego. Stopień I (łagodny) charakteryzuje się swędzeniem skóry, pojawieniem się wysypki, bólu głowy, zawrotów głowy, uczuciem zaczerwienienia głowy. II stopień (umiarkowany) - obrzęk Quinckego, tachykardia, obniżenie ciśnienia tętniczego, wzrost wskaźnika Algovera łączą się z objawami wskazanymi wcześniej. Stopień III (ciężki) objawia się utratą przytomności, ostrą niewydolnością oddechową i sercowo-naczyniową (duszność, sinica, oddychanie stridorem, mały szybki puls, gwałtowny spadek ciśnienia krwi, wysoki wskaźnik Algovera). Stopień IV (bardzo ciężki) towarzyszy utrata przytomności, ciężka niewydolność sercowo-naczyniowa: puls nie jest określony, ciśnienie krwi jest niskie. Leczenie 1. Dożylny wlew adrenaliny do stabilizacji hemodynamicznej. Można stosować dopminę 10-15 mcg/kg/min, a przy objawach skurczu oskrzeli i b - adrenomimetyki: alupent, brikanil wlew dożylnie. 2. Terapia infuzyjna w objętości 2500-3000 ml z włączeniem poliglucyny i reopolyglucyny, chyba że reakcja jest spowodowana tymi lekami. Wodorowęglan sodu 4% 400 ml, roztwory glukozy do przywrócenia BCC i hemodynamiki. 3. Stabilizatory błony dożylnie: prednizolon do 600 mg, kwas askorbinowy 500 mg, troxevasin 5 ml, etamsylan sodu 750 mg, cytochrom C 30 mg (wskazane dawki dzienne). 4. Leki rozszerzające oskrzela: eufillin 240-480 mg, noshpa 2 ml, alupent (brikanil) 0,5 mg w kroplówce. 5. Leki przeciwhistaminowe: difenhydramina 40 mg (suprastin 60 mg, tavegil 6 ml), cymetydyna 200-400 mg dożylnie (wskazano dawki dzienne). 6. Inhibitory proteazy: trasylol 400 tys. U, Contrical 100 tys. 29. Szok traumatyczny Wstrząs traumatyczny to patologiczny i krytyczny stan organizmu, który powstał w odpowiedzi na uraz, w którym funkcje układów życiowych i narządów są upośledzone i zahamowane. Podczas szoku urazowego rozróżnia się fazy apatii i erekcji. W momencie wystąpienia wstrząs może być pierwotny (1-2 godziny) i wtórny (ponad 2 godziny po urazie). Etap erekcji lub faza występowania. Świadomość pozostaje, pacjent jest blady, niespokojny, euforyczny, nieadekwatny, może krzyczeć, gdzieś biec, wyrwać się itp. Na tym etapie uwalniana jest adrenalina, dzięki czemu ciśnienie i puls mogą przez jakiś czas pozostawać w normie. Czas trwania tej fazy wynosi od kilku minut i godzin do kilku dni. Ale w większości przypadków jest krótki. Faza letargu zastępuje fazę erekcji, kiedy pacjent staje się ospały i adynamiczny, ciśnienie krwi spada i pojawia się tachykardia. Szacunki ciężkości obrażeń podano w tabeli. Ocena stopnia ciężkości urazu
Po obliczeniu punktów uzyskaną liczbę mnoży się przez współczynnik (od 1,2 do 2,0). Leczenie. Główne kierunki leczenia. 1. Eliminacja działania czynnika traumatycznego. 2. Eliminacja hipowolemii. 3. Eliminacja niedotlenienia. 30. Wstrząs krwotoczny Wstrząs krwotoczny to stan ostrej niewydolności sercowo-naczyniowej, który rozwija się po utracie znacznej ilości krwi i prowadzi do zmniejszenia perfuzji ważnych narządów. Etiologia: urazy z uszkodzeniem dużych naczyń, ostre wrzody żołądka i dwunastnicy, pęknięcie tętniaka aorty, krwotoczne zapalenie trzustki, pęknięcie śledziony lub wątroby, pęknięcie jajowodu lub ciąża pozamaciczna, obecność zrazików łożyskowych w macicy itp. Zgodnie z danymi klinicznymi i wielkością niedoboru objętości krwi rozróżnia się następujące stopnie nasilenia. 1. Nie wyrażone - nie ma danych klinicznych, poziom ciśnienia krwi jest normalny. Objętość utraty krwi wynosi do 10% (500 ml). 2. Słaby - minimalny tachykardia, niewielki spadek ciśnienia krwi, pewne oznaki skurczu naczyń obwodowych (zimne dłonie i stopy). Objętość utraty krwi wynosi od 15 do 25% (750-1200 ml). 3. Umiarkowany - tachykardia do 100-120 uderzeń na minutę, spadek ciśnienia tętna, ciśnienie skurczowe 1-90 mm Hg. Sztuka, niepokój, pocenie się, bladość, skąpomocz. Objętość utraty krwi wynosi od 100 do 25% (35-1250 ml). 4. Ciężkie - tachykardia powyżej 120 uderzeń na minutę, ciśnienie skurczowe poniżej 60 mm Hg. Art., często nie określany przez tonometr, otępienie, skrajną bladość, zimne kończyny, bezmocz. Objętość utraty krwi wynosi ponad 35% (ponad 1750 ml). Laboratorium ogólnej analizy krwi, obniżenia poziomu hemoglobiny, erytrocytów i hematokrytu. EKG pokazuje niespecyficzne zmiany w odcinku ST i załamku T, które są spowodowane niewystarczającym krążeniem wieńcowym. Leczenie wstrząsu krwotocznego obejmuje zatrzymanie krwawienia, stosowanie terapii infuzyjnej w celu przywrócenia BCC, stosowanie środków zwężających lub rozszerzających naczynia, w zależności od sytuacji. Terapia infuzyjna polega na dożylnym podaniu płynów i elektrolitów w objętości 4 litrów (sól fizjologiczna, glukoza, albumina, poliglucyna). W przypadku krwawienia wskazane jest przetoczenie jednogrupowej krwi i osocza w łącznej objętości co najmniej 4 dawek (1 dawka to 250 ml). Pokazano wprowadzenie leków hormonalnych, takich jak stabilizatory błon (prednizolon 90-120 mg). W zależności od etiologii przeprowadzana jest specyficzna terapia. 31. Szok septyczny Wstrząs septyczny to przedostanie się czynnika zakaźnego z jego pierwotnego źródła do układu krwionośnego i jego rozprzestrzenienie się po całym organizmie. Czynnikami sprawczymi mogą być: bakterie gronkowcowe, paciorkowcowe, pneumokokowe, meningokokowe i enterokokowe, a także Escherichia, Salmonella i Pseudomonas aeruginosa itp. Wstrząsowi septycznemu towarzyszy dysfunkcja układu płucnego, wątrobowego i nerkowego, naruszenie krzepnięcia krwi co prowadzi do wystąpienia zespołu zakrzepowo-krwotocznego (zespołu Machabeli), który rozwija się we wszystkich przypadkach sepsy. Na przebieg sepsy ma wpływ rodzaj patogenu, co jest szczególnie istotne przy nowoczesnych metodach leczenia. Wyniki badań laboratoryjnych wskazują na postępującą niedokrwistość (spowodowaną hemolizą i hamowaniem hematopoezy). Leukocytoza do 12 χ 109/l, jednak w ciężkich przypadkach, gdy powstaje ostre zagłębienie narządów krwiotwórczych, można również zaobserwować leukopenię. Objawy kliniczne wstrząsu bakteryjnego: dreszcze, wysoka gorączka, niedociśnienie, sucha ciepła skóra - najpierw zimna i mokra, bladość, sinica, zaburzenia psychiczne, wymioty, biegunka, skąpomocz. Charakteryzuje się neutrofilią z przesunięciem formuły leukocytów w lewo do mielocytów; ESR wzrasta do 30-60 mm/h lub więcej. Zwiększa się poziom bilirubiny we krwi (do 35-85 µmol/l), co dotyczy również zawartości azotu resztkowego we krwi. Obniża się krzepliwość krwi i wskaźnik protrombiny (do 50-70%), zmniejsza się zawartość wapnia i chlorków. Całkowite białko krwi jest zmniejszone, co występuje z powodu albuminy, a poziom globulin (alfa globulin i β - globulin) wzrasta. W moczu białko, leukocyty, erytrocyty i cylindry. Poziom chlorków w moczu jest obniżony, a mocznik i kwas moczowy są podwyższone. Leczenie ma przede wszystkim charakter etiologiczny, dlatego przed przepisaniem terapii przeciwbakteryjnej konieczne jest określenie patogenu i jego wrażliwości na antybiotyki. Środki przeciwdrobnoustrojowe należy stosować w maksymalnych dawkach. W leczeniu wstrząsu septycznego konieczne jest stosowanie antybiotyków obejmujących całe spektrum mikroorganizmów Gram-ujemnych. Najbardziej racjonalne jest połączenie ceftazydymu i impinemu, które okazały się skuteczne przeciwko Pseudomonas aeruginosa. Leki takie jak klindamycyna, metronidazol, tikarcylina czy imipinem są stosowane jako leki z wyboru w przypadku wystąpienia opornego patogenu. Jeśli gronkowce zostaną wyhodowane z krwi, konieczne jest rozpoczęcie leczenia penicyliną. Leczenie niedociśnienia polega na pierwszym etapie leczenia w celu zapewnienia odpowiedniej objętości płynu wewnątrznaczyniowego. Stosować roztwory krystaloidów (izotoniczny roztwór chlorku sodu, mleczan Ringera) lub koloidy (albumina, dekstran, poliwinylopirolidon). Zaletą koloidów jest to, że po ich wprowadzeniu wymagane ciśnienie napełniania osiągane jest najszybciej i utrzymuje się przez długi czas. Jeśli nie ma efektu, stosuje się wsparcie inotropowe i (lub) leki wazoaktywne. 32. Zatrucie alkoholem metylowym Alkohol metylowy wchłania się wszystkimi drogami – oddechową, pokarmową i przezskórną. Dawka śmiertelna metanolu przyjętego doustnie waha się w granicach 40-250 ml, ale przyjęcie nawet 10-20 ml może spowodować ślepotę. Zatrucie występuje również po przyjęciu różnych mieszanin alkoholi zawierających od 1,5 do 2,5% metanolu. Po wchłonięciu metanol rozprowadzany jest po wszystkich tkankach ze względu na jego rozpuszczalność w wodzie. Najwięcej gromadzi się w nerkach i przewodzie pokarmowym, najmniej w mózgu, mięśniach i tkance tłuszczowej. Do patologicznych zmian anatomicznych zalicza się obrzęk mózgu oraz uszkodzenie początkowo zapalnego, a później dystroficznego charakteru komórek zwojowych siatkówki. W niektórych przypadkach oprócz uszkodzenia układu nerwowego stwierdza się zmiany zwyrodnieniowe wątroby, nerek, płuc i mięśnia sercowego. W toksycznym działaniu metanolu można wyróżnić działanie dwufazowe. W początkowym okresie (faza I) metanol działa na organizm jako cała cząsteczka i ma głównie działanie narkotyczne, ale słabsze niż alkohol etylowy. Następnie (faza II) objawia się szkodliwy wpływ produktów utleniania. W obrazie klinicznym rozróżnia się okresy: zatrucie, utajone lub względne samopoczucie (trwające od kilku godzin do 1-2 dni), główne objawy zatrucia i, przy korzystnym wyniku, odwrotny rozwój. W zależności od nasilenia rozróżnia się łagodny, umiarkowany (lub okulistyczny) i ciężki (lub uogólniony). Przy łagodnym zatruciu obserwuje się zmęczenie, ból głowy, nudności i stan lekkiego zatrucia, które występują po okresie utajonym od 30 minut do kilku godzin. Jednoczesne wchłanianie alkoholu etylowego i metylowego wydłuża okres utajony i zmniejsza nasilenie zatrucia. Leczenie 1. Zatrzymanie wnikania trucizny do organizmu. Zaprzestanie używania trucizny, usunięcie ze skażonej atmosfery, usunięcie trucizny ze skóry. 2. Usuwanie niewchłoniętej trucizny (z przewodu pokarmowego): 1) sonda do płukania żołądka; 2) stosowanie adsorbentów lub solankowych środków przeczyszczających; 3) oczyszczanie lub lewatywa syfonowa. 3. Usunięcie wchłoniętej trucizny: 1) wymuszanie diurezy; 2) metody detoksykacji pozaustrojowej (hemosorpcja, hemodializa, dializa otrzewnowa, chirurgia wymiany krwi). 4. Terapia antidotum, czyli neutralizacja trucizny poprzez neutralizację fizyczną lub chemiczną, a także rywalizację z trucizną o punkty podania. 5. Utrzymanie funkcji życiowych organizmu. 6. Normalizacja stanu wodno-elektrolitowego, kwasowo-zasadowego organizmu. 7. Leczenie odległych następstw i powikłań. 33. Zatrucie alkoholem etylowym i glikolem etylenowym Podczas przyjmowania dawek toksycznych - pobudzenie, ataksja, otępienie, śpiączka z zahamowaniem odruchów, zapach alkoholu z ust, zaczerwienienie twarzy, zapalenie spojówek, "gra" źrenic, wymioty, mimowolne oddawanie moczu, tachykardia, "chrypka" oddychanie , zapaść, wymioty z możliwością aspiracji wymiotów wt. Leczenie Płukanie żołądka przez grubą sondę, a następnie wprowadzenie środka przeczyszczającego z solą fizjologiczną, lewatywa syfonowa. Podskórnie 1 ml 0,1% roztworu atropiny, 2 ml kordiaminy, 1 ml 20% roztworu kofeiny, z zapaścią - domięśniowo 1 ml 1% roztworu mezatonu. W przypadku braku odruchów gardłowych - intubacja tchawicy i wentylacja mechaniczna. Wymuszanie diurezy z jednoczesnym podaniem 4% roztworu wodorowęglanu sodu w objętości obliczonej według wzoru Astrup, hipertoniczne (10 i 20%) roztwory glukozy z insuliną, witaminami B i C, kokarboksylazą, kwasem nikotynowym. Z depresją oddechową - powoli dożylnie 3-5 ml 1,5% roztworu etimizolu, 10 ml 2,4% roztworu aminofiliny, 1 ml 5% roztworu efedryny, inhalacja tlenem. Z aspiracją - awaryjna bronchoskopia sanitarna. Antybiotyki pozajelitowe. Zatrucie glikolem etylenowym (przeciw zamarzaniu) Średnia dawka śmiertelna wynosi około 100 ml. Jest szybko wchłaniany w przewodzie pokarmowym i rozprowadzany do wszystkich tkanek, tworząc maksymalne stężenie w mózgu. Główny efekt toksyczny obserwuje się w miąższu nerek, gdzie rozwija się martwica nabłonka kanalików, obrzęk śródmiąższowy i ogniska martwicy krwotocznej w warstwie korowej. Obrzęk znajduje się w mózgu. W klinice zatrucia rozróżnia się 3 okresy: 1) początkowe – trwające do 12 godzin, przeważają objawy uszkodzenia OUN ze względu na rodzaj zatrucia alkoholowego; 2) neurotoksyczne – gdy łączą się objawy postępu uszkodzenia OUN oraz zaburzeń układu oddechowego i sercowo-naczyniowego; 3) nefrotoksyczne - w 2-5 dniu dominuje uszkodzenie nerek w obrazie klinicznym zatrucia. Leczenie Płukanie żołądka wodą lub 2% roztworem wodorowęglanu sodu, a następnie wprowadzenie 30 g siarczanu magnezu do 200 ml wody. Wewnątrz 200 ml 30% roztworu alkoholu etylowego. 3-5 g wodorowęglanu sodu w 100 ml wody. Obfity napój. Domięśniowo 1-2 ml kordiaminy, 1 ml 20% roztworu kofeiny. Dożylnie 400 ml 5% roztworu glukozy z 5 ml 5% roztworu kwasu askorbinowego i 8 jm mieszaniny glukozon-wokaina insuliny, 400 ml poliglucyny, 400 ml hemodezu, 80-120 g furosemidu, 60-100 mg prednizolon. 34. Zatrucie dichloroetanem Główne drogi wejścia to przewód pokarmowy, drogi oddechowe i skóra. Śmiertelna dawka DCE dla ludzi po podaniu doustnym wynosi 10-20 ml. Toksyczne działanie DCE wynika z działania narkotycznego na ośrodkowy układ nerwowy, uszkodzenia wątroby, nerek, przewodu pokarmowego i wyraźnego wpływu na układ sercowo-naczyniowy. W obrazie klinicznym wiodącymi objawami są: toksyczna encefalopatia, ostre toksyczne zapalenie żołądka i żołądka i jelit, upośledzenie oddychania zewnętrznego, toksyczne zapalenie wątroby, upośledzona czynność nerek. W pierwszych godzinach po podaniu pojawiają się zawroty głowy, ataksja, pobudzenie psychomotoryczne, drgawki kloniczne, depresja świadomości, aż do śpiączki. Jednym z wczesnych objawów zatrucia są zaburzenia żołądkowo-jelitowe w postaci nudności, powtarzające się wymioty z domieszką żółci. Naruszenie funkcji oddychania zewnętrznego często występuje zgodnie z typem obturacji i aspiracji i wiąże się ze zwiększonym wydzielaniem śliny, krwotokiem oskrzelowym i aspiracją. Obserwuje się hamowanie funkcji ośrodka oddechowego, rozwój hipertoniczności mięśni oddechowych i sztywność klatki piersiowej. Leczenie W przypadku zatrucia oparami - usunięcie ofiary z dotkniętego obszaru, z depresją oddechową IVL. Jeśli trucizna dostanie się do środka - płukanie żołądka przez grubą sondę, a następnie wprowadzenie 3-4 łyżek sproszkowanego węgla aktywnego w 200 ml wody i 150-200 ml oleju wazelinowego, lewatywa syfonowa. Dożylnie 20-40 ml 30% roztworu tiosiarczanu sodu, domięśniowo 5 ml 5% roztworu unitiolu. dożylnie 400 ml poliglucyny, 400 ml hemodezu, 400 ml 5% roztworu glukozy, 80-120 mg furosemidu (lasix), 6-8 ml 5% roztworu kwasu askorbinowego. Domięśniowo 2 ml kordiaminy, z zapaścią - 1 ml 1% roztworu mezatonu, 1 ml 20% roztworu kofeiny, 100-150 mg prednizolonu. Wraz ze wzrostem niewydolności wątrobowo-nerkowej przeprowadza się swoistą terapię. Bolus dożylny 400 ml poliglucyny, 400 ml hemodezu, 400 ml 5% glukozy, 80-120 mg furosemidu, 6-8 ml 5% kwasu askorbinowego, 100-150 mg prednizolonu, na zapaść 1 ml 1% mezaton. Domięśniowo 2-4 ml 6% bromku tiaminy i 2-4 ml 5% pirydoksyny. W przypadku pobudzenia psychomotorycznego 1 ml 3% roztworu fenozepamu. Wdychanie tlenu, w przypadku depresji oddechowej – wentylacja mechaniczna przez rurkę oddechową. W pierwszym dniu najskuteczniejszą i najoszczędniejszą metodą jest dializa otrzewnowa. W skład standardowego roztworu do dializy wchodzą: chlorek potasu 0,3 g, chlorek sodu 8,3 g, chlorek magnezu 0,1 g, chlorek wapnia 0,3 g, glukoza 6 g na 1 litr wody. Jednocześnie do jamy brzusznej pacjenta wstrzykuje się do 2 litrów roztworu elektrolitu z dodatkiem 500 tysięcy jednostek penicyliny i 1000 jednostek heparyny. 35. Zatrucie trucizną grzybową i jadem węża Po okresie utajonym trwającym od 1-2 do 36 godzin pojawiają się skurczowe bóle brzucha, ślinotok, nudności, nieugięte wymioty, biegunka, odwodnienie, zapaść, majaczenie, halucynacje, drgawki. W 2-3 dniu - zjawiska niewydolności nerkowo-wątrobowej z bezmoczem, azotemią, żółtaczką. W ciężkim zatruciu liniami i smardzami możliwa jest hemoliza. Leczenie Płukanie żołądka przez grubą rurkę, a następnie wprowadzenie 3-4 łyżek sproszkowanego węgla aktywnego w 200 ml wody i 30 g siarczanu magnezu (sodu) w 100 ml wody, lewatywa syfonowa. Podskórnie 1 ml 0,1% roztworu atropiny, 2 ml kordiaminy. W zatruciu smardzami atropina nie jest stosowana jako antidotum. Dożylnie 400 ml poliglucyny, 400 ml gemodezu, 400 ml 5% roztworu glukozy z 4-6 ml 5% roztworu kwasu askorbinowego, 80-120 mg furosemidu (lasix). Domięśniowo 1-2 ml 6% roztworu bromku tiaminy i 2 ml 5% roztworu chlorowodorku pirydoksyny (nie wstrzykiwać w jednej strzykawce). Złagodzenie zespołu bólowego domięśniowo po wprowadzeniu 1 ml 0,2% roztworu platifillin, 2 ml 2% roztworu papaweryny. Z drgawkami, pobudzenie psychoruchowe - domięśniowo 1-2 ml 3% roztworu fenozepamu lub mieszaniny litycznej (1-2 ml 2,5% roztworu chloropromazyny, 1-2 ml 1% roztworu dimedrolu, 5-10 ml 25% roztwór siarczanu magnezu) pod kontrolą ciśnienia krwi. Wymuszanie diurezy. W ciężkich przypadkach - hemosorpcja, wczesna hemodializa. Terapia objawowa. Zatrucie jadem węża Ból i szybko rozprzestrzeniający się obrzęk w miejscu ukąszenia, senność, depresja oddechowa, zapaść, hemoliza wewnątrznaczyniowa z hemoglobinurią, ciężkie krwotoki podskórne, czasami drgawki. Prawdopodobnie niewydolność nerek. W przypadku ukąszenia kobry zmiany miejscowe są mniej wyraźne, przeważają zaburzenia opuszkowe (zaburzenia mowy i połykania, opadanie powiek, paraliż mięśni ruchowych) i depresja oddechowa. Leczenie Odsysanie krwi i limfy z rany (nie później niż 30-60 minut po ukąszeniu) powstałej w miejscu ukąszenia za pomocą kubka do wysysania krwi. Płukanie rany 1% roztworem nadmanganianu potasu. Wstrzyknięcie do rany 0,3-0,5 ml 0,1% roztworu adrenaliny. Jeśli to możliwe, pilne podanie specyficznej jedno- lub wieloważnej surowicy przeciw wężowi po wstępnym dożylnym podaniu 100-150 ml hydrokortyzonu lub 50-100 ml prednizolonu. W przypadku ukąszeń kobry - dożylnie surowica Anticobra w dawce 300 ml w połączeniu z 1 ml 0,05% roztworu prozerinu i wielokrotne podawanie co 30 minut z 1 ml 0,1% roztworu atropiny. 36. Zatrucie kwasem i arsenem Wdychanie oparów powoduje podrażnienie oczu i górnych dróg oddechowych (łzawienie, katar, kaszel, duszność). Możliwe jest odruchowe zatrzymanie oddechu. Po okresie utajonym (od 2 do 24 godzin) powstaje toksyczne zapalenie płuc lub toksyczny obrzęk płuc. Przy uderzeniu w oczy, na skórę - oparzenia chemiczne. Po spożyciu - chemiczne oparzenie jamy ustnej, gardła, przełyku, żołądka, możliwy obrzęk krtani z niewydolnością oddechową. Powtarzające się krwawe wymioty, podrażnienie otrzewnej, a czasami perforacja przełyku lub żołądka. Zapaść, wstrząs, zespół krwotoczny. Możliwa hemoliza wewnątrznaczyniowa, nerczyca hemoglobinuriowa z ostrą niewydolnością nerek (nerkowo-wątrobową). Płukanie żołądka bezdętkowe i sztuczne wymioty są niebezpieczne ze względu na możliwość ponownego poparzenia przełyku i aspiracji kwasu. Nie wstrzykiwać solnych roztworów przeczyszczających i zasadowych. Leczenie Płukanie żołądka przez grubą sondę zimną wodą po wstępnym wstrzyknięciu dożylnym lub domięśniowym 1-2 ml 2% roztworu promedolu. Wewnątrz kawałków lodu Almagel A 15-20 ml co godzinę. Dożylnie 800 ml poliglucyny, 400 ml hemodezu, mieszaniny glukozon-wokaina (400 ml 5% roztworu glukozy z 25 ml 2% roztworu nowokainy), 50-150 mg prednizolonu lub 150-250 mg hydrokortyzonu, 10 tysięcy jednostek heparyny, 80-120 mg furosemidu (Lasix). Ulgę w bólu osiąga się poprzez dożylne wstrzyknięcie 1-2 ml 0,005% roztworu fentanylu i 2-4 ml 0,25% roztworu droperydolu, w przypadku uporczywych bólów brzucha - wstrzyknięcie domięśniowe 1-2 ml 0,2% roztworu platyfiliny, 2 ml 2 % roztwór papaweryny. Inhalacja tlenowa ze środkiem przeciwpieniącym. Wraz ze wzrostem obrzęku krtani - dożylnie 200-400 mg prednizolonu, 1-2 ml 1% roztworu difenhydraminy, 10-20 ml 2,4% roztworu aminofiliny, 1-2 ml 5% roztworu efedryny . Jeśli nie ma efektu, tracheostomia, inhalacja tlenu i, jeśli jest to wskazane, wentylacja mechaniczna. Zatrucie arsenem i jego związkami: metaliczny posmak w ustach, ból brzucha, wymioty, luźne stolce, ciężkie odwodnienie, drgawki, tachykardia, obniżone ciśnienie krwi, śpiączka, ostra niewydolność nerek. W wyniku zatrucia wodorem arsenem rozwija się hemoliza wewnątrznaczyniowa i hemoglobinuria. Leczenie Płukanie żołądka przez grubą rurkę (2-3 razy dziennie) z wprowadzeniem na początku i na koniec 50 ml 5% roztworu unithiolu, powtarzane lewatywy syfonowe z dodatkiem unithiolu. Kontynuacja terapii antidotum dożylnie lub domięśniowo z wprowadzeniem 5% roztworu unitiolu (do 300 ml dziennie), kroplówka dożylna 20 ml 10% tetacyny wapnia (ED1A) w 400 ml 5% roztworu glukozy. 37. Zatrucie alkaliami, atropiną, konopiami zatrucie alkaliami Po spożyciu rozwija się chemiczne oparzenie błony śluzowej jamy ustnej, przełyku i żołądka. Ból wzdłuż przełyku i brzucha, wymioty z domieszką krwi, krwawienie z przełyku i żołądka. Możliwa perforacja przełyku, żołądka z rozwojem zapalenia śródpiersia, zapalenie otrzewnej. Z oparzeniem krtani - chrypka głosu, bezgłos, trudności w oddychaniu (stridor). W ciężkich przypadkach - wstrząs oparzeniowy, skąpomocz. Kontakt ze skórą powoduje oparzenia chemiczne. Traktuj jak w przypadku zatrucia kwasem. Zatrucie atropiną Suchość w ustach, chrypka, suchość, przekrwienie skóry, rozszerzone źrenice, duszność, kołatanie serca, tachykardia, pragnienie, nudności, trudności w oddawaniu moczu. W ciężkim zatruciu - możliwe jest pobudzenie psychoruchowe, majaczenie, halucynacje, drgawki, zaburzenia rytmu serca, śpiączka, zapaść. Leczenie W razie potrzeby płukanie żołądka przez grubą sondę, bogato nasmarowaną olejem wazelinowym, wprowadzenie 3-4 łyżek. l. sproszkowany węgiel aktywny w 200 ml wody i 30 mg siarczanu magnezu w 100 ml wody. dożylnie 2-4 ml 0,05% roztworu proseryny, 400-800 ml 5% roztworu glukozy, 40-80 mg furosemidu (lasix). Obfity napój. Łagodzenie pobudzenia psychomotorycznego i drgawek domięśniowo poprzez podanie 1-2 ml 3% roztworu fenozepamu lub mieszaniny litycznej (2 ml 2,5% roztworu aminazyny, 2 ml 1% roztworu difenhydraminy i 10 ml 25 % roztwór siarczanu magnezu) lub 1-2 g wodzianu chloralu w lewatywie z dodatkiem 1-2 g skrobi na 25-50 ml wody, dożylnie 10-15 ml 20% roztworu hydroksymaślanu sodu, 2-4 ml 0,5% roztworu seduxenu. W przypadku ciężkiej tachykardii, ekstrasystoli - dożylnie anaprilin (1-2 ml 0,25% roztworu) lub tabletka anaprilin (40 mg) pod językiem. Z zapaścią - dożylnie 1 ml 1% roztworu mezatonu w 10 ml 0,9% roztworu chlorku sodu. Z ostrą hipertermią - domięśniowo 2 ml 50% roztworu analgezji, okłady lodowe na dużych naczyniach i głowie, mokre okłady. Zatrucie marihuaną (haszysz, marihuana, marihuana, plan) Występuje euforia, pobudzenie psychoruchowe, żywe halucynacje wzrokowe, rozszerzone źrenice, szum w uszach. Następnie osłabienie, letarg, obniżenie nastroju, senność, bradykardia, hipotermia. Leczenie W przypadku zatrucia doustnego - płukanie żołądka przez grubą sondę, a następnie wprowadzenie 3-4 łyżek. l. sproszkowany węgiel aktywny w 200 ml wody. Dożylnie 400-800 ml 5% roztworu glukozy z 5-10 ml 5% roztworu kwasu askorbinowego i 8-16 jednostek insuliny, 40-80 mg furosemidu (lasix), domięśniowo 2 ml 6% roztworu bromku tiaminy. 38. Zatrucie kokainą, dikainą, narkotycznymi lekami przeciwbólowymi zatrucie kokainą Klinicznie objawia się ogólnym pobudzeniem, bólem głowy, zaczerwienieniem twarzy, rozszerzonymi źrenicami, tachykardią, przyspieszonym oddychaniem, podwyższonym ciśnieniem krwi, omamami. W ciężkich przypadkach - drgawki, śpiączka, porażenie oddechowe, zapaść. Powtarzane płukanie żołądka przez grubą sondę 0,1% roztworem nadmanganianu potasu, a następnie wprowadzenie 3-4 łyżek. l. sproszkowany węgiel aktywny w 200 ml wody i 30 g siarczanu magnezu w 100 ml wody. Dożylnie 400 ml gemodezu, 400 ml 5% roztworu glukozy z 5-10 ml 5% roztworu kwasu askorbinowego, 40-80 mg furosemidu (lasix). Podekscytowany - unieruchomienie ofiary domięśniowo 1-2 ml 3% roztworu fenozepamu lub mieszaniny litycznej (1-2 ml 2,5% roztworu chloropromazyny, 2 ml 1% roztworu difenhydraminy i 5-10 ml 25% - roztwór siarczanu magnezu) pod kontrolą ciśnienia krwi. W przypadku drgawek podaje się do lewatywy 1-2 g wodzianu chloralu z 1-2 g skrobi w 25-50 ml wody, dożylnie powoli 15-20 ml 20% roztworu hydroksymaślanu sodu, jeśli nie ma efektu, powoli domięśniowo do 20 ml 2,5% roztworu tiopentalu sodu lub heksenalu. Wraz z rozwojem śpiączki, okład z lodu na głowie, dożylnie 40 ml 40% roztworu glukozy z 4-6 ml 5% roztworu kwasu askorbinowego i 8 jednostek insuliny, powoli dożylnie lub domięśniowo 2-4 ml 6% roztworu bromku tiaminy i 2-4 ml 5% roztworu chlorowodorku pirydoksyny, 80-120 mg furosemidu. Przy ciężkiej depresji oddechowej przeprowadza się wentylację mechaniczną, dożylnie powoli 2 ml kordiaminy, wdychanie tlenu. Zatrucie narkotycznymi lekami przeciwbólowymi (morfina, omnopon, droperydol) Senność lub utrata przytomności, zwężenie źrenic, hipertoniczność mięśni (czasem drgawki), depresja oddechowa, bradykardia, zapaść. Porażenie oddechowe jest możliwe przy zachowanej świadomości pacjenta. Płukanie żołądka przez grubą sondę (przy zachowaniu świadomości), a następnie wprowadzenie 3-4 łyżek. l. sproszkowany węgiel aktywny i 30 g siarczanu sodu, lewatywa syfonowa. Dożylnie 400 ml gemodezu, 400 ml poliglucyny, 400 ml 5% roztworu glukozy, 60-80 mg furosemidu (lasix). Podskórnie 1-2 ml 0,1% roztworu atropiny, 1-2 ml kordiaminy, 1 ml 20% roztworu kofeiny. Wraz z rozwojem śpiączki, okład z lodu na głowie dożylnie 40 ml 40% roztworu glukozy z 5-10 ml 5% roztworu kwasu askorbinowego i 8 jednostek insuliny, dożylnie powoli lub domięśniowo 2-4 ml 6% roztworu bromku tiaminy i 2-4 ml 5% roztworu chlorowodorku pirydoksyny, 80-120 mg furosemidu (lasix). W razie potrzeby - cewnikowanie pęcherza i ekstrakcja moczu. Z depresją oddechową - IVL, wdychanie tlenu. Hemosorpcja (2-3 razy dziennie do przywrócenia świadomości). 39. Ból Ból jest nieprzyjemnym stanem czuciowym i emocjonalnym spowodowanym rzeczywistym lub potencjalnym patologicznym wpływem na tkanki. W OUN ból jest prowadzony dwiema głównymi drogami. Specyficzna ścieżka - tylne rogi rdzenia kręgowego, specyficzne jądra wzgórza, kora tylnego centralnego zakrętu. Droga ta jest niskoneuronalna, szybka, prowadzi ból progowy, emocjonalnie bezbarwny, precyzyjnie zlokalizowany (ból epikrytyczny). Niespecyficzny sposób - tylne rogi rdzenia kręgowego, niespecyficzne jądra wzgórza, kora płatów czołowych i ciemieniowych rozproszone. Prowadzi podprogowy, zabarwiony emocjonalnie, słabo zlokalizowany ból. Jest powolna, wieloneuronowa, ponieważ tworzy liczne elementy oboczne rdzenia przedłużonego, tworu siatkowatego, układu limbicznego i hipokampu. Podprogowe impulsy bólowe sumują się we wzgórzu. Impulsy prowadzone wzdłuż niespecyficznej ścieżki bólu pobudzają ośrodki emocjonalne układu limbicznego, ośrodki autonomiczne podwzgórza i rdzeń przedłużony. Dlatego bólowi towarzyszy strach, bolesne doświadczenia, wzmożony oddech, puls, wzrost ciśnienia krwi, rozszerzenie źrenic, zaburzenia dyspeptyczne. Działaniu nocyceptywnego układu bólowego przeciwdziała układ antynoceceptywny, którego główne neurony zlokalizowane są w okołowodoprzewodowej istocie szarej (akwedukt Sylviusa łączy komorę III i IV). Ich aksony tworzą ścieżki zstępujące do rdzenia przedłużonego i rdzenia kręgowego oraz ścieżki wstępujące do formacji siatkowatej, wzgórza, podwzgórza, układu limbicznego, zwojów podstawy mózgu i kory. Mediatorami tych neuronów są pentapeptydy: metenkefalina i leuenkefalina, które mają odpowiednio metioninę i leucynę jako końcowe aminokwasy. Enkefaliny pobudzają receptory opiatowe. W synapsach enkefalinergicznych receptory opiatowe znajdują się na błonie postsynaptycznej, ale ta sama błona jest presynaptyczna dla innych synaps. Receptory opiatowe są związane z cyklazą adenylanową i powodują jej hamowanie poprzez zaburzenie syntezy cAMP w neuronach. W efekcie zmniejsza się napływ wapnia i uwalnianie mediatorów, w tym mediatorów bólu - peptydów: substancji P, cholecystokininy, somatostatyny, kwasu glutaminowego. Receptory opiatowe pobudzane są nie tylko przez mediatory – enkefaliny, ale także przez inne składniki układu antynocepcyjnego – hormony mózgowe (endorfiny). Agoniści peptydowi receptorów opiatowych powstają podczas proteolizy substancji peptydowych mózgu: proopiokortyny, proenkefalin A i B. Wszystkie te peptydy powstają w podwzgórzu. Receptory opiatów pobudzają receptory we wszystkich strukturach mózgu biorących udział w przewodzeniu i odczuwaniu bólu, tworząc emocjonalnie zabarwione reakcje na ból. Jednocześnie zmniejsza się uwalnianie mediatorów bólu, a wszystkie reakcje towarzyszące bólowi ulegają osłabieniu. 40. Leki przeciwbólowe Lek przeciwbólowy (kwas acetylosalicylowy, paracetamol, morfina) to lek zmniejszający ból różnego pochodzenia. Do klasycznych leków przeciwbólowych nie należą leki, które zmniejszają ból wywołany tylko pewnym czynnikiem sprawczym lub eliminują określony zespół bólowy, na przykład leki zobojętniające sok żołądkowy, ergotamina (migrena), karbamazepina (neuralgia), nitrogliceryna (dławica piersiowa). Kortykosteroidy hamują odpowiedź zapalną i wynikający z niej ból, ale pomimo ich powszechnego stosowania do tych celów, nie stanowią również klasycznych środków przeciwbólowych. Leki przeciwbólowe dzielą się na narkotyczne, działające na struktury ośrodkowego układu nerwowego i powodujące senność, takie jak opioidy, oraz nienarkotyczne, działające głównie na struktury obwodowe, takie jak paracetamol, kwas acetylosalicylowy. Dodatkowe leki wzmacniające działanie leków przeciwbólowych Leki z tej grupy same w sobie nie są lekami przeciwbólowymi, lecz są stosowane w połączeniu z lekami przeciwbólowymi, gdyż mogą zmienić nastawienie do bólu, jego percepcję i poziom lęku, lęku, depresji (trójpierścieniowe leki przeciwdepresyjne mogą nawet powodować zmniejszenie zapotrzebowania na morfina u pacjenta w stanie terminalnym). Takimi lekami mogą być leki psychotropowe, a także te, które wpływają na mechanizmy bólu, np. likwidując skurcze mięśni gładkich i prążkowanych. Narkotyczne środki przeciwbólowe to leki ziołowe i syntetyczne, które selektywnie zmniejszają odczuwanie bólu, zwiększają tolerancję bólu poprzez zmniejszenie emocjonalnego zabarwienia bólu i jego wegetatywnego akompaniamentu, wywołują euforię i uzależnienie od narkotyków. Klasyfikacja narkotycznych leków przeciwbólowych i ich antagonistów 1. Pochodne piperydyno-fenantrenu: 1) morfina; 2) kodeina (metylomorfina, 5-7 razy słabsza od morfiny jako środek przeciwbólowy); 3) etylomorfina (dionina o sile równej morfinie). 2. Pochodne fenylopiperydyny: 1) promedol (3-4 razy słabszy od morfiny); 2) fentanyl (100-400 razy silniejszy niż morfina). 3. Pochodne difenylometanu: 1) pirytramid (dipidolor) - równy morfinie; 2) tramadol (tramal) - nieco gorszy od morfiny. 4. Agoniści-antagoniści: 1) agoniści receptora opiatowego i antagoniści receptora opiatowego - buprenorfina (norfina) (25-30 razy silniejsza niż morfina); 2) agoniści receptora opiatowego i antagoniści receptora opiatowego - pentazocyna (lexir) (2-3 razy słabszy od morfiny) i butorfanol (moradol) (równy morfina). 41. Etapy znieczulenia Znieczulenie ogólne lub znieczulenie to stan organizmu, który charakteryzuje się chwilowym wyłączeniem świadomości osoby, jej wrażliwości na ból i odruchów, a także rozluźnieniem mięśni mięśni szkieletowych, spowodowanym działaniem narkotycznych środków przeciwbólowych na centralny układ nerwowy. W zależności od sposobów wprowadzania leków do organizmu rozróżnia się znieczulenie wziewne i bezinhalacyjne. Istnieją 4 etapy znieczulenia: 1) analgezja; 2) podniecenie; 3) etap chirurgiczny, podzielony na 4 poziomy; 4) etap przebudzenia. Etap analgezji Pacjent jest przytomny, ale obserwuje się pewien letarg, drzemie, odpowiada na pytania monosylabami. Wrażliwość powierzchowna i bólowa jest nieobecna, ale jeśli chodzi o wrażliwość dotykową i termiczną, są one zachowane. Na tym etapie wykonywane są krótkotrwałe interwencje chirurgiczne, takie jak otwarcie ropowicy, ropnie, badania diagnostyczne itp. Etap jest krótkotrwały, trwa 3-4 minuty. Faza wzbudzenia Na tym etapie ośrodki kory mózgowej są zahamowane, a ośrodki podkorowe znajdują się w tym czasie w stanie pobudzenia. Jednocześnie świadomość pacjenta jest całkowicie nieobecna, odnotowuje się wyraźne pobudzenie motoryczne i mowy. Pacjenci zaczynają krzyczeć, próbować wstawać ze stołu operacyjnego. Obserwuje się przekrwienie skóry, puls staje się częsty, wzrasta skurczowe ciśnienie krwi. Źrenica oka rozszerza się, ale reakcja na światło utrzymuje się, obserwuje się łzawienie. Często pojawia się kaszel, zwiększone wydzielanie oskrzeli, czasem wymioty. Nie można wykonać interwencji chirurgicznej na tle wzbudzenia. W tym okresie powinieneś nadal nasycać ciało narkotykiem w celu wzmocnienia znieczulenia. Czas trwania etapu zależy od ogólnego stanu pacjenta i doświadczenia anestezjologa. Zazwyczaj czas trwania wzbudzenia wynosi 7-15 minut. Etap chirurgiczny Wraz z początkiem tego etapu znieczulenia pacjent uspokaja się, oddech staje się spokojny i równomierny, tętno i ciśnienie krwi zbliżają się do normy. W tym okresie możliwe są interwencje chirurgiczne. W zależności od głębokości znieczulenia rozróżnia się 4 stopnie i III stopień znieczulenia. Poziom pierwszy: pacjent jest spokojny, liczba ruchów oddechowych, liczba uderzeń serca i ciśnienie krwi zbliżają się do wartości początkowych. Źrenica stopniowo zaczyna się zwężać, zachowuje się jego reakcja na światło. Drugi poziom: ruch gałek ocznych jest zatrzymany, są one unieruchomione w pozycji centralnej. Źrenice rozszerzają się, a ich reakcja na światło słabnie. Zmniejsza się napięcie mięśni, co pozwala na operacje brzucha. Trzeci poziom charakteryzuje się głębokim znieczuleniem. Jednocześnie źrenice oczu rozszerzają się w reakcji na silny bodziec świetlny. Znieczulenie na czwartym poziomie zagraża życiu pacjenta, ponieważ może dojść do zatrzymania oddechu i krążenia. Etap przebudzenia Gdy tylko ustaje wprowadzanie środków odurzających, ich stężenie we krwi spada, a pacjent przechodzi przez wszystkie etapy znieczulenia w odwrotnej kolejności, następuje przebudzenie. 42. Przygotowanie pacjenta do znieczulenia Anestezjolog odgrywa bezpośrednią i często główną rolę w przygotowaniu pacjenta do znieczulenia i operacji. Obowiązkowym momentem jest badanie pacjenta przed operacją, ale jednocześnie ważna jest nie tylko choroba podstawowa, dla której ma być wykonana operacja, ale także obecność chorób współistniejących, o które szczegółowo pyta anestezjolog . Konieczne jest poznanie sposobu leczenia pacjenta z powodu tych chorób, efektu leczenia, czasu trwania leczenia, obecności reakcji alergicznych, czasu ostatniego zaostrzenia. Jeżeli pacjent podda się zabiegowi chirurgicznemu w zaplanowany sposób, wówczas w razie potrzeby przeprowadzana jest korekta istniejących chorób współistniejących. W przypadku rozchwianych i próchnicowych zębów istotne znaczenie ma higiena jamy ustnej, które mogą być dodatkowym i niepożądanym źródłem infekcji. Anestezjolog dowiaduje się i ocenia stan psychoneurologiczny pacjenta. Na przykład w schizofrenii stosowanie leków halucynogennych (ketaminy) jest przeciwwskazane. Operacja w okresie psychozy jest przeciwwskazana. W przypadku deficytu neurologicznego jest on wstępnie korygowany. Historia alergii ma ogromne znaczenie dla anestezjologa, w tym celu określono nietolerancję leków, a także żywności, chemii gospodarczej itp. Jeśli pacjent ma zaostrzoną anemnezę alergiczną, nawet na leki, podczas znieczulenia może rozwinąć się reakcja alergiczna, aż do wstrząsu anafilaktycznego. Dlatego środki odczulające (difenhydramina, suprastyna) są wprowadzane do premedykacji w dużych ilościach. Ważnym punktem jest obecność pacjenta w przebytych operacjach i znieczuleniu. Okazuje się, na czym polegało znieczulenie i czy były jakieś komplikacje. Zwraca się uwagę na stan somatyczny pacjenta: kształt twarzy, kształt i rodzaj klatki piersiowej, budowę i długość szyi, nasilenie tkanki tłuszczowej podskórnej, obecność obrzęków. Wszystko to jest niezbędne, aby dobrać odpowiednią metodę znieczulenia i leków. Pierwszą zasadą przygotowania pacjenta do znieczulenia podczas każdej operacji i przy zastosowaniu jakiegokolwiek znieczulenia jest oczyszczenie przewodu pokarmowego (żołądek jest przepłukiwany przez sondę, wykonuje się lewatywy oczyszczające). Aby stłumić reakcję psycho-emocjonalną i stłumić aktywność nerwu błędnego, przed operacją pacjentowi podaje się leki - premedykację. W nocy fenazepam jest przepisywany domięśniowo. Pacjentom z niestabilnym układem nerwowym przepisuje się środki uspokajające (seduxen, relanium) na dzień przed operacją. 40 minut przed zabiegiem podaje się domięśniowo lub podskórnie narkotyczne leki przeciwbólowe: 1 ml 1-2% roztworu promololu lub 1 ml pentozociny (lexir), 2 ml fentanylu lub 1 ml 1% morfiny. W celu stłumienia funkcji nerwu błędnego i zmniejszenia wydzielania śliny podaje się 0,5 ml 0,1% roztworu atropiny. 43. Znieczulenie dożylne i wziewne Zaletą dożylnego znieczulenia ogólnego jest szybkie wprowadzenie pacjenta do znieczulenia. Przy tego rodzaju znieczuleniu nie ma podniecenia, a pacjent szybko zasypia. Ale środki odurzające, które są stosowane do podawania dożylnego, powodują krótkotrwałe znieczulenie, więc nie mogą być stosowane w czystej postaci jako mononarkoza do długotrwałych operacji. Barbiturany – tiopental sodu i heksenal – są w stanie szybko wywołać sen narkotyczny, podczas gdy nie ma etapu pobudzenia, a wybudzenie jest szybkie. Obrazy kliniczne znieczulenia przeprowadzonego za pomocą tiopentalu sodu i heksenalu są podobne. Geksenal ma mniej hamujący wpływ na ośrodek oddechowy. Stosowane są świeżo przygotowane roztwory pochodnych kwasu barbiturowego. W chirurgii znieczulenie barbituranami jako mononarkozą stosuje się do krótkotrwałych operacji, które nie trwają dłużej niż 20 minut (np. otwieranie ropni, ropowica, redukcja zwichnięć, manipulacje diagnostyczne, repozycjonowanie fragmentów kości). Pochodne kwasu barbiturowego stosuje się również do znieczulenia indukcyjnego. Hydroksymaślan sodu podaje się dożylnie bardzo powoli. Lek powoduje powierzchowne znieczulenie, dlatego często stosuje się go w połączeniu z innymi środkami odurzającymi, takimi jak barbiturany – propanidyd. Jest często używany do znieczulenia indukcyjnego. Ketamina może być stosowana w mononarkozie oraz do znieczulenia indukcyjnego. Lek powoduje powierzchowny sen, stymuluje aktywność układu sercowo-naczyniowego (wzrost ciśnienia krwi, przyspieszenie tętna). Znieczulenie wziewne przeprowadza się za pomocą łatwo odparowujących (lotnych) cieczy - eteru, halotanu, metoksyfluranu (pentranu), trichloroetylenu, chloroformu lub gazowych substancji odurzających - podtlenku azotu, cyklopropanu. W znieczuleniu dotchawiczym substancja narkotyczna dostaje się do organizmu z aparatu do znieczulenia przez rurkę wprowadzoną do tchawicy. Zaletą metody jest to, że zapewnia drożność dróg oddechowych i może być stosowana w operacjach szyi, twarzy, głowy, eliminuje możliwość aspiracji wymiocin, krwi; zmniejsza ilość stosowanego leku; poprawia wymianę gazową poprzez zmniejszenie „martwej” przestrzeni. Znieczulenie dotchawicze jest wskazane przy dużych zabiegach chirurgicznych, jest stosowane jako znieczulenie wieloskładnikowe ze środkami zwiotczającymi mięśnie (znieczulenie złożone). Całkowite stosowanie kilku leków w małych dawkach zmniejsza toksyczny wpływ na organizm każdego z nich. Nowoczesne znieczulenie mieszane służy do znieczulenia, wyłączenia świadomości, odprężenia. Znieczulenie i wyłączenie przytomności odbywa się za pomocą jednej lub więcej substancji odurzających – wziewnych lub niewdychanych. Znieczulenie przeprowadza się na pierwszym poziomie etapu chirurgicznego. Rozluźnienie lub rozluźnienie mięśni uzyskuje się przez frakcyjne podawanie środków zwiotczających mięśnie. 44. Etapy znieczulenia Istnieją trzy etapy znieczulenia. 1. Wprowadzenie do znieczulenia. Znieczulenie wstępne można przeprowadzić dowolną substancją narkotyczną, wobec której występuje dość głęboki sen znieczulający bez etapu pobudzenia. Najczęściej stosuje się barbiturany, fentanyl w połączeniu z sombrevinem, zmielone z sombrevinem. Często stosuje się również tiopental sodu. Leki stosuje się w postaci 1% roztworu, podaje się je dożylnie w dawce 400-500 mg. Na tle znieczulenia indukcyjnego podaje się środki zwiotczające mięśnie i wykonuje się intubację tchawicy. 2. Utrzymanie znieczulenia. W celu utrzymania znieczulenia ogólnego można użyć dowolnego środka odurzającego, który może chronić organizm przed urazem chirurgicznym (halotan, cyklopropan, podtlenek azotu z tlenem), a także neurolepta-nalgezja. Znieczulenie utrzymuje się na pierwszym i drugim poziomie etapu operacyjnego, a środki zwiotczające mięśnie podaje się w celu zniesienia napięcia mięśniowego, które powoduje mioplegię wszystkich grup mięśni szkieletowych, w tym oddechowych. Dlatego głównym warunkiem nowoczesnej połączonej metody znieczulenia jest wentylacja mechaniczna, którą przeprowadza się poprzez rytmiczne ściskanie torby lub futra lub za pomocą aparatu do sztucznego oddychania. Ostatnio najbardziej rozpowszechniona neuroleptanalgezja. Dzięki tej metodzie do znieczulenia stosuje się podtlenek azotu z tlenem, fentanyl, droperydol, środki zwiotczające mięśnie. Znieczulenie wstępne dożylne. Znieczulenie utrzymuje się przez inhalację podtlenku azotu tlenem w stosunku 2:1, frakcyjne dożylne podawanie fentanylu i droperydolu 1-2 ml co 15-20 minut. Przy zwiększonej częstości akcji serca podaje się fentanyl, ze wzrostem ciśnienia krwi - droperydol. Ten rodzaj znieczulenia jest bezpieczniejszy dla pacjenta. Fentanyl zwiększa ulgę w bólu, droperydol hamuje reakcje wegetatywne. 3. Wycofanie się ze znieczulenia. Pod koniec operacji anestezjolog stopniowo wstrzymuje podawanie substancji odurzających i zwiotczających mięśnie. Świadomość powraca do pacjenta, przywracane jest samodzielne oddychanie i napięcie mięśniowe. Kryteriami oceny adekwatności oddychania spontanicznego są wskaźniki PO2, PCO2 i pH. Po przebudzeniu, przywróceniu spontanicznego oddychania i napięcia mięśni szkieletowych anestezjolog może ekstubować pacjenta i przetransportować go na dalszą obserwację na sali pooperacyjnej. Podczas znieczulenia ogólnego główne parametry hemodynamiki są stale określane i oceniane. Mierz ciśnienie krwi, tętno co 10-15 minut. U osób z chorobami układu sercowo-naczyniowego, a także podczas operacji klatki piersiowej konieczne jest stałe monitorowanie funkcji mięśnia sercowego. Obserwację elektroencefalograficzną można wykorzystać do określenia poziomu znieczulenia. Aby kontrolować wentylację płuc i zmiany metaboliczne podczas znieczulenia i operacji konieczne jest badanie stanu kwasowo-zasadowego (PO2, PCO2, pH, BE). 45. Powikłania znieczulenia Powikłania podczas znieczulenia mogą wystąpić z powodu niewłaściwej techniki znieczulenia lub wpływu środków znieczulających na narządy życiowe. Jedną z takich komplikacji są wymioty. Na początku wprowadzania znieczulenia wymioty mogą być związane z charakterem choroby dominującej (zwężenie odźwiernika, niedrożność jelit) lub z bezpośrednim działaniem leku na ośrodek wymiotny. Na tle wymiotów aspiracja jest niebezpieczna - przedostawanie się treści żołądkowej do tchawicy i oskrzeli. Treść żołądka, która ma wyraźną kwaśną reakcję, opadając na struny głosowe, a następnie wnikając do tchawicy, może prowadzić do skurczu krtani lub skurczu oskrzeli, powodując niewydolność oddechową z późniejszym niedotlenieniem - jest to tak zwany zespół Mendelssohna, któremu towarzyszy sinica, skurcz oskrzeli, częstoskurcz. Niebezpieczna może być regurgitacja - bierne wrzucanie treści żołądkowej do tchawicy i oskrzeli. Powikłania ze strony układu oddechowego mogą wystąpić z powodu upośledzenia drożności dróg oddechowych. Może to być spowodowane wadami aparatu do znieczulenia. Powikłania intubacji tchawicy wykonywanej metodą laryngoskopii bezpośredniej można podzielić na: 1) uszkodzenie zębów przez ostrze laryngoskopu; 2) uszkodzenie strun głosowych; 3) wprowadzenie rurki dotchawiczej do przełyku; 4) wprowadzenie rurki dotchawiczej do oskrzela prawego; 5) wyjście rurki dotchawiczej z tchawicy lub jej zgięcie. Zaburzenia rytmu serca (częstoskurcz komorowy, dodatkowy skurcz, migotanie komór) mogą wystąpić z wielu powodów: 1) niedotlenienie i hiperkapnia wynikające z przedłużonej intubacji lub niedostatecznej wentylacji podczas znieczulenia; 2) przedawkowanie substancji odurzających – barbituranów, halotanu; 3) zastosowanie adrenaliny na tle fluorotanu, co zwiększa wrażliwość fluorotanu na katecholaminy. Uszkodzenie nerwów obwodowych To powikłanie występuje dzień lub dłużej po znieczuleniu. Najczęściej dochodzi do uszkodzenia nerwów kończyn górnych i dolnych oraz splotu ramiennego. Wynika to z nieprawidłowej pozycji pacjenta na stole operacyjnym (odwodzenie ręki ponad 90 od ciała, umieszczenie ręki za głową, zamocowanie ręki do łuku stołu operacyjnego, położenie nóg na uchwyty bez wyściółki). Prawidłowa pozycja pacjenta na stole eliminuje napięcie pni nerwowych. Leczenie prowadzone jest przez neuropatologa i fizjoterapeutę. 46. Znieczulenie miejscowe Znieczulenie powierzchniowe Ten rodzaj znieczulenia przeprowadza się przez kontakt substancji znieczulającej z jednym lub drugim narządem, jego powierzchnią. W tym celu 1-3% roztwór kokainy, 0,25-2% roztwór dikainy, 1-2% roztwór lidokainy, 1-5% roztwór trimekainy i 0,5-2% roztwór piromekainy. Większość środków znieczulających miejscowo wiąże się z unieczynnionymi kanałami sodowymi, zapobiegając ich aktywacji i przedostawaniu się sodu do komórki podczas depolaryzacji błony, uzyskując w ten sposób efekt przeciwbólowy. Technika znieczulenia powierzchniowego jest prosta i polega na nasmarowaniu, zakropleniu roztworu lub rozpyleniu go za pomocą specjalnych pistoletów natryskowych. Początek działania środka znieczulającego jest zależny od pH, przy czym niskie pH zabiera więcej czasu niż przy wysokim pH. Czas działania środka znieczulającego zależy od stopnia jego związania z białkami. Ten rodzaj znieczulenia znajduje zastosowanie w manipulacjach diagnostycznych oraz w okulistyce, otorynolaryngologii. Znieczulenie regionalne Znieczulenie regionalne obejmuje znieczulenie splotowe, przewodzące, zewnątrzoponowe, przykręgowe i inne. W przeciwieństwie do znieczulenia ogólnego, znieczulenie regionalne zapewnia odpowiednią analgezję chirurgiczną dzięki obwodowej blokadzie impulsów bólowych przy zachowaniu prawidłowych funkcji życiowych. Znieczulenie miejscowe jest trudne technicznie i wymaga dokładnej znajomości anatomicznej i topograficznej lokalizacji splotu nerwowego lub przewodnika nerwowego, wyraźnej orientacji w stałych punktach identyfikacyjnych (występy kostne, tętnice, mięśnie), umiejętności oceny oporności tkanek i odczuć pacjenta. Aby wyłączyć wrażliwość na ból, wystarczy wprowadzić 1% roztwór trimekainy (lidokainy), a aby wyłączyć wrażliwość proprioceptywną i osiągnąć rozluźnienie mięśni, należy użyć bardziej stężonych roztworów znieczulających miejscowo (na przykład trimekainy 2-2,5% ). Przywrócenie wrażliwości przebiega w odwrotnej kolejności, tzn. najpierw pojawiają się odczucia napięcia mięśniowego i proprioceptywnego, a następnie odczucia bólu i temperatury. Efekt znieczulenia zależy od ilości środka znieczulającego wnikającego przezkroczowo i powodującego odpowiednią blokadę progową. Podwojenie stężenia wstrzykiwanego środka znieczulającego wydłuża znieczulenie o 1/3, a wprowadzenie podwójnej objętości – tylko o 3-9%. Miejscowe środki znieczulające często prowadzą do reakcji anafilaktycznych. Trimekaina: czas działania wynosi 1-1,5 godziny, maksymalna pojedyncza dawka to 800-1000 mg. Lidokainę (ksykainę) stosuje się w 1-2% roztworze, czas znieczulenia wynosi do 2,5-3 h. Bupiwokainę (markainę) stosuje się w 0,5-0,75% roztworze w maksymalnej jednorazowej dawce 150-170 mg , czas działania 8-12 h. W przypadku stosowania anestetyków długodziałających dodanie lidokainy wyraźnie przyspiesza początek działania, skracając okres utajony. 47. Znieczulenie splotu szyjnego (ASP) OZW, wykonywane jednostronnie lub dwustronnie, pozwala na wykonanie wszelkich operacji na szyi, tarczycy, naczyniach ramienno-głowowych w przypadku ran postrzałowych, urazów i chorób nowotworowych. Splot szyjny (us cervicalis) powstaje z przednich gałęzi czterech górnych nerwów szyjnych (C1-C4), gdy wychodzą one z otworów międzykręgowych. Znajduje się na przedniej powierzchni środkowego mięśnia pochylnego i mięśnia unoszącego łopatkę, poprzecznie do wyrostków poprzecznych kręgów szyjnych. Nerwy ruchowe splotu szyjnego unerwiają mięśnie szyi, a nerwy czuciowe - skórę okolicy potylicznej głowy, przednią i boczną powierzchnię szyi, obszar podobojczykowy do poziomu żeber I i II oraz małżowina uszna. Największym nerwem splotu szyjnego jest przeponowy (p. prenicus), który tworzy się z C3-C4 i rzadziej z dodatkowej gałęzi z C5. Większość nerwów czuciowych wychodzi pośrodku spod tylnej krawędzi mięśnia mostkowo-obojczykowo-sutkowego i rozchodzi się w powierzchownych warstwach szyi, skóry okolicy potylicznej głowy i górnej części klatki piersiowej. Technika znieczulenia 2 cm poniżej kąta żuchwy, przed mięśniem mostkowo-obojczykowo-sutkowym, określa się pulsację tętnicy szyjnej wewnętrznej. Pozioma gałąź kości gnykowej odpowiada poziomowi procesu poprzecznego kręgu C3. Punkt wstrzyknięcia igły znajduje się na przecięciu linii, która jest kontynuacją poziomej gałęzi kości gnykowej, z przednią krawędzią mięśnia mostkowo-obojczykowo-sutkowego. W tym miejscu przecięcia, w warunkach aseptycznych, tworzy się „skórka cytryny”, przez którą wprowadzana jest igła iniekcyjna z zewnątrz do wewnątrz i od przodu do tyłu, prowadząc ją przyśrodkowo do mięśnia mostkowo-obojczykowo-sutkowego i za tętnicę szyjną wewnętrzną tętnicy (w szczelinie między mięśniem mostkowo-obojczykowo-sutkowym a wyczuwalną tętnicą szyjną wewnętrzną) do momentu pojawienia się parestezji lub oparcia igły na wyrostku poprzecznym kręgu C3. Głębokość wstrzyknięcia nie przekracza 2-5 cm Igła jest bezpiecznie zamocowana w tej pozycji i wykonywany jest test aspiracji, określający, czy koniec igły znajduje się w świetle naczynia. W celu znieczulenia z obu stron wstrzykuje się 10-12 ml 2% roztworu trimekainy. Aby wzmocnić znieczulenie splotu szyjnego, można dodatkowo zablokować powierzchowne gałęzie, które docierają do przedniej powierzchni szyi. Miejscem ich wyjścia jest środek tylnej krawędzi mięśnia mostkowo-obojczykowo-sutkowego. Igła jest wstrzykiwana w miejscu ich wyjścia pod powierzchowną powięź szyi. Roztwór 2% trimekainy podaje się w ilości 3-5 ml doczaszkowo i doogonowo (w kształcie wachlarza). Odpowiednie znieczulenie następuje po 8-12 minutach i zapewnia skuteczną ulgę w bólu u większości pacjentów w ciągu 1,5-2 godzin. 48. Znieczulenie splotu ramiennego (APS) APS umożliwia wykonywanie wszelkich operacji na kończynie górnej, stawie barkowym, barku, przedramieniu i dłoni: amputacje, chirurgiczne leczenie ran z repozycjonowaniem i utrwalaniem odłamów kostnych, operacje na naczyniach krwionośnych i nerwach, redukcja zwichnięć barku itp. Wysoka Częstość zabiegów chirurgicznych na kończynie górnej, zwłaszcza w czasie wojny, rodzi pytanie o racjonalne metody znieczulenia podczas tych operacji. Znieczulenie splotu ramiennego według Winnie Pacjent leży na plecach, głowa jest odwrócona w kierunku przeciwnym do miejsca nakłucia, podbródek jest przyłożony do przeciwległej obręczy barkowej. Ręka od strony nakłucia leży wzdłuż ciała, lekko ściągnięta w dół. Charakterystyczne obiekty: mięsień mostkowo-obojczykowo-sutkowy, łuska przednia, przestrzeń śródmiąższowa, żyła szyjna zewnętrzna, obojczyk, chrząstka pierścieniowata. Technika znieczulenia. Skórę traktuje się roztworem antyseptycznym. W tylnej części mięśnia mostkowo-obojczykowo-sutkowego, który wyraźnie zarysowuje się przy lekkim uniesieniu głowy, na poziomie chrząstki pierścieniowatej, opuszki palców lewej ręki należy położyć na mięśniu pochyłym przednim. Przy dalszym przesunięciu palców w bok o 0,5-1,5 cm wyczuwalna jest przestrzeń międzypochyłowa między mięśniami pochyłymi przednimi i środkowymi. Staje się bardziej wyraźny przy głębokim oddechu, gdy mięśnie pochyłe napinają się. W głębi przestrzeni międzystopniowej wyczuwalne są procesy poprzeczne kręgów szyjnych (uczucie stałego oporu), a przy zwiększonym nacisku opuszkiem palca często powstają parestezje w barku lub obręczy barkowej; doogonowo w przestrzeni międzypochyłowej można wyczuć tętnicę podobojczykową. Przestrzeń międzypochylistą w górnym odcinku przecina żyła szyjna zewnętrzna. Punkt wkłucia igły znajduje się w górnej części przestrzeni międzyskokowej, na poziomie chrząstki pierścieniowatej. W tym momencie tworzy się „skórka cytryny”, przez którą igła jest skierowana do środka i lekko w dół, od przodu do tyłu (grzbietowo) do wyrostka poprzecznego C6 pod kątem 30° do płaszczyzny strzałkowej. Kiedy igła przesuwa się do wewnątrz na odległość 1,5-4 cm, pojawia się parestezja, a czubek igły opiera się na wyrostku poprzecznym 6. kręgu szyjnego. W tej pozycji igłę unieruchomia się lub podciąga o 1-2 mm i po teście aspiracyjnym podaje się 30-40 ml 2% roztworu trimekainy (lidokainy) lub 0,5-0,75% roztworu bupiwokainy (markainy). wstrzyknięty. Podczas wstrzyknięcia pierwszych mililitrów roztworu znieczulenia miejscowego pacjent odczuwa krótkotrwały ból („porażenie prądem”), wskazujący na prawidłowe umieszczenie końcówki igły. W przypadku braku parestezji można sprawdzić położenie końcówki igły wstrzykując 0,5 ml 0,9% roztworu chlorku sodu pobranego z lodówki. Pojawienie się uczucia bólu w kończynie górnej wskazuje na kontakt zimnego roztworu z nerwem. 49. Znieczulenie nerwów obwodowych w okolicy nadgarstka W przypadku operacji ręki konieczne jest znieczulenie nerwu łokciowego, pośrodkowego i promieniowego. We wszystkich przypadkach igłę wstrzykuje się na poziomie proksymalnego fałdu nadgarstka. Podczas znieczulenia pacjent leży na plecach, w okolicy nadgarstka ramię jest supinowane i lekko zgięte. Charakterystyczne obiekty: styloid łokciowy, grochowaty, ścięgno zginacza nadgarstka łokciowego i ścięgno zginacza długiego nadgarstka. Znieczulenie nerwu łokciowego Technika znieczulenia gałęzi dłoniowej nerwu łokciowego. Punkt wkłucia igły znajduje się na poziomie bliższego załamania nadgarstka, przyśrodkowo od ścięgna zginacza łokciowego nadgarstka. Igłę wprowadza się na głębokość 1-2 cm przez tkankę podskórną w kierunku kości grochowatej. Po pojawieniu się parestezji i ujemnym wyniku testu aspiracyjnego należy unieruchomić igłę i wstrzyknąć 3-5 ml 2% roztworu trimekainy. W przypadku braku parestezji igłę wprowadza się do momentu zetknięcia się z kością, a po jej usunięciu przeprowadza się infiltrację tkanek 2% roztworem trimekainy. Technika znieczulenia gałęzi grzbietowej nerwu łokciowego. Punkt wkłucia igły znajduje się na poziomie przecięcia proksymalnego fałdu nadgarstka z przyśrodkową krawędzią ścięgna zginacza łokciowego. Igła skierowana jest do wyrostka rylcowatego kości łokciowej. Aby uzyskać parestezję, wstrzykuje się 3-5 ml 2% roztworu trimekainy. W przypadku braku parestezji igłę usuwa się, a do tkanek wprowadza się 5-10 ml 2% roztworu trimekainy. znieczulenie nerwu pośrodkowego Technika znieczulenia. Punkt wkłucia igły znajduje się na linii proksymalnego fałdu skórnego nadgarstka pomiędzy ścięgnem długiego mięśnia dłoniowego a zginaczem promieniowym ręki. Po prostopadłym przesunięciu igły przez tkankę podskórną na głębokość 0,5-1 cm i uzyskaniu parestezji, igłę utrwala się i wstrzykuje 3-5 ml 2% roztworu lidokainy. Jeśli nie jest możliwe uzyskanie parestezji na głębokości 1 cm, tkanki nasącza się w kształcie wachlarza 5-10 ml 2% roztworu trimekainy, powoli wyciągając igłę. Znieczulenie nerwu promieniowego Technika znieczulenia. Miejsce wstrzyknięcia znajduje się na poziomie proksymalnego fałdu skórnego nadgarstka, bocznie od tętnicy promieniowej na występie wierzchołka „tabaka anatomicznej”. Gdy pojawia się parestezja, igłę unieruchamia się, z ujemnym testem aspiracyjnym wstrzykuje się 3-5 ml 2% roztworu trimekainy. W przypadku braku parestezji, 5-10 ml 2% roztworu trimekainy wstrzykuje się w kształcie wachlarza do leżących poniżej tkanek, tworząc „bransoletę” naciekową o długości 3-3,5 cm ze ścięgien krótkiego prostownika i długiego odwodziciela kciuka z jednej strony do długiego prostownika kciuka - z drugiej. 50. Znieczulenie kończyn dolnych Aby wykonać interwencje chirurgiczne na kończynie dolnej, konieczne jest znieczulenie wszystkich czterech głównych nerwów. Trzy z nich - udowy, zasłonowy i zewnętrzny skórny uda - wywodzą się ze splotu lędźwiowego, a nerw kulszowy powstaje częściowo z lędźwiowego i trzech odgałęzień splotu krzyżowego. Technika znieczulenia. Skórę traktuje się roztworem dezynfekującym. Z roztworem znieczulającym tworzy się „skórkę cytryny”, po czym igłę wstrzykuje się pod więzadło pachwinowe 1-1,5 cm poniżej tego ostatniego i 0,5-1 cm w bok od palpowanej tętnicy udowej. Igła jest skierowana przez tkankę podskórną nieco w kierunku proksymalnym pod więzadło pachwinowe, gdzie na głębokości 3-4 cm po nakłuciu powięzi igła zawodzi z utratą oporu i może dojść do parestezji sięgającej powierzchni przedniej uda. W tej pozycji igłę mocuje się kciukiem i palcem wskazującym lewej ręki, a krawędź dłoni lewej ręki dociska siłą do tkanek miękkich uda dystalnie do igły i 35-40 ml Wstrzykuje się 1,5% roztwór trimekainy. Nacisk na tkanki miękkie trwa 1,5-2 minuty. W ten sposób znieczulenie nerwu udowego za pomocą zacisku zamienia się w znieczulenie splotu lędźwiowego, wykonywane z dostępu przedniego. Działanie znieczulenia trwa 2-2,5 godziny. Znieczulenie splotu lędźwiowego można wykonać z dostępu tylnego z jednoczesnym znieczuleniem nerwów udowego (L2-L4) i zasłonowego (L2-L3), nerwu udowo-udowego (L1-L2) oraz nerwu skórnego bocznego udowego (L2-L3) . Pozycja pacjenta podczas znieczulenia jest po zdrowej stronie z ugiętymi nogami. Punkty orientacyjne: wyrostek kolczysty 4. kręgu lędźwiowego (linia łącząca grzebienie biodrowe z tyłu); 3 cm ogonowo wzdłuż grzbietów wyrostków kolczystych od wyrostka kolczystego 4. kręgu lędźwiowego i 5 cm w bok od ostatniego punktu. Technika znieczulenia. Z wyrostka kolczystego 4. kręgu lędźwiowego w kierunku ogonowym rysuje się linię o długości 3 cm, od której końca prostopadła o długości 5 cm jest bocznie przywrócona ku górze. to punkt wstrzyknięcia igły. Po wytworzeniu „skorupki cytrynowej” igłę o długości 12-15 cm wprowadza się prostopadle do skóry, aż do zetknięcia się z wyrostkiem poprzecznym V kręgu lędźwiowego. Czaszkowo, zsuwając się z wyrostka poprzecznego V kręgu lędźwiowego, igła wchodzi w grubość mięśnia kwadratowego lędźwiowego. Jednocześnie wyczuwalny jest opór przed wprowadzeniem do niego roztworu za pomocą strzykawki (lub sprężysty opór występuje przy deformacji pęcherzyka powietrza w strzykawce). Igłę wprowadza się na głębokość, na której występuje uczucie „utraty oporu” (lub nie deformuje się pęcherzyk powietrza). Ten test wskazuje, że igła znajduje się w powięzi między czworobocznym lędźwiowo-lędźwiowym a głównym. Igłę mocuje się na tej głębokości i wstrzykuje się 5-5 ml 35-40% roztworu trimekainy (lidokainy) w celu uzyskania znieczulenia. 51. Znieczulenie nerwu kulszowego Znieczulenie nerwu kulszowego z dostępu przedniego Technika znieczulenia. Pacjent leży na plecach. Przedni górny kolec biodrowy i najbardziej wystający punkt krętarza większego kości udowej są połączone ze sobą linią prostą, a od ostatniego punktu przywracana jest prostopadłość do przedniej powierzchni uda. Długość prostopadłej jest równa odległości pomiędzy kolcem biodrowym przednim górnym a krętarzem większym kości udowej, a koniec tej prostopadłej stanowi punkt projekcji. W fizjologicznej pozycji kończyny dolnej, po potraktowaniu skóry roztworem dezynfekcyjnym i wytworzeniu „skórki cytryny”, igłę o długości 12-15 cm kieruje się pionowo w dół, aż do oparcia się o krętarz mniejszy kości udowej. Po ześlizgnięciu się igły z krętarza mniejszego, bez zmiany głównego kierunku, igła zostaje wprowadzona jeszcze głębiej – 4-5 cm, aż do wystąpienia parestezji. Jeśli nie można uzyskać parestezji, igłę należy ponownie wprowadzić do kości i obracając kończynę do wewnątrz o 7-10, igłę przesuwa się ponownie, aż do pojawienia się parestezji u pacjenta. Znieczulenie nerwu kulszowego z dostępu tylnego Technika znieczulenia. Pacjent leży na boku zdrowym, znieczulana kończyna jest zgięta w stawach biodrowych i kolanowych pod kątem 45-60. Z najbardziej wystającej części krętarza większego kości udowej rysuje się linię prostą do kolca biodrowego tylnego górnego, od którego środka obniża się w kierunku ogonowym prostopadłość o długości 4-5 cm. jako punkt projekcyjny nerwu kulszowego. Igłę wprowadza się pod kątem 90° do czołowej płaszczyzny ciała pacjenta i wprowadza do momentu uzyskania parestezji lub kontaktu z kością. Jeśli to konieczne, igłę należy wyciągnąć i wprowadzić około 0,5 cm z boku lub przyśrodku w stosunku do pierwszego wstrzyknięcia. Uzyskanie parestezji jest obowiązkowe. Podaje się 20-25 ml 2% roztworu lidokainy (trimekainy). Technika znieczulenia nie ulegnie zmianie, jeśli pacjent leży na brzuchu. Znieczulenie w dole podkolanowym Technika znieczulenia. Górny róg romboidalnego dołu znajduje się na poziomie górnej krawędzi rzepki. Punkt iniekcji leży 1-1,5 cm poniżej kąta górnego na dwusiecznej opuszczonej pod tym kątem, utworzonej od zewnątrz przez ścięgno mięśnia dwugłowego uda, od wewnątrz przez ścięgna mięśnia półbłoniastego i półścięgnistego uda. Kierunek ruchu igły jest ściśle pionowy z pacjentem w pozycji leżącej, aż do uzyskania parestezji nerwu piszczelowego. W przypadku braku parestezji igła jest skierowana w kształcie wachlarza, podciągając ją za każdym razem do poziomu tkanki podskórnej. Po teście aspiracji wstrzykuje się 5-10 ml 2% roztworu trimekainy. Aby zablokować wspólny nerw strzałkowy z tego samego punktu, igłę kieruje się bocznie pod kątem 30-45 do płaszczyzny czołowej. Po otrzymaniu parestezji wstrzykuje się 5-10 ml 2% roztworu trimekainy. Nie ma komplikacji ani przeciwwskazań. 52. Powikłania znieczulenia regionalnego Podczas RZS powikłania występują dość rzadko i można je podzielić na dwie grupy. 1. Konkretne, które są bardziej związane z błędami technicznymi metodologii: 1) błędne wstrzyknięcie środka miejscowo znieczulającego do kanału kręgowego lub przestrzeni zewnątrzoponowej dożylnie lub dotętniczo (ze znieczuleniem splotu szyjnego, znieczuleniem splotu lędźwiowego z dostępem pachwinowym); 2) nakłucie jam i narządów (jamy opłucnej, płuca); 3) powstanie krwiaka z zaniedbaniem przebicia i uszkodzenia dużego naczynia; krwiak ściska otaczającą tkankę lub wiązkę nerwowo-naczyniową; 4) przedłużone i ciężkie niedociśnienie, które występuje z szybką resorpcją znieczulenia miejscowego; 5) uraz splotu nerwowego lub przewodnika końcem igły iniekcyjnej podczas brutalnej manipulacji; 6) brak efektu przeciwbólowego po znieczuleniu splotowym lub przewodzeniowym. 2. Niespecyficzny, objawiający się głównie ogólnymi i miejscowymi reakcjami organizmu na działanie znieczulenia miejscowego w postaci reakcji toksycznych i alergicznych. W zależności od czasu, dawki i miejsca podania środka znieczulającego mogą wystąpić niespecyficzne powikłania. W tym przypadku przeważają uszkodzenia ośrodkowego układu nerwowego lub sercowo-naczyniowego. Powikłania od strony ośrodkowego układu nerwowego mogą być łagodne (ograniczone tylko do pobudzenia ośrodkowego) lub ciężkie, co objawia się zahamowaniem ośrodkowego układu nerwowego z możliwym całkowitym porażeniem. Charakter niespecyficznych powikłań: 1) przedawkowanie środka znieczulającego z jednoczesnym podaniem dużej dawki (powyżej 1 g) trimekainy lub lidokainy dotętniczo lub dożylnie; 2) reakcje alergiczne na wprowadzenie środka miejscowo znieczulającego, charakteryzujące się zespołem objawów zaburzeń ośrodkowego układu nerwowego i sercowo-naczyniowego: lęk, zaburzenia świadomości, zaburzenia mowy, drgania mięśni, drgawki, głębokie oddychanie, zaburzenia rytmu serca, rozszerzenie QR, obniżenie ciśnienia krwi, tachykardia, bezdech, asystolia; 3) powikłania infekcyjne z powodu złej jakości obróbki pola operacyjnego w miejscu znieczulenia; 4) rozwój niedociśnienia przy znieczuleniu splotowym i przewodzeniowym jest znacznie rzadszy niż przy znieczuleniu zewnątrzoponowym i podpajęczynówkowym; 5) wraz z wprowadzeniem stężonych roztworów środków miejscowo znieczulających w niewielkim odsetku przypadków obserwuje się rozwój bradykardii. 53. Znieczulenie lędźwiowe Blokada według Wiszniewskiego Ten rodzaj znieczulenia uzyskuje się poprzez wstrzyknięcie środka znieczulającego do kanału kręgowego. Technika nakłucia lędźwiowego jest opisana w wykładzie nr 2. Osobliwością jest to, że poziom nakłucia jest wyższy (T12-1_1, L1-L2) i po wyjęciu trzpienia z igły natychmiast wstrzykuje się środek znieczulający. Objętość środka znieczulającego wynosi 3-5 ml. Naropin podaje się w stężeniu 0,5%, lidokainę - w 2%, marcainę - w 0,5%. Czas trwania znieczulenia wynosi 4-6 h. Ten rodzaj znieczulenia powoduje również ciężkie niedociśnienie. Przy wysokim poziomie znieczulenia (T12-L1) możliwa jest niewydolność oddechowa. Najczęstszym powikłaniem jest ból głowy. Blokada szyjki macicy według A. V. Vishnevsky'ego Pacjent kładzie się na stole na plecach tak, aby ręka po stronie proponowanej blokady wisiała nad krawędzią stołu. Mięsień mostkowo-obojczykowo-sutkowy powinien być rozluźniony. Pod obręczą barkową umieszcza się wałek, głowę cofa się w przeciwnym kierunku; w tej pozycji dobrze zarysowane są anatomiczne kontury szyi. Pole jest traktowane smarowaniem alkoholem i jodem. Lekarz stoi po stronie blokady o tej samej nazwie. Miejsce wstrzyknięcia to kąt utworzony przez przecięcie żyły tylnej krawędzi mięśnia mostkowo-obojczykowo-sutkowego. Palec wskazujący lewej ręki umieszcza się na tylnej krawędzi mięśnia mostkowo-obojczykowo-sutkowego, powyżej miejsca jego przecięcia z żyłą szyjną zewnętrzną. Mocno naciskając palec na to miejsce, próbują przesunąć wiązkę nerwowo-naczyniową do linii środkowej. W takim przypadku palec łatwo wyczuwa przednią powierzchnię kręgów szyjnych. Wstrzyknięcie igły i jej wprowadzenie należy wykonywać powoli, w górę i do wewnątrz, cały czas skupiając się na przedniej powierzchni kręgosłupa. Igła porusza się wzdłuż 2% roztworu nowokainy przesyłanego małymi porcjami (3-0,25 cm), co zapewnia bezpieczeństwo wstrzyknięcia. Strzykawka podczas wstrzykiwania jest wielokrotnie wyjmowana z igły w celu kontroli. Po przyłożeniu igły do kręgu czują, jak się o nią opiera. Następnie nacisk na igłę ulega osłabieniu, dzięki czemu odsuwa się ona o 1-2 mm, po czym wstrzykuje się 40 do 60 ml roztworu, który rozprzestrzeniając się pełzającym naciekiem wzdłuż rozcięgna przedkręgowego, pokrywa błędny, współczulny , a często nerwy przeponowe, przerywające (blokujące) przenoszenie podrażnień z okolicy opłucnej. O skuteczności blokady wagosympatycznej świadczy pojawienie się objawu Hornera (zwężenie źrenicy, zwężenie szpary powiekowej i cofnięcie gałki ocznej). Rytm oddechowy i puls stają się rzadsze, zmniejsza się duszność i sinica, poprawia się stan ogólny. Aby uniknąć wkłucia igły w naczynia szyi, mięsień mostkowo-obojczykowo-sutkowy wraz z leżącym poniżej pęczkiem nerwowo-naczyniowym powinien być wystarczająco mocno przesunięty palcem wskazującym do linii środkowej. Ważne jest, aby skierować igłę do góry i do wewnątrz, ponieważ przesuwanie jej w kierunku poziomym grozi wprowadzeniem rozwiązania pod rozcięgno przedkręgowe i późniejsze powikłanie w postaci zespołu bólowego, który nie ustaje w ciągu dnia. 54. Ocena ciężkości pacjenta Ocena stanu somatycznego pacjenta. 1 punkt - pacjenci, których choroba jest zlokalizowana i co do zasady nie powoduje zaburzeń ogólnoustrojowych, czyli praktycznie ludzie zdrowi. 2 punkty - obejmuje to pacjentów z niewyrażonymi zaburzeniami, które umiarkowanie zakłócają życiową aktywność organizmu bez wyraźnych zmian homeostazy. 3 punkty - pacjenci z życiowymi zaburzeniami ogólnoustrojowymi, które znacząco zakłócają funkcjonowanie organizmu, ale nie prowadzą do niepełnosprawności. 4 punkty - pacjenci z ciężkimi zaburzeniami ogólnoustrojowymi, które stanowią duże zagrożenie dla życia ludzkiego i prowadzą do niepełnosprawności. 5 punktów - pacjenci, których stan uznano za krytyczny, ryzyko zgonu w ciągu 24 godzin jest wysokie. Wielkość i charakter interwencji chirurgicznej: 1 punkt - małe operacje za: usunięcie guzów położonych powierzchownie i zlokalizowanych, otwarcie małych ropni, amputację palców rąk i nóg, podwiązanie i usunięcie hemoroidów, nieskomplikowaną wyrostek robaczkowy i przepukliny. 2 punkty - operacje o umiarkowanym nasileniu: usunięcie powierzchownie zlokalizowanych nowotworów złośliwych wymagających przedłużonej interwencji; otwarcie ropni zlokalizowanych w jamach; amputacja i dezartykulacja kończyn górnych i dolnych; operacje na naczyniach obwodowych; skomplikowane wycięcie wyrostka robaczkowego i przepukliny wymagające rozległej interwencji; próbna torakotomia i laparotomia; inne podobne pod względem złożoności i zakresu interwencji. 3 punkty - rozległe interwencje chirurgiczne: radykalne operacje na narządach jamy brzusznej (z wyjątkiem wymienionych powyżej); radykalne operacje na narządach jamy klatki piersiowej. rozszerzone amputacje kończyn, takie jak amputacja transilisacral; Operacja mózgu. 4 punkty - operacje na sercu, duże naczynia i inne złożone interwencje wykonywane w specjalnych warunkach (sztuczne krążenie, hipotermia itp.). Klasyfikacja obiektywnego statusu pacjenta, opracowana przez Amerykańskie Towarzystwo Anestezjologów (ASA). 1. Nie ma zaburzeń ogólnoustrojowych. 2. Łagodne zaburzenia ogólnoustrojowe bez upośledzenia czynnościowego. 3. Umiarkowane i ciężkie choroby ogólnoustrojowe z dysfunkcją. 4. Ciężka choroba ogólnoustrojowa, stale zagrażająca życiu i prowadząca do niewydolności funkcji. 5. Stan terminalny, wysokie ryzyko śmierci w ciągu dnia, niezależnie od operacji. 6. Śmierć mózgu, dawstwo narządów do przeszczepu. 55. Sztuczna wentylacja płuc Sztuczna wentylacja płuc (ALV) zapewnia wymianę gazową między otaczającym powietrzem (lub pewną mieszaniną gazów) a pęcherzykami płucnymi, stosowana jest jako środek resuscytacji w przypadku nagłego zaprzestania oddychania, jako składnik znieczulenia oraz jako środek intensywnej opieki w przypadku ostrej niewydolności oddechowej, a także niektórych chorób układu nerwowego i mięśniowego. Nowoczesne metody sztucznej wentylacji płuc (ALV) można podzielić na proste i sprzętowe. W sytuacjach awaryjnych (bezdech, rytm patologiczny, oddychanie agonalne, narastająca hipoksemia i (lub) hiperkapnia oraz duże zaburzenia metaboliczne) zwykle stosuje się prostą metodę wentylacji mechanicznej. Najprostsze są metody wydechowe, czyli wentylacja mechaniczna (sztuczne oddychanie) z ust do ust i z ust do nosa. Metody sprzętowe stosuje się, gdy konieczna jest długotrwała wentylacja mechaniczna (od godziny do kilku miesięcy, a nawet lat). Respirator Phase-50 ma ogromne możliwości. Urządzenie Vita-1 przeznaczone jest do praktyki pediatrycznej. Respirator podłącza się do dróg oddechowych pacjenta poprzez rurkę dotchawiczą lub kaniulę tracheostomijną. Wentylacja sprzętowa odbywa się w trybie normalnej częstotliwości, która waha się od 12 do 20 cykli na minutę. W praktyce spotyka się wentylacje o wysokiej częstotliwości (powyżej 1 cykli na minutę), podczas których objętość oddechowa ulega znacznemu zmniejszeniu (do 60 ml lub mniej), zmniejsza się nadciśnienie w płucach pod koniec wdechu, a także wentylacje wewnątrz klatki piersiowej poprawia się ciśnienie i przepływ krwi do serca. Ponadto tryb wysokiej częstotliwości ułatwia adaptację (adaptację) pacjenta do respiratora. Istnieją trzy metody wentylacji wysokiej częstotliwości: wolumetryczna, oscylacyjna i strumieniowa. Objętość jest zwykle przeprowadzana z częstością oddechów 80-100 na 1 min, oscylacyjnym IVL - 600-3600 na 1 min, co zapewnia wibracje ciągłego lub przerywanego przepływu gazu. Najbardziej rozpowszechniona wentylacja strumieniowa o wysokiej częstotliwości z częstością oddechów 100-300 na minutę, w której strumień tlenu o ciśnieniu 1-2 atm jest wdmuchiwany do dróg oddechowych przez igłę lub cewnik o średnicy 2-4 mm. Prowadzona jest także wentylacja pomocnicza, ale w tym przypadku zachowany jest oddech spontaniczny pacjenta. Gaz dostarczany jest po wykonaniu przez pacjenta słabej próby wdechu lub zsynchronizowaniu pacjenta z indywidualnie wybranym trybem pracy urządzenia. Istnieje również tryb przerywanej wentylacji obowiązkowej (PPVL), który wykorzystuje się w procesie stopniowego przejścia od wentylacji sztucznej do oddychania spontanicznego. W tym przypadku pacjent oddycha samodzielnie, ale dodatkowo do dróg oddechowych dostarczany jest ciągły przepływ mieszaniny gazowej. Na tym tle, z ustaloną częstotliwością (od 10 do 1 raz na minutę), urządzenie wykonuje sztuczną inhalację, zbiegającą się (zsynchronizowany PPVL) lub niezbiegającą się (niezsynchronizowany PPVL) ze spontanicznym wdechem pacjenta. Stopniowa redukcja sztucznych oddechów przygotowuje pacjenta do samodzielnego oddychania. 56. Terapia infuzyjna Terapia infuzyjna to wstrzyknięcie kroplowe lub wlew dożylny lub podskórny leków i płynów biologicznych w celu normalizacji równowagi wodno-elektrolitowej, kwasowo-zasadowej organizmu, a także wymuszonej diurezy (w połączeniu z diuretykami). Wskazania do terapii infuzyjnej: wszelkiego rodzaju wstrząsy, utrata krwi, hipowolemia, utrata płynów, elektrolitów i białek w wyniku nieustępliwych wymiotów, intensywnej biegunki, odmowy przyjmowania płynów, oparzeń, choroby nerek; naruszenia zawartości jonów zasadowych (sodu, potasu, chloru itp.), kwasicy, zasadowicy i zatrucia. Roztwory krystaloidów są w stanie zrekompensować niedobór wody i elektrolitów. Nanieść 0,85% roztwór chlorku sodu, roztwory Ringera i Ringera-Locke'a, 5% roztwór chlorku sodu, 5-40% roztwory glukozy i inne roztwory. Podaje się je dożylnie i podskórnie, strumieniem (z silnym odwodnieniem) i kroplówką, w objętości 10-50 ml/kg lub większej. Cele terapii infuzyjnej to: przywrócenie BCC, eliminacja hipowolemii, zapewnienie odpowiedniej pojemności minutowej serca, utrzymanie i przywrócenie prawidłowej osmolarności osocza, zapewnienie odpowiedniego mikrokrążenia, zapobieganie agregacji krwinek, normalizacja funkcji transportu tlenu przez krew. Roztwory koloidalne to roztwory substancji wielkocząsteczkowych. Przyczyniają się do zatrzymywania płynu w łożysku naczyniowym. Stosuje się Hemodez, poliglucynę, reopoliglyukin, reogluman. Wraz z ich wprowadzeniem możliwe są powikłania, które objawiają się w postaci reakcji alergicznej lub pirogennej. Drogi podania - dożylnie, rzadziej podskórnie i kroplówka. Dzienna dawka nie przekracza 30-40 ml/kg. Mają właściwości odtruwające. Jako źródło żywienia pozajelitowego stosuje się je w przypadku długotrwałej odmowy jedzenia lub niemożności karmienia doustnie. Dekstransy to koloidalne substytuty osocza, co czyni je wysoce skutecznymi w szybkim odzyskiwaniu BCC. Dekstransy mają specyficzne właściwości ochronne przed chorobami niedokrwiennymi i reperfuzją, których ryzyko jest zawsze obecne podczas dużych zabiegów chirurgicznych. Świeżo mrożone osocze to produkt pobierany od jednego dawcy. FFP oddziela się od krwi pełnej i zamraża natychmiast w ciągu 6 godzin od pobrania krwi. Przechowywany w 30 C w plastikowych torebkach przez 1 rok. Biorąc pod uwagę labilność czynników krzepnięcia, FFP należy przetaczać w ciągu pierwszych 2 godzin po szybkim rozmrożeniu w temperaturze 37 C. Transfuzja świeżo mrożonego osocza (FFP) stwarza wysokie ryzyko zarażenia się niebezpiecznymi infekcjami, takimi jak HIV, wirusowe zapalenie wątroby typu B i C itp. Częstość reakcji anafilaktycznych i pirogennych podczas przetaczania FFP jest bardzo wysoka, dlatego należy wziąć pod uwagę zgodność z systemem ABO. A dla młodych kobiet należy wziąć pod uwagę Rh - kompatybilność. Autor: Kolesnikova M.A.
▪ Inwestycje. Notatki do wykładów
Nowy sposób kontrolowania i manipulowania sygnałami optycznymi
05.05.2024 Klawiatura Primium Seneca
05.05.2024 Otwarto najwyższe obserwatorium astronomiczne na świecie
04.05.2024
▪ Chemicy walczą z globalnym ociepleniem ▪ Ćwiczenia nóg pozytywnie wpływają na zdrowie mózgu i układu nerwowego ▪ Późna kolacja niszczy pamięć
▪ sekcja witryny Technologia podczerwieni. Wybór artykułów ▪ artykuł Urządzenie odwadniające. Wskazówki dla mistrza domu ▪ artykuł Dlaczego kciuk na tylnej łapie nietoperza nazywany jest toaletą? Szczegółowa odpowiedź ▪ artykuł Refrakcja atmosferyczna. Laboratorium naukowe dla dzieci
Strona główna | biblioteka | Artykuły | Mapa stony | Recenzje witryn www.diagram.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese

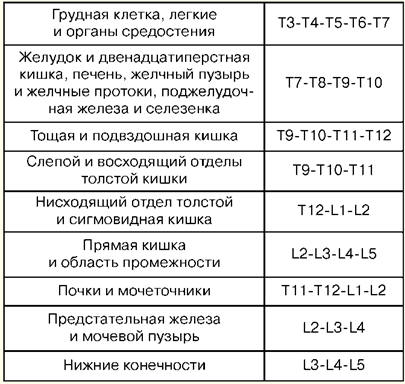


 Zobacz inne artykuły Sekcja
Zobacz inne artykuły Sekcja 