
|
Notatki z wykładów, ściągawki
Terapia szpitalna. Ściągawka: krótko, najważniejsza
Katalog / Notatki z wykładów, ściągawki Spis treści
1. Reumatyzm. Etiologia i patogeneza Reumatyzm (choroba Sokolskiego-Buyo) to ogólnoustrojowa choroba zapalna tkanki łącznej z dominującą lokalizacją procesu w układzie sercowo-naczyniowym, która rozwija się u osób do niej predysponowanych (z reguły są to osoby młode) z powodu ostrej infekcji z paciorkowcem hemolitycznym grupy b BUT. Tę definicję choroby podał w 1989 roku V. A. Nasonov. Klęska innych narządów i układów w reumatyzmie ma drugorzędne znaczenie i nie determinuje jej nasilenia i późniejszego rokowania. Etiologia. Paciorkowce beta-hemolizujące grupy A powodują infekcje górnych dróg oddechowych. Dlatego początek reumatyzmu z reguły poprzedza dławica piersiowa, zaostrzenie przewlekłego zapalenia migdałków, a we krwi pacjentów zwiększona ilość antygenu paciorkowcowego i przeciwciał przeciwko paciorkowcom (ASL-O, ASG, ASA, antydeoksyrybonukleaza B (anty-DNaza B) są wykrywane. W rozwoju reumatyzmu rolę odgrywają czynniki wiekowe i społeczne (niekorzystne warunki życia, niedożywienie), ważna jest również predyspozycja genetyczna (reumatyzm jest chorobą dziedziczoną poligenicznie, dobrze wiadomo o istnieniu rodzin „reumatycznych”), która polega na odpowiedź hiperimmunologiczna na antygeny paciorkowców, skłonność pacjentów do procesów autoimmunologicznych i immunokompleksowych. Patogeneza. W reumatyzmie występuje złożona i zróżnicowana odpowiedź immunologiczna (reakcje nadwrażliwości typu natychmiastowego i opóźnionego) na liczne antygeny paciorkowców. Kiedy infekcja dostanie się do organizmu, wytwarzane są przeciwciała przeciw paciorkowcom i powstają kompleksy immunologiczne (antygeny paciorkowców + przeciwciała przeciwko nim + dopełniacz), które krążą we krwi i osadzają się w łóżku mikrokrążenia. Toksyny i enzymy Streptococcus mają również szkodliwy wpływ na mięsień sercowy i tkankę łączną. Ze względu na genetycznie uwarunkowany defekt układu odpornościowego, antygeny paciorkowców i kompleksy immunologiczne nie są całkowicie i szybko eliminowane z organizmu pacjentów. W rezultacie procesy autoimmunologiczne rozwijają się w zależności od rodzaju nadwrażliwości typu opóźnionego, a we krwi pacjentów znajdują się limfocyty reagujące z tkanką serca. Komórki te mają duże znaczenie w powstawaniu zmian narządowych (głównie serca). W tkance łącznej przy reumatyzmie zachodzą zmiany fazowe: obrzęk śluzowy – zmiany włóknikowate – martwica włóknikowata. Morfologiczną ekspresją zaburzeń immunologicznych są reakcje komórkowe - naciek limfocytów i plazmocytów, powstawanie ziarniniaka reumatycznego lub Ashofftalalaevskaya. Proces patologiczny kończy się stwardnieniem. Gdy serce jest uszkodzone, proces zapalny może rozprzestrzenić się na wszystkie błony serca (pancarditis) lub osobno na każdą z błon. 2. Obraz kliniczny reumatyzmu Wszystkie objawy choroby można podzielić na sercowe i pozasercowe. Z tych pozycji można opisać obraz kliniczny choroby. Etap I: ujawnia się związek choroby z przeniesioną infekcją. W typowych przypadkach po 1-2 tygodniach od bólu gardła lub ostrej choroby układu oddechowego temperatura ciała wzrasta, czasem do 38-4°C, z wahaniami w ciągu dnia w granicach 1-2 C i silnym poceniem się (zwykle bez dreszczy). Najczęstszym objawem reumatyzmu jest uszkodzenie serca - choroba reumatyczna serca: jednoczesne uszkodzenie mięśnia sercowego i wsierdzia. Pacjenci skarżą się na łagodny ból lub dyskomfort w okolicy serca, znacznie rzadziej występują lekkie duszności podczas ćwiczeń, przerwy lub kołatanie serca. Reumocarditis u młodych pacjentów z reguły jest ciężkie: od samego początku choroby obserwuje się ciężką duszność podczas ćwiczeń iw spoczynku, ciągły ból w sercu i kołatanie serca. Rzadko występuje zapalenie osierdzia, a także pozasercowe objawy reumatyzmu. Wraz z rozwojem suchego zapalenia osierdzia pacjenci odnotowują tylko stały ból w okolicy serca. W przypadku wysiękowego zapalenia osierdzia, charakteryzującego się nagromadzeniem surowiczo-włóknistego wysięku w worku sercowym, ból znika, ponieważ arkusze osierdzia w stanie zapalnym są oddzielone gromadzącym się wysiękiem. Najbardziej charakterystyczną cechą reumatyzmu jest porażka układu mięśniowo-szkieletowego w postaci reumatycznego zapalenia wielostawowego. Zmiany reumatyczne nerek są również niezwykle rzadkie, wykrywane tylko w badaniu moczu. Zespół brzuszny (zapalenie otrzewnej) występuje prawie wyłącznie u dzieci i młodzieży z ostrym reumatyzmem pierwotnym. W II etapie poszukiwań diagnostycznych wykrycie oznak uszkodzenia serca ma niewielkie znaczenie. W pierwotnej reumatycznej chorobie serca serce zwykle nie jest powiększone. Osłuchiwanie ujawnia stłumiony ton I, czasami pojawienie się tonu III, cichy szmer skurczowy na wierzchołku. Ta symptomatologia wynika ze zmian w mięśniu sercowym. W przypadku uszkodzenia zastawki aortalnej może być słyszalny szmer protorozkurczowy w punkcie Botkina, a dźwięczność tonu II może zostać zachowana. U pacjentów z zapaleniem wielostawowym obserwuje się deformację stawów z powodu zapalenia błony maziowej i tkanek okołostawowych, bólu przy palpacji stawu. Rumień w kształcie pierścienia (objaw prawie patognomoniczny dla reumatyzmu) występuje niezwykle rzadko (u 1-2% pacjentów). Na III etapie poszukiwań diagnostycznych dane z badań laboratoryjnych i instrumentalnych pozwalają nam ustalić aktywność procesu patologicznego i wyjaśnić uszkodzenie serca i innych narządów. Wskaźniki ostrej fazy: neutrofilia z przesunięciem liczby leukocytów w lewo; wzrost zawartości 2-globulin, a następnie wzrost poziomu globulin; zwiększona zawartość fibrynogenu; pojawienie się białka C-reaktywnego; ESR wzrasta. Parametry immunologiczne, zwiększone miano przeciwciał przeciwko paciorkowcom (antyhialuronidaza i antystreptokinaza powyżej 1:300, anty-O-streptolizyna powyżej 1:250). 3. Diagnoza reumatyzmu Wraz ze stopniowym początkiem reumatyzmu, diagnoza syndromiczna zaproponowana przez AI Niestierowa w 1973 r. (patrz Tabela 1) ma znaczenie: zespół kliniczny i epidemiologiczny; zespół sercowo-naczyniowy (patrz Tabela 2). Tabela 1
Tabela 2
4. Diagnostyka różnicowa reumatyzmu Należy odróżnić reumatyczne zapalenie wielostawowe od niereumatycznych (patrz tabela). stół
5. Leczenie reumatyzmu Cały kompleks leczenia reumatyzmu składa się z terapii przeciwbakteryjnej i przeciwzapalnej, środków mających na celu przywrócenie homeostazy immunologicznej. Zaleca się stosowanie racjonalnej, zbilansowanej diety, skupienie się na adaptacji do aktywności fizycznej, przygotowanie do pracy, terminowe leczenie chirurgiczne pacjentów ze złożonymi wadami serca. Wszystkim pacjentom w aktywnej fazie reumatyzmu pokazano penicylinę (1 200 000-1 500 000 jm na 6 dawek dziennie, co 4 godziny), która ma działanie bakteriobójcze na wszystkie rodzaje paciorkowców A. Przebieg leczenia wynosi 2 tygodnie w aktywnej fazie reumatyzmu, w przyszłości wymagane jest przejście na przedłużoną bicylinę-5 (1 500 000 jednostek). W przypadku nietolerancji penicyliny można przepisać erytromycynę 250 mg 4 razy dziennie. Leki o działaniu przeciwzapalnym, które są stosowane w nowoczesnym leczeniu aktywnej fazy reumatyzmu, to glikokortykosteroidy, pochodne salicylowe, indolowe, pochodne kwasu fenylooctowego itp. Prednizolon stosuje się w dawce 20-30 mg dziennie (przez 2 tygodnie, następnie dawkę zmniejsza się o 2,5-5 mg co 5-7 dni, w sumie przez 1,5-2 miesiące) w przypadku pierwotnego i nawrotowego z III i II stopień aktywności procesu reumatycznej choroby serca, z zapaleniem błon surowiczych i pląsawicy, z rozwojem niewydolności serca w wyniku czynnego zapalenia serca. Kortykoidy wpływają na metabolizm wodno-solny, dlatego w leczeniu należy stosować chlorek potasu 3-4 g/dobę, pananginę i inne, z zatrzymaniem płynów - antagoniści aldosteronu (weroszpiron do 6-8 tabletek dziennie), leki moczopędne (lasix). 40 -80 mg / dzień, furosemid 40-80 mg / dzień itp.), z euforią - środki uspokajające itp. Niesteroidowe leki przeciwzapalne są również szeroko stosowane w reumatyzmie: średnie dawki kwasu acetylosalicylowego wynoszą 3-4 g dziennie, rzadziej 5 g dziennie lub więcej. Kwas acetylosalicylowy stosuje się 1 g 3-4 razy dziennie po posiłkach przez 1-3 miesiące lub dłużej z prawidłową tolerancją i pod warunkiem kontroli skutków ubocznych. Skuteczne stosowanie pochodnej kwasu indoloctowego - indometacyny w reumatyzmie od ponad 20 lat. Ma wyraźny efekt terapeutyczny: subiektywne objawy zapalenia serca (ból serca, kołatanie serca, duszność) znikają do 8-10 dnia terapii, a obiektywne objawy - do 14-16 dnia. Znikanie zapalenia wielostawowego i zapalenia błon surowiczych następuje jeszcze szybciej. W leczeniu reumatyzmu ważne jest połączenie trzech głównych etapów: szpital – klinika – uzdrowisko. Na etapie I leczenie przeprowadza się wyżej wymienionymi lekami. Po zmniejszeniu aktywności reumatyzmu i normalizacji stanu chorego przechodzą do II etapu - leczenia w sanatorium reumatologicznym. Głównym celem tego etapu jest kontynuacja leczenia niesteroidowymi lekami przeciwzapalnymi. Etap III obejmuje obserwację ambulatoryjną i leczenie profilaktyczne. 6. Klasyfikacja kardiomiopatii. Etiologia kardiomiopatii rozstrzeniowej (DCM) Kardiomiopatie to pierwotne izolowane uszkodzenia mięśnia sercowego o charakterze niezapalnym o nieznanej etiologii (idiopatyczne), nie są związane z wadami zastawkowymi lub przeciekami wewnątrzsercowymi, nadciśnieniem tętniczym lub płucnym, chorobą wieńcową serca lub chorobami ogólnoustrojowymi (takimi jak kolagenozy, amyloidoza, hemochromatoza, itp.), ponadto w końcowej fazie choroby rozwija się ciężka zastoinowa niewydolność serca i złożone naruszenia rytmu serca i drożności. Klasyfikacja kardiomiopatii jest następująca: 1) kardiomiopatia rozstrzeniowa: a) idiopatyczny; b) toksyczny; c) zakaźny; d) z kolagenozami; 2) przerostowe; 3) restrykcyjny; 4) dysplazja arytmiczna prawej komory; 5) połączenie jednego z 4 typów kardiomiopatii z nadciśnieniem tętniczym. Kardiomiopatia rozstrzeniowa (DCM) to choroba mięśnia sercowego charakteryzująca się rozlanym rozszerzeniem wszystkich komór serca (głównie lewej komory), w której na pierwszy plan wysuwa się patologia funkcji pompowania serca, a w rezultacie , przewlekła niewydolność serca (stąd druga nazwa to zastoinowa, gdy serce nie jest w stanie w pełni pompować krwi i „zatrzymuje się” w tkankach i narządach organizmu). Mięśniowa ściana serca pozostaje niezmieniona lub przerośnięta w różnym stopniu. Choroby i czynniki poprzedzające rozwój DCMP opisano w poniższej tabeli (patrz tabela). Tabela. Choroby i czynniki poprzedzające rozwój DCM
Jest to najczęstsza forma uszkodzenia mięśnia sercowego. Częstość występowania wynosi 5-8 przypadków na 100 000 osób rocznie. Nie ma jasnego wywiadu rodzinnego dla tych pacjentów. Mężczyźni chorują 2-3 razy częściej niż kobiety. 7. Patogeneza kardiomiopatii rozstrzeniowej (DCM) Patogeneza. W wyniku procesu zapalnego w mięśniu sercowym (zapalenie mięśnia sercowego) poszczególne komórki obumierają w różnych jego częściach. Zapalenie w tym przypadku ma charakter wirusowy, a komórki dotknięte wirusem stają się obcymi czynnikami dla organizmu. W związku z tym, gdy w organizmie pojawiają się antygeny, rozwija się zespół reakcji immunologicznych, których celem jest ich zniszczenie. Stopniowo martwe komórki mięśniowe są zastępowane tkanką łączną, która nie ma zdolności do rozciągliwości i kurczliwości właściwej mięśniowi sercowemu. W wyniku utraty podstawowych funkcji mięśnia sercowego serce traci zdolność do funkcjonowania jako pompa. W odpowiedzi na to (jako reakcja kompensacyjna) komory serca rozszerzają się (tzn. rozszerzają się), a w pozostałej części mięśnia sercowego dochodzi do zgrubienia i zgrubienia (tzn. rozwija się jego przerost). Aby zwiększyć dostarczanie tlenu do narządów i tkanek organizmu, występuje uporczywy wzrost częstości akcji serca (tachykardia zatokowa). Ta kompensacyjna odpowiedź tylko tymczasowo poprawia funkcję pompowania serca. Jednak możliwości rozszerzenia i przerostu mięśnia sercowego są ograniczone ilością żywotnego mięśnia sercowego i są indywidualne dla każdego konkretnego przypadku choroby. Wraz z przejściem procesu do etapu dekompensacji rozwija się przewlekła niewydolność serca. Jednak na tym etapie w grę wchodzi inny mechanizm kompensacyjny: tkanki ciała zwiększają pozyskiwanie tlenu z krwi w porównaniu ze zdrowym ciałem. Ale ten mechanizm jest niewystarczający, ponieważ zmniejszenie funkcji pompowania serca prowadzi do zmniejszenia dopływu tlenu do narządów i tkanek, co jest niezbędne do ich normalnego funkcjonowania, podczas gdy ilość w nich dwutlenku węgla wzrasta. U 2/3 pacjentów w jamach komór w późnych stadiach choroby tworzy się skrzeplina ciemieniowa (z powodu zmniejszenia funkcji pompowania serca, a także nierównomiernego skurczu mięśnia sercowego w komorach serca ), a następnie rozwój zatorowości w krążeniu płucnym lub ogólnoustrojowym. Zmiany patohistologiczne i patomorfologiczne w sercu. Kształt serca staje się kulisty, jego masa wzrasta od 500 do 1000 g, głównie za sprawą lewej komory. Mięsień sercowy staje się zwiotczały, matowy, z zauważalnymi białawymi warstwami tkanki łącznej, występuje charakterystyczna przemiana kardiomiocytów przerośniętych i zanikowych. Mikroskopowo wykrywa się rozlane zwłóknienie, można je łączyć zarówno z atrofią, jak i przerostem kardiomiocytów, w którym występuje znaczny wzrost objętości jąder, liczba mitochondriów, rozrost aparatu Golgiego, wzrost liczby miofibryli , wolny i związany z rybosomami retikulum endoplazmatycznego, obfitość granulek glikogenu. 8. Obraz kliniczny i diagnostyka kardiomiopatii rozstrzeniowej (DCM) Nie ma konkretnych objawów choroby. Obraz kliniczny jest polimorficzny i określany przez: 1) objawy niewydolności serca; 2) zaburzenia rytmu i przewodzenia; 3) zespół zakrzepowo-zatorowy. W większości przypadków rokowanie choroby zależy od porażki lewej komory serca. Przed wystąpieniem niewydolności serca DCM jest utajony. Najczęstszymi skargami na już rozpoczętą niewydolność serca są skargi na zmniejszoną wydajność, zwiększone zmęczenie, duszność podczas wysiłku, a następnie w spoczynku. W nocy ma suchy kaszel (odpowiednik astmy sercowej), później - typowe ataki astmy. Pacjenci zgłaszają się z charakterystycznym bólem dławicowym. Wraz z rozwojem przekrwienia w krążeniu ogólnoustrojowym pojawia się ciężkość w prawym podżebrzu (z powodu powiększonej wątroby), obrzęk nóg. Diagnostyka. Podczas diagnozowania choroby ważnym objawem jest znaczny wzrost serca (nie ma objawów wady zastawkowej serca ani nadciśnienia tętniczego). Kardiomegalia objawia się rozszerzeniem serca w obu kierunkach, zdeterminowanym przez perkusję, a także przemieszczeniem uderzenia wierzchołka w lewo iw dół. W ciężkich przypadkach słychać rytm galopu, tachykardię, szmery względnej niewydolności zastawki mitralnej lub trójdzielnej. W 20% przypadków rozwija się migotanie przedsionków. Ciśnienie krwi jest zwykle normalne lub nieznacznie podwyższone (z powodu niewydolności serca). Badania biochemiczne krwi i moczu mogą wykryć różne substancje toksyczne, a także niedobory witamin. Instrumentalne metody badawcze umożliwiają wykrycie: 1) oznaki kardiomegalii; 2) zmiany wskaźników hemodynamiki centralnej; 3) zaburzenia rytmu i przewodzenia. Fonokardiogram potwierdza dane osłuchowe w postaci rytmu galopu, dość powszechnego wykrywania szmeru skurczowego. Rentgen ujawnił znaczny wzrost komór i zastój krwi w (małym) krążeniu płucnym. Echokardiografia pomaga wykryć poszerzenie obu komór, hipokinezę tylnej ściany lewej komory, paradoksalny ruch przegrody międzykomorowej podczas skurczu. Przeprowadzane jest badanie radioizotopowe serca (scyntygrafia mięśnia sercowego) w celu wyjaśnienia stanu funkcji pompowania serca, a także określenia stref martwego mięśnia sercowego. Angiokardiograficznie wykrywa się te same zmiany, co na echokardiogramie. Żywa biopsja mięśnia sercowego nie dostarcza informacji do określenia etiologii kardiomiopatii. W niektórych przypadkach w biopsji można wykryć antygen wirusowy lub wzrost zawartości LDH, a także zmniejszenie produkcji energii przez mitochondria. 9. Różnicowanie/diagnostyka kardiomiopatii rozstrzeniowej (DCM) Powstaje przede wszystkim przy zapaleniu mięśnia sercowego i dystrofiach mięśnia sercowego, czyli przy schorzeniach, które czasami niesłusznie nazywa się kardiomiopatiami wtórnymi. Biopsja mięśnia sercowego zapewnia znaczną pomoc w diagnostyce różnicowej kardiomiopatii rozstrzeniowej i choroby serca, występującej z wyraźnym jej wzrostem: 1) z ciężkim rozlanym zapaleniem mięśnia sercowego stwierdza się naciek komórkowy zrębu w połączeniu ze zmianami dystroficznymi i martwiczymi w kardiomiocytach; 2) z pierwotną amyloidozą występującą z uszkodzeniem serca (tzw. kardiopatyczny wariant pierwotnej amyloidozy) występuje znaczne odkładanie amyloidu w tkance śródmiąższowej mięśnia sercowego połączone z atrofią włókien mięśniowych; 3) z hemochromatozą (choroba spowodowana naruszeniem metabolizmu żelaza), obserwuje się złogi pigmentu zawierającego żelazo w mięśniu sercowym, obserwuje się różne stopnie dystrofii i atrofii włókien mięśniowych oraz proliferację tkanki łącznej. Jako wariant DCM można rozważyć kardiomiopatie polekowe i toksyczne. Liczne środki mogą powodować toksyczne uszkodzenie mięśnia sercowego: etanol, emetyna, lit, kadm, kobalt, arsen, izoproterenol i inne trucizny. Zmiany patohistologiczne w tkankach mięśnia sercowego objawiają się w postaci ogniskowych dystrofii. Najbardziej uderzającym przykładem toksycznej kardiomiopatii jest kardiomiopatia występująca u osób pijących nadmierne ilości piwa. W ostrym stadium kardiomiopatii kobaltowej obserwuje się zwyrodnienie wodniste i tłuszczowe, zniszczenie organelli wewnątrzkomórkowych i ogniskową martwicę kardiomiocytów. Kardiomiopatia alkoholowa. Etanol ma bezpośredni toksyczny wpływ na kardiomiocyty. Makroskopowo mięsień sercowy jest zwiotczały, glinopodobny, czasami widoczne są niewielkie blizny. Tętnice wieńcowe są nienaruszone. Badanie mikroskopowe wykazuje kombinację dystrofii (obwodu i tkanki tłuszczowej), atrofii i przerostu kardiomiocytów, mogą występować ogniska rozpadu kardiomiocytów i miażdżycy. Dotknięte obszary mięśnia sercowego kontrastują z niezmienionymi. Badanie pod mikroskopem elektronowym wycinków z biopsji serca wykazuje torbielowate rozszerzenie siateczki sarkoplazmatycznej i układu T kardiomiocytów, co jest charakterystyczne dla kardiomiopatii alkoholowej. Powikłania kardiomiopatii alkoholowej - nagła śmierć w wyniku migotania komór lub przewlekłej niewydolności serca, zespół zakrzepowo-zatorowy. 10. Leczenie i profilaktyka kardiomiopatii rozstrzeniowej (DCM) Ogólne zasady leczenia DCM nie różnią się znacząco od leczenia przewlekłej niewydolności serca. W przypadkach wtórnej DCM dodatkowo przeprowadza się leczenie poprzedniej choroby (choroby zastawkowej serca itp.) I podejmuje się wszelkie środki w celu wyeliminowania przyczyn DCM. Środki rozszerzające naczynia obwodowe są dość skuteczne, szczególnie w przypadku współistniejącego zespołu dławicowego (nitrong, sustak, nitrosorbid). W przypadku zespołu dusznicy bolesnej konieczne staje się stosowanie leków przeciwdławicowych, najlepiej przedłużonych azotanów (sustak, nitrong, nitrosorbid). Adrenoblockery są skuteczne (są przepisywane w przypadku braku objawów niewydolności serca). Spośród nowoczesnych metod chirurgicznego leczenia DCMP najskuteczniejszą jest przeszczep serca (transplantacja). Jednak możliwości przeprowadzenia tej operacji są znacznie ograniczone. Z tego powodu, jako alternatywę dla przeszczepu serca w nowoczesnym leczeniu, aby wydłużyć długość życia pacjentów z DCMP, opracowano i wykonuje się operacje rekonstrukcyjne, które mają na celu wyeliminowanie niewydolności zastawki mitralnej i trójdzielnej. Alternatywą dla przeszczepu serca u chorych z DCM jest częściowe usunięcie lewej komory w celu zmniejszenia jej wielkości (operacja Baptiste). Nie tak dawno temu, do leczenia pacjentów z DCMP, opracowano specjalne modele rozruszników serca, które pozwalają na synchroniczną pracę komór serca. Prowadzi to do poprawy wypełnienia komór serca krwią i zwiększenia funkcji pompowania serca. DCM u dzieci wynosi 5-10 przypadków na 100 000 dzieci rocznie. Największy efekt w leczeniu kardiomiopatii rozstrzeniowej u małych dzieci osiąga się przy zastosowaniu kombinacji kortykosteroidów i glikozydów (prednizolonu i digoksyny). Na tle monoterapii prednizolonem następuje zmniejszenie częstości akcji serca. Monoterapia digoksyną prowadzi do zmniejszenia częstoskurczu i duszności. Biorąc pod uwagę niewskazanie przepisywania leków cytostatycznych u małych dzieci, ponieważ zaobserwowano znaczną liczbę powikłań leczenia, w pediatrii bardziej optymalne jest stosowanie długo działających glikozydów nasercowych w połączeniu z hormonami kortykosteroidowymi w kardiomiopatii rozstrzeniowej. Zapobieganie. Zapobieganie DCMP polega na wykluczeniu alkoholu, kokainy, a także uważnym monitorowaniu czynności serca podczas chemioterapii guza. Przydaje się hartowanie ciała od najmłodszych lat. Całkowita abstynencja od alkoholu w alkoholowej DCM poprawia kurczliwość serca i może wyeliminować konieczność przeszczepu serca. 11. Klasyfikacja kardiomiopatii. Etiologia kardiomiopatii przerostowej (HCM) Kardiomiopatia przerostowa (HCM) to niewieńcowa choroba mięśnia sercowego komór (głównie lewej), charakteryzująca się masywnym przerostem ich ścian z występem przegrody międzykomorowej (IVS) do jamy prawej komory, która może ulec znacznemu pogrubieniu , zmniejszenie objętości wewnętrznej komór, prawidłowa lub zwiększona kurczliwość mięśnia sercowego i upośledzona relaksacja (dysfunkcja rozkurczowa). Najczęściej występuje izolowany przerost przegrody międzykomorowej (izolowane przerostowe zwężenie podaortalne – IHSS) lub części wierzchołkowej komór. Klasyfikacja. Klasyfikacja HCM według lokalizacji przerostu (ED Wigle i wsp., 1985 z uzupełnieniami). I. Przerost LV. 1. Przerost asymetryczny, w którym występuje przerost mięśnia sercowego poszczególnych ścian lub odcinków komór (w tym przerost IVS - 90% z utrudnieniem lub bez zwężenia drogi odpływu lewej komory, przerost śródkomorowy - 1%, przerost wierzchołka lewej komory - 3%, wolna ściana przerost lewej komory i tylna część IVS - 1%). 2. Symetryczny (koncentryczny) przerost lewej komory, gdy przerost mięśnia sercowego rozciąga się na wszystkie ściany komór, występuje w 5% przypadków. II. Przerost trzustki. W przypadku, gdy przerost mięśnia sercowego uniemożliwia prawidłowy odpływ krwi z komór serca, mówi się o obturacyjnej postaci HCM. W innych przypadkach HCM nie przeszkadza. Etiologia. Choroba może być zarówno wrodzona, jak i nabyta. Wrodzona HCM jest dziedziczona w sposób autosomalny dominujący. W obrębie tej samej rodziny można zaobserwować różne formy i warianty HCM. Najczęściej dziedziczony jest asymetryczny przerost przegrody międzykomorowej. Nabyta postać HCM występuje u starszych pacjentów z nadciśnieniem tętniczym w wywiadzie. Częstość występowania wynosi 0,02-0,05%. Przyczyny rozwoju przejętego HCM nie są w pełni zrozumiałe. Zgodnie z jedną z zaproponowanych hipotez, u osób z nabytym HCM w okresie prenatalnym rozwija się defekt receptorów adrenergicznych serca zaangażowanych w regulację czynności serca, w szczególności częstości akcji serca. W efekcie znacząco wzrasta wrażliwość na noradrenalinę i podobne hormony, które zwiększają częstość akcji serca, co wpływa na rozwój u nich przerostu mięśnia sercowego, a ostatecznie HCM. patologiczny obraz. Zdezorientowany, nieregularny, chaotyczny układ kardiomiocytów i miofibryli w kardiomiocytach, zwłóknienie mięśnia sercowego jest naruszeniem architektury mięśnia sercowego. 12. Obraz kliniczny i rozpoznanie kardiomiopatii przerostowej (HCM) obraz kliniczny. HCM charakteryzuje się skrajną różnorodnością objawów, co jest przyczyną błędnej diagnozy. O obecności i czasie pojawienia się dolegliwości w HCM decydują głównie 2 czynniki: forma HCM i lokalizacja zmiany. Najpotężniejszą komorą serca jest lewa komora, dlatego z przerostem mięśnia sercowego jego ścian dolegliwości mogą nie pojawiać się przez długi czas. Odosobniona porażka prawej komory serca spotyka się niezwykle rzadko. Obraz kliniczny HCM to: 1) oznaki przerostu mięśnia sercowego komorowego (głównie lewego); 2) oznaka niewystarczającej funkcji rozkurczowej komór; 3) zmienne oznaki niedrożności drogi odpływu lewej komory. Diagnostyka. W procesie poszukiwań diagnostycznych najistotniejsze jest wykrycie szmeru skurczowego, zmiany tętna i przesuniętego rytmu wierzchołka. W diagnostyce HCM największe znaczenie mają dane echokardiograficzne, pozwalające wyjaśnić anatomiczne cechy choroby, nasilenie przerostu mięśnia sercowego, niedrożność drogi odpływu lewej komory. Ujawniają się następujące objawy: asymetryczny przerost IVS, wyraźniejszy w górnej jednej trzeciej, jego hipokineza; skurczowy ruch przedniego płatka zastawki mitralnej w kierunku przednim; kontakt przedniego płatka zastawki mitralnej z IVS w rozkurczu. Niespecyficzne objawy to: przerost lewego przedsionka, przerost tylnej ściany lewej komory, zmniejszenie średniej prędkości rozkurczowej osłony przedniego płatka zastawki mitralnej. Na EKG wszelkie specyficzne zmiany znajdują się tylko przy wystarczająco rozwiniętym przeroście lewej komory. Diagnostyka rentgenowska ma znaczenie dopiero w zaawansowanym stadium choroby, kiedy można stwierdzić wzrost lewej komory i lewego przedsionka, poszerzenie zstępującej części aorty. Na fonokardiogramie zachowane są amplitudy tonów I i II, co jest znakiem różnicowym HCM od zwężenia ujścia aorty, a także wykrywany jest szmer skurczowy o różnym nasileniu. Inwazyjne metody badawcze (sondowanie lewej części serca, angiografia kontrastowa) nie są obecnie obowiązkowe, ponieważ echokardiografia dostarcza informacji, które są dość wiarygodne do postawienia diagnozy. Sondowanie serca jest stosowane pod kontrolą telewizji rentgenowskiej. Technika wykonania metody: poprzez nakłucie dużej tętnicy w znieczuleniu miejscowym z dalszym wprowadzeniem specjalnego cewnika do jamy serca mierzy się gradient ciśnienia (różnicę) między lewą komorą a wychodzącą z niej aortą. Zwykle ten gradient nie powinien być. 13. Leczenie i zapobieganie kardiomiopatii przerostowej (HCM) Leczenie. Farmakoterapia HCM opiera się na lekach poprawiających wypełnienie komór serca w rozkurczu krwią. Leki te to grupa b-blokerów (anaprylina, atenolol, metoprolol i propranolol, 160-320 mg / dzień itp.) oraz grupa antagonistów jonów wapnia (werapamil, ale z ostrożnością). Novokinamide disopyramide zmniejsza również częstość akcji serca i ma działanie antyarytmiczne. Na samym początku leczenia stosuje się małe dawki tych leków, następnie następuje stopniowe zwiększanie dawki do maksimum tolerowanego przez pacjenta. β-blokery stosuje się ostrożnie w przypadku cukrzycy, astmy oskrzelowej i niektórych innych chorób. Podczas leczenia tymi lekami konieczne jest ciągłe monitorowanie ciśnienia krwi i tętna. Spadek ciśnienia poniżej 90/60 mm Hg jest niebezpieczny. Sztuka. i tętno poniżej 55 na minutę. Jeżeli u pacjenta występują niebezpieczne zaburzenia rytmu, których nie można leczyć beta-blokerami ani antagonistami jonów wapnia, wówczas w leczeniu takiego pacjenta stosuje się dodatkowo inne leki antyarytmiczne. Powołanie antykoagulantów jest zalecane w przypadku napadowych arytmii i migotania przedsionków, a także w obecności zakrzepów krwi w komorach serca (warfaryna itp.). W okresie leczenia tymi lekami konieczne jest regularne monitorowanie szeregu wskaźników układu krzepnięcia krwi. Przy znacznym przedawkowaniu leków przeciwzakrzepowych możliwe jest krwawienie zewnętrzne (nosowe, maciczne itp.) I wewnętrzne (krwiaki itp.). Leczenie chirurgiczne wykonuje się u pacjentów z obturacyjnym HCM, gdy leczenie zachowawcze jest nieskuteczne lub gdy gradient między lewą komorą a aortą przekracza 30 mm Hg. Sztuka. (wykonuje się operację miotomii lub myektomii - wycięcie lub usunięcie części przerośniętego mięśnia sercowego lewej komory). Wykonywana jest również wymiana zastawki mitralnej i niechirurgiczna ablacja IVS. Zapobieganie. Wszyscy pacjenci z HCM, szczególnie ci z postacią obturacyjną, są przeciwwskazani w sportach, w których możliwy jest wyraźny wzrost aktywności fizycznej w krótkim czasie (lekkoatletyka, piłka nożna, hokej). Zapobieganie chorobie polega na wczesnej diagnozie, co umożliwia wczesne rozpoczęcie leczenia choroby i zapobieganie rozwojowi ciężkiego przerostu mięśnia sercowego. Echokardiogram należy wykonać u genetycznych krewnych pacjenta. W diagnostyce ważne są również badania przesiewowe EKG i EchoCG, które są przeprowadzane podczas corocznego badania lekarskiego. U pacjentów z obturacyjnym HCM należy prowadzić profilaktykę infekcyjnego zapalenia wsierdzia (profilaktyka antybiotykowa itp.), ponieważ obecność niedrożności stwarza warunki do rozwoju tego zagrażającego życiu stanu. 14. Przyczyny kardiomiopatii restrykcyjnej (RCMP) Kardiomiopatia restrykcyjna (RCMP) - (od łacińskiego słowa restiction - "restrykcja") - grupa chorób mięśnia sercowego i wsierdzia, w których w wyniku wyraźnego zwłóknienia i utraty elastyczności z różnych przyczyn występuje utrwalona ograniczenie napełniania komór w rozkurczu. RCMP obejmuje: ciemieniowe włókniste zapalenie wsierdzia Leflera (występujące w krajach o klimacie umiarkowanym, opisane przez W. Lofflera i in., 1936) oraz zwłóknienie endomiokardialne (występujące w krajach tropikalnej Afryki, opisane przez D. Bedforda i E. Konstmana). Przyczyny RCM. Pierwotny RCM występuje bardzo rzadko, a jedyną udowodnioną przyczyną jego występowania jest tzw. zespół hipereozynofilowy (choroba Lefflera, ciemieniowe włókniste zapalenie wsierdzia Lefflera). Występuje głównie u mężczyzn w wieku 30-40 lat. W przypadku zespołu hipereozynofilowego dochodzi do zapalenia wsierdzia, które z czasem kończy się znacznym zagęszczeniem wsierdzia i jego szorstkim przyleganiem do sąsiedniego mięśnia sercowego, co prowadzi do gwałtownego zmniejszenia rozciągliwości mięśnia sercowego. Zespół Leflera charakteryzuje się także utrzymującą się przez 6 miesięcy lub dłużej eozynofilią (1500 eozynofili na 1 mm3), uszkodzeniem narządów wewnętrznych (wątroba, nerki, płuca, szpik kostny). W zdecydowanej większości przypadków pochodzenie RCMP jest drugorzędne z innych powodów, wśród których najczęstsze to: 1) amyloidoza - choroba związana z naruszeniem metabolizmu białek w organizmie; jednocześnie powstaje nieprawidłowe białko (amyloid) i odkłada się w dużych ilościach w tkankach różnych narządów; gdy serce jest uszkodzone, amyloid powoduje zmniejszenie jego kurczliwości i rozciągliwości; 2) hemochromatoza - naruszenie metabolizmu żelaza w organizmie, któremu towarzyszy zwiększona zawartość żelaza we krwi, jego nadmiar odkłada się w wielu narządach i tkankach, w tym w mięśniu sercowym, powodując w ten sposób zmniejszenie jego rozciągliwości; 3) sarkoidoza – choroba o nieznanej etiologii, charakteryzująca się tworzeniem skupisk komórek (ziarniniaków) w narządach i tkankach; najczęściej dotknięte są płuca, wątroba, węzły chłonne i śledziona; a rozwijające się ziarniniaki w mięśniu sercowym prowadzą do zmniejszenia jego rozciągliwości; 4) choroby wsierdzia (zwłóknienie wsierdzia, fibroelastoza wsierdzia itp.), Gdy występuje znaczne pogrubienie i zagęszczenie wsierdzia, co również prowadzi do ostrego ograniczenia rozciągliwości mięśnia sercowego. W szczególności fibroelastoza wsierdzia może wystąpić tylko u niemowląt; ta choroba nie jest kompatybilna z życiem ze względu na wczesny rozwój ciężkiej niewydolności serca. 15. Obraz kliniczny i rozpoznanie kardiomiopatii restrykcyjnej (RCMP) obraz kliniczny. Objawy choroby są niezwykle polimorficzne i determinują objawy zaburzeń krążenia w małym lub dużym kręgu (w zależności od pierwotnej zmiany prawej lub lewej komory). Skargi mogą być nieobecne lub mogą wynikać z przekrwienia w krążeniu płucnym lub ogólnoustrojowym. Pacjenci zwykle skarżą się na duszność, która pojawia się po raz pierwszy podczas wysiłku, a wraz z postępem choroby duszność obserwuje się w spoczynku. Ze względu na zmniejszenie funkcji pompowania serca pacjent skarży się na zmęczenie i słabą tolerancję na wszelkie obciążenia. Z czasem łączą się obrzęki nóg, powiększona wątroba i opuchlizna brzucha. Okresowo pojawia się nieregularne bicie serca, a wraz z rozwojem uporczywych blokad może dojść do omdlenia. Pierwszy etap rozwoju choroby (martwiczy) charakteryzuje się pojawieniem się gorączki, utraty wagi, kaszlu, wysypki skórnej i tachykardii. Diagnostyka. Rozpoznanie RCM jest niezwykle trudne. Można śmiało mówić o tej patologii dopiero po wykluczeniu szeregu podobnie występujących chorób (takich jak idiopatyczne zapalenie mięśnia sercowego typu Abramova-Fiedlera, wysiękowe zapalenie osierdzia, wada zastawkowa serca). Podczas badania pacjentów z RCMP stwierdza się objawy charakterystyczne dla zastoinowej niewydolności serca (obrzęk, powiększenie wątroby i wodobrzusze), a także wyraźną pulsację żył szyi. Podczas osłuchiwania duże znaczenie ma wykrycie powiększonego serca, cichego późnego szmeru skurczowego i głośnego wczesnego III tonu. Badanie EKG ujawnia umiarkowany przerost mięśnia sercowego, a także różne zaburzenia rytmu i przewodzenia impulsu serca oraz niespecyficzne zmiany załamka T w EKG. Echokardiografia jest jedną z najbardziej pouczających metod diagnozowania choroby, z jej pomocą, pogrubieniem wsierdzia, zmianą charakteru wypełnienia komór serca, zmniejszeniem funkcji pompowania serca, szybkim ruchem przedniego płatka zastawki mitralnej podczas rozkurczu i szybki wczesny ruch tylnej ściany lewej komory na zewnątrz. Rezonans magnetyczny pozwala uzyskać informacje o anatomii serca, określić patologiczne wtrącenia w mięśniu sercowym oraz zmierzyć grubość wsierdzia. Podczas badania parametrów hemodynamiki centralnej określa się podwyższone ciśnienie napełniania w obu komorach, a końcowe ciśnienie w lewej komorze jest wyższe niż w prawej komorze. Wentrykulografia ujawnia wzmożony skurcz lewej komory, gładkie kontury jej ścian, czasami z ubytkiem wypełnienia w wierzchołku (oznaczenie obliteracji). Występują oznaki niedomykalności zastawek, w szczególności zastawki mitralnej lub trójdzielnej. 16. Diagnostyka różnicowa, leczenie i profilaktyka kardiomiopatii restrykcyjnej (RCMP) Diagnostyka różnicowa. W diagnostyce różnicowej RCMP bardzo ważne jest uwzględnienie podobieństwa choroby w zewnętrznych objawach z zaciskającym zapaleniem osierdzia, ale metoda leczenia tych chorób jest diametralnie przeciwna. Żywa biopsja mięśnia sercowego i wsierdzia jest zwykle stosowana jednocześnie z sondowaniem serca, co pozwala uzyskać więcej informacji w celu wyjaśnienia charakteru choroby i dalszego leczenia. W niezwykle rzadkich przypadkach, gdy powyższe metody diagnostyczne nie pozwalają odróżnić RCMP od zaciskającego zapalenia osierdzia, na stole operacyjnym wykonuje się bezpośrednią rewizję osierdzia. Wszyscy pacjenci z RCMP wymagają kompleksowego badania klinicznego, biochemicznego i dodatkowego w celu określenia pozasercowych przyczyn choroby. Leczenie. Leczenie choroby stwarza znaczne trudności. Większość leków stosowanych w leczeniu niewydolności serca może nie przynieść pożądanych rezultatów ze względu na to, że ze względu na charakterystykę choroby niemożliwe jest uzyskanie znaczącej poprawy podatności mięśnia sercowego (w niektórych przypadkach przepisuje się antagonistów jonów wapnia w tym celu). Diuretyki (aldakton) służą do usuwania nadmiaru płynów w organizmie. Aby wyeliminować uporczywe zaburzenia przewodzenia, konieczne może być założenie (implant) stałego rozrusznika serca. Jest to spowodowane chorobami takimi jak sarkoidoza i hemochromatoza, prowadzącymi do rozwoju wtórnego RCMP, podlegają one samoleczeniu. W leczeniu sarkoidozy stosuje się leki hormonalne (prednizolon itp.), A w przypadku hemochromatozy regularne upuszczanie krwi (w celu zmniejszenia stężenia żelaza w organizmie). Leczenie amyloidozy mięśnia sercowego jest bezpośrednio zależne od przyczyn jej wystąpienia. Wskazane jest stosowanie leków przeciwzakrzepowych na zakrzepicę w komorach serca. Leczenie chirurgiczne stosuje się w przypadkach RCMP spowodowanych uszkodzeniem wsierdzia. Podczas operacji, jeśli to możliwe, wycina się część wsierdzia, która uległa zmianom. W niektórych przypadkach, jeśli występuje niewydolność zastawek przedsionkowo-komorowych, wykonuje się ich protetykę. Niektóre formy amyloidowego uszkodzenia mięśnia sercowego leczy się przeszczepem serca. Zapobieganie RCM. Niestety środki zapobiegawcze dla tej choroby są ograniczone. Przede wszystkim konieczne jest wczesne wykrycie potencjalnie usuwalnych przyczyn amyloidozy, sarkoidozy, hemochromatozy itp. Aby osiągnąć te cele, bardzo ważne jest przeprowadzanie corocznego badania lekarskiego populacji. 17. Etiologia infekcyjnego zapalenia wsierdzia (IE) Infekcyjne zapalenie wsierdzia (IE) to choroba polegająca na polipowatościowo-wrzodziejącym uszkodzeniu aparatu zastawkowego serca (często z rozwojem niewydolności zastawkowej) lub wsierdziu ciemieniowym (rzadziej dotyczy to śródbłonka aorty lub najbliższej dużej tętnicy ). Choroba jest wywoływana przez różne patogenne mikroorganizmy i towarzyszy jej ogólnoustrojowa zmiana narządów wewnętrznych (nerki, wątroba, śledziona) na tle zmienionej reaktywności organizmu. Etiologia. Patogennymi czynnikami sprawczymi choroby są najczęściej grupa kokosowa mikroorganizmów - paciorkowce (wcześniej wyizolowano streptococcus Viridans w 90% przypadków), gronkowce (złote, białe), enterokoki, pneumokoki. W ostatnich latach, w związku z powszechnym stosowaniem antybiotyków, zmienił się zakres patogenów drobnoustrojowych. Chorobę może wywołać flora Gram-ujemna (Escherichia coli, Pseudomonas aeruginosa, Proteus, Klebsiella); udowodniono ważną rolę patogennych grzybów, Sarcinus, Brucella i wirusów. Choroby wywoływane przez te patogeny mają cięższy przebieg, szczególnie zapalenie wsierdzia spowodowane infekcją grzybiczą (zwykle pojawia się na skutek nieracjonalnego stosowania antybiotyków). Jednak u części pacjentów nie udaje się wykryć prawdziwego czynnika wywołującego chorobę (częstotliwość ujemnych wyników posiewów krwi wynosi 20-50%). Często dochodzi do infekcji w miejscu protezy zastawki – tzw. protetyczna IE, która rozwija się głównie w ciągu 2 miesięcy po operacji wymiany zastawki serca. W tym przypadku czynnik sprawczy choroby najczęściej ma charakter paciorkowcowy. Tak więc źródła infekcji i bakteriemii w IE są bardzo zróżnicowane (chirurgia jamy ustnej, zabiegi chirurgiczne i diagnostyczne w obrębie układu moczowo-płciowego, operacje układu sercowo-naczyniowego (w tym wymiana zastawki), przedłużony pobyt cewnika w żyle, częste wlewy dożylne i badania metodami endoskopowymi, przewlekła hemodializa (przeciek tętniczo-żylny), dożylne podawanie leków). Istnieją tak zwane pierwotne IE, które rozwinęły się na nienaruszonych zastawkach, a także IE na tle wrodzonych i nabytych zmian w sercu i jego aparacie zastawkowym - wtórne zapalenie wsierdzia. Zmiany te umożliwiają wyodrębnienie chorych na odrębne grupy ryzyka: wady serca (wrodzone i nabyte), wypadanie płatka zastawki mitralnej, tętniaki tętniczo-żylne, tętniaki pozawałowe, przecieki, stan po operacjach serca i dużych naczyń. 18. Patogeneza i klasyfikacja zakaźnego zapalenia wsierdzia (IE) Patogeneza. Mechanizm rozwoju IE jest złożony i niewystarczająco zbadany. W rozwoju choroby można wyróżnić 3 etapy. Etap I (zakaźny-toksyczny) przebiega z różnym stopniem nasilenia zatrucia. Następuje rozwój bakterii, niszczenie zastawek, co prowadzi do rozwoju chorób serca; na tym samym etapie proces jest często uogólniany z powodu hematogennego rozprzestrzeniania się infekcji - kawałki guzków lub kolonii drobnoustrojów mogą oddzielić się od zastawki, guzki mogą pęknąć. Etap II - immunozapalny, w którym drobnoustroje utrwalone na zastawkach powodują przedłużoną autouczulenie i hiperergiczne uszkodzenie narządów i tkanek organizmu (uogólnienie immunologiczne procesu). Etap III - dystroficzny - występuje wraz z postępem procesu patologicznego: zaburzone są funkcje wielu narządów, dochodzi do niewydolności serca i nerek, dodatkowo pogarszając przebieg choroby (patrz tabela). Tabela Klasyfikacja IE
Rozróżnia się również aktywne i nieaktywne (uzdrowione) IE. Istnieje również klasyfikacja chirurgiczna, w której wyróżniają: 1) zmiana ogranicza się do płatków zastawki; 2) zmiana rozciąga się poza zastawkę. Ostra IZW (szybko postępująca, rozwija się w ciągu 8-10 tygodni) występuje rzadko, zwykle u osób, które wcześniej nie chorowały na serce, i klinicznie objawia się obrazem ogólnej sepsy. Podostre IE (najczęściej) trwa 3-4 miesiące, przy odpowiedniej terapii lekowej może dojść do remisji. Przewlekłe IE utrzymuje się przez wiele miesięcy z okresami zaostrzeń i remisji, charakteryzuje się łagodnymi objawami klinicznymi. Przy niekorzystnym przebiegu pojawiają się poważne powikłania, a pacjenci umierają z powodu postępującej niewydolności serca, zwiększając zatrucie septyczne. 19. Obraz kliniczny i diagnostyka infekcyjnego zapalenia wsierdzia (IE) obraz kliniczny. Objawy IZW są przedstawiane jako zespoły. 1. Zespół zmian zapalnych i posocznicy. 2. Zespół ogólnego zatrucia organizmu. 3. Zespół uszkodzenia zaworu. 4. Zespół „laboratoryjnych” zaburzeń immunologicznych. 5. Zespół powikłań zakrzepowo-zatorowych. 6. Zespół uogólnienia zmian. Rozpoznanie IZW opiera się przede wszystkim na wczesnym wykryciu czynnika sprawczego choroby. W tym celu wykorzystuje się następujące badania laboratoryjne i instrumentalne. 1. Uzyskanie dodatniego posiewu krwi. 2. Przeprowadzenie NBT (test nitrobluetetrazolium). 3. Kliniczne badanie krwi w celu wykrycia wskaźników ostrej fazy: można wykryć wzrost ESR do 50 mm / h lub więcej, leukocytozę z przesunięciem formuły leukocytów w lewo lub (w stadium II) leukopenię i niedokrwistość hipochromiczną. 4. Identyfikacja zmian immunologicznych. 5. Badanie moczu wykonuje się w celu wyjaśnienia zmian w różnych narządach i układach, gdy wykryte zostanie kłębuszkowe zapalenie nerek, objawiające się białkomoczem, cylindrurią i krwiomoczem. 6. Bezpośredni znak diagnostyczny IE - obecność roślinności na zastawkach serca - jest wykrywany za pomocą echokardiografii. Tak więc z całej gamy objawów należy wyróżnić główne i dodatkowe. Główne kryteria rozpoznania IE: 1) gorączka z temperaturą powyżej 38°C z dreszczami; 2) Plamy Lukina; 3) guzki Oslera; 4) zapalenie wsierdzia na niezmienionych zastawkach (pierwotne) lub na tle reumatycznych i wrodzonych wad serca. zakaźne zapalenie mięśnia sercowego; 5) mnoga tętnicza choroba zakrzepowo-zatorowa, pęknięcia tętniaków grzybiczych z krwotokami; 6) splenomegalia; 7) dodatni posiew krwi; 8) wyraźny pozytywny efekt stosowania antybiotyków. Dodatkowe kryteria rozpoznania IE: 1) podwyższenie temperatury ciała do 38°C, wyziębienie; 2) krwotoki na skórze; 3) szybka utrata wagi; 4) asymetryczne zapalenie stawów drobnych stawów rąk, stóp; 5) anemizacja; 6) ESR powyżej 40 mm/h; 7) ostro dodatnia SRV; 8) obecność czynnika reumatoidalnego; 9) a-globuliny powyżej 25%; 10) wzrost zawartości immunoglobulin M, E i A. 20. Leczenie i zapobieganie infekcyjnemu zapaleniu wsierdzia (IE) Leczenie. Leczenie IZW powinno być jak najwcześniejsze i etiotropowe, biorąc pod uwagę dane bakteriologiczne. Wskazane jest połączenie leczenia zachowawczego i chirurgicznego. W leczeniu IZW we wszystkich grupach wiekowych stosuje się przede wszystkim antybiotyki, które działają bakteriobójczo na mikroorganizmy. Lekiem pierwszego wyboru nadal jest penicylina. Dzienna dawka - do 20 000 000 IU podawana jest dożylnie i domięśniowo. Nie należy jednak wykluczać, że u pacjentów w wieku podeszłym i starczym przy leczeniu penicyliną i innymi antybiotykami w dużych dawkach często obserwuje się działanie kardiotoksyczne. Przy nieznanej etiologii leczenie rozpoczyna się od wysokich dawek benzylopenicyliny domięśniowo lub dożylnie do 18 000 000-20 000 000 jednostek lub więcej, kombinacji ze streptomycyną do 1 g / m dziennie lub aminoglikozydami (gentamycyna, tobramycyna w ilości 4-6 mg / dzień) stosuje się kg na dzień). Cefalosporyny są również podstawowymi lekami stosowanymi w leczeniu IZW: najczęściej stosowane są klaforan, cefamizyna (4-10 g/dobę domięśniowo i dożylnie) oraz zeporyna (10-16 g/dobę) i kefzol (do 8-10 g dożylnie) itp.). Fusydyna ma dobre działanie przeciwgronkowcowe, w niektórych przypadkach jest skuteczna w oporności drobnoustrojów na inne antybiotyki (2-3 g/dobę). Leczenie antybiotykami jest przepisywane przez długi czas w ciągu 1,5-2 miesięcy, aż do całkowitego wyeliminowania infekcji. Przy zmniejszonej immunoreaktywności organizmu środki przeciwbakteryjne łączy się z immunoterapią pasywną za pomocą immunomodulatorów (tymalina, T-aktywina itp.). Aby zapobiec zakrzepicy, na przykład w przypadku zapalenia wsierdzia, które rozwinęło się na tle posocznicy angiogennej, tworzy się kontrolowaną hipokoagulację za pomocą heparyny (20 000–25 000 jednostek dożylnie lub podskórnie). W celu hamowania enzymów proteolitycznych stosuje się contrical (do 40 000-60 000 jednostek dożylnie). Gdy IE zastawkowe przyczyniły się do powstania wady zastawkowej serca lub objawy choroby nie ustępują pomimo masywnej antybiotykoterapii, wskazane jest przeprowadzenie leczenia operacyjnego. Głównym celem operacji jest zachowanie własnej zastawki pacjenta. Czasem ograniczają się do usunięcia roślinności, zszycia pęknięć zastawek itp. Jeśli zastawka pod wpływem infekcji zostanie prawie całkowicie zniszczona, zastępuje się ją sztuczną (protezą) przy użyciu protez mechanicznych i biologicznych. Zapobieganie. Zapobieganie IE polega na terminowym oczyszczeniu przewlekłych ognisk infekcji w jamie ustnej, migdałkach, nosogardzieli, zatokach przynosowych, zastosowaniu aktywnej antybiotykoterapii w ostrych chorobach paciorkowcowych i gronkowcowych (zapalenie migdałków itp.). Zaleca się utwardzenie ciała. 21. Etiologia astmy oskrzelowej (BA) Do tej pory nie istnieje wyczerpująca definicja astmy, jednak najpełniejszą definicję tej choroby podał G. B. Fedoseev w 1982 roku. Astma oskrzelowa (BA) jest niezależną, przewlekłą, nawracającą chorobą z pierwotnym uszkodzeniem dróg oddechowych, głównym i obowiązkowym mechanizmem patogenetycznym jest zmieniona reaktywność oskrzeli spowodowana specyficznymi (immunologicznymi) i (lub) niespecyficznymi, wrodzonymi lub nabytymi mechanizmami, a głównym (obowiązkowym) objawem klinicznym jest atak astmy i (lub) stan astmatyczny ( stan astmatyczny) z powodu skurczu mięśni gładkich oskrzeli, nadmiernego wydzielania, dyskrynii i obrzęku błony śluzowej oskrzeli. Etiologia. W występowaniu astmy ważną rolę odgrywa połączenie kilku czynników. Pod tym względem istnieją 2 formy astmy - atopowa (od łacińskiej atopii - „dziedziczna predyspozycja”) i zakaźno-alergiczna. Dziedziczna predyspozycja wynika z powiązania niektórych antygenów zgodności tkankowej (HCA) z ciężkością astmy, a nasilenie choroby szczególnie często obserwuje się u nosicieli antygenów B35 i B40. Czynnikami wewnętrznymi w rozwoju choroby są biologiczne wady układu odpornościowego, hormonalnego, autonomicznego układu nerwowego, wrażliwość i reaktywność oskrzeli, klirens śluzowo-rzęskowy, śródbłonek naczyń płucnych, system szybkiej odpowiedzi (komórki tuczne itp.), metabolizm kwasu arachidonowego, itp. Czynniki zewnętrzne obejmują: 1) alergeny zakaźne (wirusy, bakterie, grzyby, drożdże itp.); 2) alergeny niezakaźne (pyłki, kurz, przemysłowe, lecznicze, spożywcze; alergeny kleszczy, owadów i zwierząt); 3) drażniące mechaniczne i chemiczne (metal, drewno, krzemiany, pyły bawełniane; opary kwasów, zasad; opary itp.); 4) czynniki meteorologiczne i fizykochemiczne (zmiany temperatury i wilgotności powietrza, wahania ciśnienia barometrycznego, pola magnetycznego Ziemi, wysiłek fizyczny itp.); 5) stresujące, neuropsychiczne skutki i aktywność fizyczna. Czynniki zakaźne mogą mieć nie tylko działanie alergizujące, ale także obniżać próg wrażliwości organizmu na alergeny niezakaźne (atopowe), zwiększać dla nich przepuszczalność błony śluzowej dróg oddechowych; w celu wytworzenia zmiany w reaktywności komórek docelowych (komórki tuczne, bazofile, monocyty itp.) i układów efektorowych. 22. Patogeneza astmy oskrzelowej (BA) Patogeneza. Zmieniona reaktywność oskrzeli jest centralnym ogniwem w patogenezie choroby i może mieć charakter pierwotny i wtórny. W pierwszym przypadku zmiana reaktywności jest wrodzona i nabyta. Wtórne zmiany reaktywności oskrzeli są przejawem zmian reaktywności układu odpornościowego, hormonalnego i nerwowego organizmu. Mówiąc więc o patogenezie AD, możemy wyróżnić 2 grupy mechanizmów: immunologiczny i nieimmunologiczny. Typ I (atopowy, reaginiczny lub anafilaktyczny). W odpowiedzi na spożycie antygenów egzoalergenowych (pyłek, białka zwierzęce i roślinne, bakterie i leki) dochodzi do zwiększonej produkcji (reagin), które są utrwalane i gromadzone na komórkach tucznych (pierwotnych komórkach efektorowych). To jest immunologiczny etap AD. Następnie rozwija się patochemiczny etap procesu - degranulacja komórek tucznych z uwolnieniem substancji wazoaktywnych, skurczowych i chemotaktycznych (histamina, serotonina, różne czynniki chemotaktyczne itp.). Pod wpływem substancji biologicznie czynnych rozpoczyna się patofizjologiczny etap patogenezy: zwiększa się przepuszczalność złoża mikrokrążenia, co prowadzi do rozwoju obrzęku, surowiczego zapalenia i skurczu oskrzeli. Reakcja typu III (typ immunokompleksowy, czyli zjawisko Artusa) rozwija się pod wpływem egzoalergenów i endoalergenów. Reakcja zachodzi w strefie nadmiaru antygenu z udziałem wytrącających się przeciwciał należących do immunoglobulin klas O i M. Szkodliwe działanie utworzonego kompleksu antygen-przeciwciało jest realizowane poprzez aktywację dopełniacza, uwalnianie enzymów lizosomalnych. Występuje uszkodzenie błon podstawnych, skurcz mięśni gładkich oskrzeli, rozszerzenie naczyń krwionośnych i zwiększenie przepuszczalności mikronaczyń. Typ IV (nadwrażliwość komórkowa typu opóźnionego) charakteryzuje się tym, że uczulone limfocyty mają działanie niszczące. W tym przypadku mediatorami reakcji alergicznej są limfokiny (działają na makrofagi, komórki nabłonkowe), enzymy lizosomalne i aktywowany układ kininowy. Pod wpływem tych substancji rozwija się obrzęk, obrzęk błony śluzowej, skurcz oskrzeli, nadprodukcja lepkiej wydzieliny oskrzelowej. Mechanizmy nieimmunologiczne są podstawową zmianą reaktywności oskrzeli w wyniku wrodzonych i nabytych wad biologicznych. Mechanizmy nieimmunologiczne działają na pierwotne lub wtórne komórki efektorowe lub na receptory mięśni gładkich oskrzeli, naczyń krwionośnych, komórek gruczołów oskrzelowych. Zmienia to reaktywność komórek docelowych, a przede wszystkim komórek tucznych, czemu towarzyszy nadmierna produkcja substancji biologicznie czynnych (histamina, leukotrieny itp.). Ostatnio mówi się o szczególnej roli niedoboru glikokortykosteroidów i zaburzeń dysowarianicznych w patogenezie zaburzeń obturacji oskrzeli. Niedobór glikokortykosteroidów prowadzi do rozwoju nadreaktywności komórek tucznych, zmniejszonej syntezy katecholamin, aktywacji prostaglandyn F2a, a także zaburzeń układu odpornościowego. 23. Klasyfikacja astmy oskrzelowej (BA) Klasyfikacja. Przewaga jednego lub drugiego mechanizmu w patogenezie AD umożliwia rozróżnienie jej różnych cech patogenetycznych. Obecnie stosowana jest klasyfikacja zaproponowana przez G. B. Fedoseeva (1982). Etapy rozwoju AD. I - stan przed astmą (stany zagrażające rozwojowi: ostre i przewlekłe zapalenie oskrzeli, ostre i przewlekłe zapalenie płuc z elementami skurczu oskrzeli w połączeniu z naczynioruchowym nieżytem nosa, pokrzywką). II - klinicznie ukształtowane BA (uznawane za takie po pierwszym ataku lub natychmiastowym wystąpieniu stanu astmatycznego). Formy licencjackie: 1) immunologiczne; 2) nieimmunologiczne. Mechanizmy patogenetyczne (warianty kliniczne i patogenetyczne) AD: 1) atopowy; 2) zależne od infekcji; 3) autoimmunologiczny; 4) dyshormonalne; 5) brak równowagi neuropsychicznej; 6) zaburzenia równowagi adrenergicznej; 7) brak równowagi cholinergicznej; 8) pierwotna zmieniona reaktywność oskrzeli. Ciężkość BA: 1) łagodny przebieg (zaostrzenia są rzadkie, 2-3 razy w roku, krótkotrwałe ataki astmy są zatrzymywane przez przyjmowanie różnych leków rozszerzających oskrzela); 2) umiarkowane (częstsze zaostrzenia 3-4 razy w roku, ataki astmy są cięższe i zatrzymywane przez zastrzyki leków); 3) ciężki przebieg (charakteryzujący się częstymi i długotrwałymi zaostrzeniami, ciężkimi atakami, często przechodzącymi w stan astmatyczny). Fazy progresji astmy: 1) zaostrzenie (obecność nawracających ataków astmy lub stanu astmatycznego); 2) ustępujące zaostrzenie (ataki stają się rzadsze i łagodniejsze, fizyczne i czynnościowe objawy choroby są mniej wyraźne niż w fazie zaostrzenia); 3) remisja (ustępują typowe objawy astmy: nie występują napady astmy, drożność oskrzeli zostaje całkowicie lub częściowo przywrócona). komplikacje: 1) płuc: rozedma, niewydolność płuc, niedodma, odma opłucnowa, stan astmatyczny itp.; 2) pozapłucne: serce płucne (skompensowane i zdekompensowane rozwojem prawokomorowej niewydolności serca), dystrofia mięśnia sercowego itp. 24. Diagnostyka różnicowa astmy oskrzelowej (BA) Diagnostyka różnicowa. BA różni się od astmy sercowej (patrz Tabela 1). Tabela 1 Diagnostyka różnicowa AD
25. Leczenie i profilaktyka astmy oskrzelowej (BA) Leczenie. W leczeniu astmy zaleca się podejście etapowe (krok 1 – najmniejsze nasilenie astmy, krok 4 – największe). Etap 1: Łagodny, przerywany przebieg, w którym objawy astmy pojawiają się po ekspozycji na wyzwalacz (np. pyłek lub sierść zwierząt) lub z powodu ćwiczeń. Leczenie polega na przyjmowaniu leków profilaktycznych w razie potrzeby (przepisywane są leki wziewne – agoniści, kromoglikan, nedokromil lub leki antycholinergiczne). Jeśli astma objawia się częstszymi objawami, wzrostem zapotrzebowania na leki rozszerzające oskrzela, konieczne staje się przejście do następnego etapu. Etap 2. Lekko uporczywy kurs. Terapia podstawowa obejmuje leki przeciwzapalne, wziewne kortykosteroidy, kromoglikan sodu lub nedokromil sodu. W przypadku cięższych i długotrwałych zaostrzeń podaje się krótki cykl doustnych kortykosteroidów. Etap 3 charakteryzuje się umiarkowanym nasileniem BA. Tacy pacjenci wymagają codziennego przyjmowania profilaktycznych leków przeciwzapalnych. Dawka kortykosteroidów wziewnych wynosi 800-2000 mcg w połączeniu z długo działającymi lekami rozszerzającymi oskrzela. Etap 4. Ciężka astma, gdy nie jest całkowicie kontrolowana. W takim przypadku celem leczenia jest osiągnięcie jak najlepszych rezultatów. Leczenie pierwotne polega na wyznaczeniu wziewnych kortykosteroidów w dużych dawkach. Cięższe zaostrzenie może wymagać leczenia doustnymi kortykosteroidami, które są przepisywane w minimalnych dawkach lub co drugi dzień. Aby zapobiec rozwojowi skutków ubocznych, wysokie dawki kortykosteroidów wziewnych podaje się przez spejser. Krok 5 obejmuje zmniejszenie dawki leków wspomagających. Jest to możliwe, jeśli astma pozostaje pod kontrolą przez co najmniej 3 miesiące, co pozwala zmniejszyć ryzyko wystąpienia działań niepożądanych i zwiększa podatność chorego na zaplanowane leczenie. "Redukcja" leczenia odbywa się pod stałą kontrolą objawów, objawów klinicznych i wskaźników funkcji oddechowych poprzez stopniowe zmniejszanie (anulowanie) ostatniej dawki lub dodatkowych leków. Zapobieganie. Profilaktyka pierwotna astmy obejmuje leczenie pacjentów w stanie przedastmowym, wykrywanie wad biologicznych u praktycznie zdrowych osób z obciążoną dziedzicznością zagrażających zachorowaniu na astmę, eliminację potencjalnie niebezpiecznych alergenów, substancji drażniących i innych. czynniki, które mogą prowadzić do rozwoju choroby ze środowiska pacjenta. Podczas leczenia pacjentów w stanie przedastmatycznym konieczne jest odkażenie ognisk infekcji, leczenie alergicznej rinozinusopatii, zastosowanie różnych metod leczenia nielekowego, w tym akupunktury i psychoterapii, terapii ruchowej, baroterapii, leczenia uzdrowiskowego. Przedstawiono przeprowadzanie odczulania specyficznego i niespecyficznego. 26. Etiologia i patogeneza przewlekłego zapalenia oskrzeli (CB) Przewlekłe obturacyjne zapalenie oskrzeli jest rozlaną niealergiczną zmianą zapalną drzewa oskrzelowego, spowodowaną długotrwałym działaniem drażniącym na oskrzela różnymi czynnikami, która ma postępujący przebieg i charakteryzuje się obturacyjną wentylacją płucną, tworzeniem śluzu i funkcją drenażową oskrzeli drzewo, które objawia się kaszlem, plwociną i dusznością. Przewlekłe zapalenie oskrzeli dzieli się na pierwotne i wtórne. Pierwotne przewlekłe zapalenie oskrzeli jest niezależną chorobą, która nie jest związana z innymi procesami oskrzelowo-płucnymi lub uszkodzeniem innych narządów i układów, w której występuje rozlana zmiana w drzewie oskrzelowym. HB wtórna rozwija się na tle innych chorób – zarówno płucnych, jak i pozapłucnych. Etiologia. W rozwoju CB odgrywają rolę czynniki egzogenne. Zespół obturacyjny rozwija się w wyniku połączenia wielu czynników: 1) skurcz mięśni gładkich oskrzeli w wyniku drażniącego działania czynników egzogennych i zmian zapalnych błony śluzowej; 2) nadmierne wydzielanie śluzu, zmiany jego właściwości reologicznych, prowadzące do zakłócenia transportu śluzowo-rzęskowego i zablokowania oskrzeli lepką wydzieliną; 3) metaplazja nabłonka od cylindrycznego do wielowarstwowego płaskonabłonkowego i jego przerost; 4) naruszenia produkcji środka powierzchniowo czynnego; 5) obrzęk zapalny i naciek błony śluzowej; 6) zapadnięcie się małych oskrzeli i zatarcie oskrzelików; 7) zmiany alergiczne w błonie śluzowej. Różne stosunki zmian w błonie śluzowej powodują powstawanie pewnej postaci klinicznej: 1) w przypadku nieobturacyjnego nieobturacyjnego zapalenia oskrzeli przeważają powierzchowne zmiany właściwości strukturalnych i funkcjonalnych błony śluzowej; 2) w przypadku śluzowo-ropnego (ropnego) zapalenia oskrzeli dominują procesy zakaźnego zapalenia. Jednak możliwa jest również sytuacja, w której długotrwałe nieżytowe zapalenie oskrzeli spowodowane dodaniem infekcji może stać się śluzowo-ropne itp. W nieobturacyjnej odmianie wszystkich klinicznych postaci przewlekłego zapalenia oskrzeli zaburzenia wentylacji są nieznacznie nasilone; 3) zaburzenia obturacyjne początkowo pojawiają się tylko na tle zaostrzenia choroby i są spowodowane zmianami zapalnymi w oskrzelach, hiper- i dyskrynii, skurczem oskrzeli (odwracalne elementy niedrożności), ale potem utrzymują się stale, podczas gdy zespół obturacyjny rośnie powoli. 27. Obraz kliniczny przewlekłego zapalenia oskrzeli (CB) obraz kliniczny. Główne objawy HB to kaszel, produkcja plwociny, duszność. Wraz z zaostrzeniem choroby lub niedotlenieniem z rozwojem niewydolności płuc i innymi powikłaniami ujawniają się objawy ogólne (pocenie się, osłabienie, gorączka, zmęczenie itp.). Kaszel jest najbardziej typowym objawem choroby. Zgodnie z jej naturą i konsystencją plwociny można przyjąć wariant przebiegu choroby. W przypadku nieobturacyjnego wariantu nieżytowego zapalenia oskrzeli kaszelowi towarzyszy wydzielanie niewielkiej ilości śluzowej wodnistej plwociny (częściej rano, po wysiłku lub z powodu zwiększonego oddychania). Na początku choroby kaszel nie przeszkadza pacjentowi; pojawienie się napadowego kaszlu wskazuje na rozwój niedrożności oskrzeli. Kaszel nabiera odcienia szczekania i ma charakter napadowy z wyraźnym zapadnięciem się tchawicy i dużych oskrzeli. W przypadku ropnego i śluzowo-ropnego zapalenia oskrzeli pacjenci bardziej martwią się odkrztuszaniem plwociny. W przypadku zaostrzenia choroby plwocina nabiera charakteru ropnego, jej ilość wzrasta, czasami plwocina jest z trudem wydalana (z powodu niedrożności oskrzeli podczas zaostrzenia). W obturacyjnym wariancie zapalenia oskrzeli kaszel jest nieproduktywny i hacking, któremu towarzyszy duszność, z niewielką ilością plwociny. Duszność występuje u wszystkich pacjentów z przewlekłym zapaleniem oskrzeli w różnym czasie. Pojawienie się duszności u pacjentów z "długotrwałym kaszlem" początkowo ze znacznym wysiłkiem fizycznym wskazuje na dodanie niedrożności oskrzeli. W miarę postępu choroby duszność staje się bardziej wyraźna i stała, tj. rozwija się niewydolność oddechowa (płucna). W wariancie nieobturacyjnym CB postępuje powoli, duszność zwykle pojawia się po 20-30 latach od zachorowania. Tacy pacjenci prawie nigdy nie naprawiają początku choroby, a jedynie wskazują na pojawienie się powikłań lub częstych zaostrzeń. Istnieje historia nadwrażliwości na zimno, a większość pacjentów zgłasza długotrwałe palenie. U wielu pacjentów choroba wiąże się z zagrożeniami zawodowymi w miejscu pracy. Analizując historię kaszlu, należy upewnić się, że pacjent nie ma innej patologii aparatu oskrzelowo-płucnego (gruźlica, guzy, rozstrzenie oskrzeli, pylica płuc, choroby ogólnoustrojowe tkanki łącznej itp.), której towarzyszą te same objawy. Czasami historia wskazuje na krwioplucie z powodu łagodnej wrażliwości błony śluzowej oskrzeli. Nawracające krwioplucie wskazuje na krwotoczną postać zapalenia oskrzeli. Ponadto krwioplucie w przewlekłym, długotrwałym zapaleniu oskrzeli może być pierwszym objawem raka płuca lub rozstrzenia oskrzeli. 28. Diagnoza przewlekłego zapalenia oskrzeli (CB) Diagnostyka. Osłuchiwanie ujawnia ciężki oddech (wraz z rozwojem rozedmy może ulec osłabieniu) i suche rzężenia o charakterze rozlanym, których barwa zależy od kalibru dotkniętych oskrzeli (świszczący oddech, dobrze słyszalny po wydechu, jest charakterystyczny dla zmian małych oskrzeli) . Wraz z zaostrzeniem obturacyjnego zapalenia oskrzeli wzrasta duszność, nasila się zjawisko niewydolności oddechowej. W zaawansowanych przypadkach przewlekłego zapalenia oskrzeli i z dodatkowymi powikłaniami pojawiają się objawy rozedmy płuc, niewydolności oddechowej i serca (prawej komory) - pojawiają się niewyrównane serce płucne: akrocyjanoza, stwardnienie lub obrzęk nóg i stóp, zmiany w obrębie paznokci forma okularów zegarkowych i końcowych paliczków dłoni i stóp - w postaci pałeczek perkusyjnych, obrzęk żył szyjnych, pulsacja w nadbrzuszu z powodu prawej komory, akcent II tonu w II międzyżebrowym przestrzeń po lewej stronie mostka, powiększenie wątroby. Wskaźniki laboratoryjne i instrumentalne mają różny stopień istotności w zależności od etapu procesu. Badanie rentgenowskie narządów klatki piersiowej jest wykonywane u wszystkich pacjentów z przewlekłym zapaleniem oskrzeli, jednak na zdjęciach radiologicznych z reguły nie stwierdza się zmian w płucach. Może wystąpić deformacja siatki wzoru płuc, z powodu rozwoju pneumosklerozy. Badanie rentgenowskie odgrywa ważną rolę w diagnostyce powikłań (ostre zapalenie płuc, rozstrzenie oskrzeli) oraz w diagnostyce różnicowej z chorobami o podobnych objawach. Bronchografia służy wyłącznie do diagnozowania rozstrzenia oskrzeli. Bronchoskopia ma duże znaczenie w diagnostyce przewlekłego zapalenia oskrzeli i jego różnicowaniu z chorobami o podobnym obrazie klinicznym. Potwierdza obecność procesu zapalnego; wyjaśnia charakter zapalenia; ujawnia zaburzenia czynnościowe drzewa tchawiczo-oskrzelowego; pomaga w identyfikacji zmian organicznych drzewa oskrzelowego. Badanie funkcji oddychania zewnętrznego prowadzi się w celu identyfikacji restrykcyjnych i obturacyjnych zaburzeń wentylacji płuc. Zgodnie ze spirogramem obliczany jest indeks Tiffno oraz wskaźnik prędkości powietrza – PSDV. Łączna ocena oporności oskrzeli i objętości płuc również pomaga w określeniu stopnia niedrożności. Radiopulmonografia z użyciem radioaktywnego izotopu 133Xe jest wykonywana w celu wykrycia nierównej wentylacji związanej z niedrożnością małych oskrzeli. Elektrokardiografia jest niezbędna do wykrycia przerostu prawej komory i prawego przedsionka, który rozwija się wraz z nadciśnieniem płucnym. W klinicznym badaniu krwi stwierdza się wtórną erytrocytozę będącą wynikiem przewlekłego niedotlenienia z rozwojem ciężkiej niewydolności płuc. Wskaźniki „fazy ostrej” są wyrażane umiarkowanie. Badanie mikrobiologiczne plwociny i treści oskrzelowej jest ważne dla określenia etiologii zaostrzenia przewlekłego zapalenia oskrzeli i wyboru terapii przeciwdrobnoustrojowej. 29. Diagnostyka różnicowa przewlekłego zapalenia oskrzeli (CB) stół Różnicowe kryteria diagnostyczne dla CB
30. Leczenie przewlekłego zapalenia oskrzeli (CB) Leczenie. Obejmuje zestaw środków, które różnią się w okresie zaostrzenia i remisji choroby. Podczas zaostrzenia przewlekłego zapalenia oskrzeli rozróżnia się dwa kierunki leczenia: etiotropowy i patogenetyczny. Leczenie etiotropowe ma na celu wyeliminowanie procesu zapalnego w oskrzelach: wskazana jest terapia antybiotykami, lekami sulfanilamidowymi, antyseptycznymi, fitoncydami itp. Leczenie rozpoczyna się od antybiotyków z serii penicylin (penicylina, ampicylina) lub grupy cefalosporyn (cefamezyna , tseporin), a przy braku efektu stosuje się rezerwę antybiotyków z grupy (gentamycyna itp.). Najkorzystniejszą drogą podania jest droga dotchawicza (aerozol lub napełnienie strzykawką krtaniową przez bronchoskop). Leczenie patogenetyczne ma na celu poprawę wentylacji płuc; przywrócenie drożności oskrzeli; kontrola nadciśnienia płucnego i niewydolności prawej komory. Przywrócenie wentylacji płucnej, oprócz eliminacji procesu zapalnego w oskrzelach, ułatwia tlenoterapia i terapia ruchowa. Najważniejsze w leczeniu przewlekłego zapalenia oskrzeli - przywrócenie drożności oskrzeli - osiąga się poprzez poprawę ich drenażu i wyeliminowanie skurczu oskrzeli. Aby poprawić drenaż oskrzeli, przepisywane są środki wykrztuśne (gorący napój alkaliczny, wywary z ziół, mukaltin itp.), leki mukolityczne (acetylocysteina, bromheksyna; z ropną lepką wydzieliną - aerozole enzymów proteolitycznych - chymopsin, trypsyna); stosuje się bronchoskopię terapeutyczną. Aby wyeliminować skurcz oskrzeli, stosuje się eufilinę (dożylnie, w czopkach, tabletkach), efedrynę, atropinę; możliwe są pojedyncze wizyty w aerozolu leków sympatykomimetycznych: fenoterol, siarczan orcyprenaliny (astmopenta) i nowy lek domowy „Soventol”, leki antycholinergiczne: atrovent, troventol. Skuteczne preparaty przedłużonej aminofiliny (teopec, teodur, theobelong itp.) - 2 razy dziennie. W przypadku braku efektu takiej terapii, małe dawki kortykosteroidów podaje się doustnie (10-15 mg prednizolonu dziennie) lub dotchawiczo (zawiesina hydrokortyzonu - 50 mg). Jako dodatkową terapię przepisywane są: 1) leki przeciwkaszlowe: z bezproduktywnym kaszlem - libexin, tusuprex, bromheksyna, z kaszlem hackingiem - kodeina, dionina, stoptussin; 2) leki zwiększające odporność organizmu: witaminy A, C, grupa B, stymulanty biogenne. Obecnie w leczeniu przewlekłego zapalenia oskrzeli coraz częściej stosuje się leki immunokorekcyjne: T-aktywinę lub tymalinę (100 mg podskórnie przez 3 dni); wewnątrz - katergen, nukleinian sodu lub pentoksyl (w ciągu 2 tygodni), lewamizol (dekaris). Zabieg fizjoterapeutyczny: przepisać diatermię, elektroforezę chlorku wapnia, kwarc na klatkę piersiową, masaż klatki piersiowej i ćwiczenia oddechowe. 31. Zapalenie płuc. Etiologia, patogeneza, klasyfikacja Zapalenie płuc jest ostrą chorobą zakaźną i zapalną o charakterze ogniskowym, w której w proces patologiczny zaangażowane są sekcje oddechowe i śródmiąższowa tkanka łączna płuc. Klasyfikacja E.V. Gembitsky'ego (1983). Według etiologii: 1) bakteryjny (wskazujący na patogen); 2) wirusowy (wskazujący na patogen); 3) zrogowaciały; 4) riketsjalny; 5) mykoplazma; 6) grzybicze; 7) mieszane; 8) zakaźno-alergiczny; 9) nieznana etiologia. Według patogenezy: 1) podstawowy; 2) wtórne. Charakterystyka kliniczna i morfologiczna: 1) miąższowy: krupowy; ogniskowy; 2) pełnoekranowy. Według lokalizacji i zasięgu: jednostronne; dwustronny. Według ciężkości: wyjątkowo ciężki; ciężki; umiarkowany; łagodny i nieudany. Downstream: ostry; przedłużony (radiologiczne i kliniczne ustąpienie zapalenia płuc). Etiologia. Większość zapaleń płuc ma pochodzenie zakaźne. Zapalenie płuc alergiczne i wywołane działaniem czynników fizycznych lub chemicznych jest rzadkie. Bakteryjne zapalenie płuc jest częściej diagnozowane u osób w średnim i starszym wieku; wirusowe zapalenie płuc - u młodych ludzi. W etiologii pierwotnego bakteryjnego zapalenia płuc wiodącą rolę odgrywają pneumokoki. Podczas epidemii grypy wzrasta rola związków wirusowo-bakteryjnych (najczęściej gronkowców), a także mikroorganizmów oportunistycznych. We wtórnym zapaleniu płuc wiodącą rolę etiologiczną odgrywają bakterie Gram-ujemne (klebsiella pneumoniae i pałeczka grypy); w występowaniu zachłystowego zapalenia płuc duże znaczenie ma infekcja beztlenowa. Patogeneza. Czynnik zakaźny wchodzi z zewnątrz do odcinków oddechowych płuc przez oskrzela: wdech i aspiracja (z nosogardzieli lub jamy ustnej). Drogą krwiopochodną patogen wnika do płuc głównie we wtórnym zapaleniu płuc lub w zakrzepowej genezie zapalenia płuc. Limfogenne rozprzestrzenianie się infekcji z początkiem zapalenia płuc obserwuje się tylko przy urazach klatki piersiowej. Duże znaczenie w patogenezie zapalenia płuc mają także reakcje alergiczne i autoalergiczne. 32. Diagnoza zapalenia płuc Najistotniejsze dla diagnozy jest obecność zespołu zmian zapalnych w tkance płucnej. Zespół ten składa się z następujących objawów: 1) opóźnienie w oddychaniu dotkniętej chorobą strony klatki piersiowej; 2) skrócenie dźwięku perkusyjnego w obszarze projekcji zmiany w większym lub mniejszym stopniu; 3) wzmożone drżenie głosu i bronchofonia w tym samym obszarze; 4) zmiana charakteru oddychania (twardy, oskrzelowy, osłabiony itp.); 5) pojawienie się patologicznych odgłosów oddechowych (mokre, dźwięczne, drobne bulgoczące rzęsy i trzeszczenie). Natura oddychania może się zmieniać na różne sposoby. W początkowej fazie krupowego zapalenia płuc oddychanie może być osłabione, z przedłużonym wydechem; w fazie hepatyzacji wraz ze wzrostem przytępienia dźwięku perkusji słychać oddech oskrzelowy; przy rozdzielczości ogniska płucnego ze spadkiem otępienia perkusyjnego oddychanie staje się trudne. Objawy pomagają postawić diagnozę etiologiczną: 1) wykrycie wysypki o małych plamkach, jak w przypadku różyczki, w połączeniu z limfadenopatią jest charakterystyczne dla infekcji adenowirusem; 2) miejscowe powiększenie węzłów chłonnych wskazuje na okołoogniskowe zapalenie płuc; 3) grzybicze zapalenie płuc połączone ze zmianami błon śluzowych, skóry i paznokci; 4) zespół wątrobowo-płucny i lekka żółtaczka występują w zapaleniu płuc w przebiegu kornitu i Curickettsi; 5) w przypadku typowego krupowego zapalenia płuc charakterystyczny jest wygląd pacjenta: blada twarz z gorączkowym rumieńcem po stronie zmiany, wykwity opryszczkowe, obrzęk skrzydeł nosa podczas oddychania. Najważniejszą metodą wyjaśnienia obecności zapalenia płuc i stopnia zaangażowania tkanki płucnej w proces jest fluorografia wielkoformatowa i badanie rentgenowskie narządów klatki piersiowej. Bronchografia ujawnia próchnicę w tkance płucnej, a także obecność rozstrzeni oskrzeli, wokół której w czasie zaostrzenia możliwe są zmiany naciekowe (perifocal pneumonia). Badanie bakteriologiczne plwociny (lub popłuczyn oskrzelowych) przed wyznaczeniem antybiotyków pomaga wykryć patogen i określić jego wrażliwość na antybiotyki. Nasilenie procesu zapalnego ocenia się na podstawie nasilenia parametrów krwi ostrej fazy i ich dynamiki (leukocytoza ze zmianą wzoru leukocytów, wzrost ESR, zwiększona zawartość globulin a2, fibrynogen, pojawienie się CRP, wzrost poziomu kwasów sialowych). Przy przedłużającym się przebiegu zapalenia płuc i rozwoju powikłań badana jest reaktywność immunologiczna organizmu. 33. Leczenie zapalenia płuc Leczenie. Natychmiast po postawieniu diagnozy konieczne jest rozpoczęcie terapii etiotropowej zapalenia płuc. Duże znaczenie mają wyobrażenia empiryczne dotyczące możliwego patogenu, ponieważ badanie bakteriologiczne plwociny jest prowadzone od dłuższego czasu i u większości pacjentów, nawet przy nowoczesnym podejściu do tego badania, daje niepewne, a czasem błędne wyniki. Obecnie penicyliny straciły na znaczeniu jako lek z wyboru w leczeniu zapalenia płuc. W związku z powyższym w leczeniu zapalenia płuc dużą wagę przywiązuje się do makrolidów, które okazały się skuteczne nie tylko przeciwko pneumokokom, ale także przeciwko Mycoplasma pneumoniae, Chlamydia pneumoniae. Dawkowanie antybiotyków stosowanych w leczeniu zapalenia płuc. 1. Penicyliny: penicylina benzylowa (500 000-1 000 000 IU dożylnie co 6-8 godzin lub 500 000-1 000 000 IU co 4 godziny domięśniowo), ampicylina (0,5-1,0-2,0 g domięśniowo co 6-8 godzin lub 0,5 g co 6 godzin dożylnie), amoksycylina (0,5-1,0 g co 8 godzin doustnie lub 0,5-1,0 g co 8-12 godzin domięśniowo, dożylnie), oksacylina (0,5 g co 4-6 godzin doustnie, domięśniowo, dożylnie). 2. Cefalosporyny: I generacja - cefalotyna (keflin) (0,5-2,0 g co 4-6 godzin domięśniowo, dożylnie), cefazolina (kefzol) (0,5-2,0 g, co 8 godzin domięśniowo, dożylnie), II generacja - cefuroksym (zinacef , ketocef) (0,75-1,5 g co 6-8 godzin domięśniowo, dożylnie), III generacja - cefotaksym (klaforan) (1,0-2,0 g, maksymalnie do 12 g/dobę co 12 godzin domięśniowo, dożylnie), ceftriakson (longacef, rocefina) (1,0-2,0-4,0 g co 24 godziny domięśniowo, dożylnie). 3. Aminoglikozydy: Genetamycyna (80 mg co 12 godzin IM, IV), Amikacin (10-15 mg/kg co 12 godzin IM, IV), Tobramycyna (Brulamycin) (3-5 mg/kg co 8 godzin IM, IV) . 4. Makrolidy: erytromycyna (0,5 g co 6-8 godzin doustnie lub 0,5-1,0 g co 6-8 godzin dożylnie), rovamycyna (3,0 mln j.m. co 8-12 godzin doustnie lub 1,5-3,0 mln j.m. co 8-12 godzin godziny dożylnie). 5. Fluorochinolony: pefloksacyna (leflacyna) (400 mg co 12 godzin doustnie, i.v.), cyprofloksacyna (cyprobay) (500 mg co 12 godzin doustnie lub 200-400 mg co 12 godzin dożylnie), ofloksacyna (zanocin, tarivid) (200 mg co 12 godzin doustnie). 6. Tetracykliny: doksycyklina (wibramycyna) (200 mg w 1. dobie, w kolejnych dniach – 100 mg co 24 h doustnie), minocyklina (minocyna) (200 mg w 1. dobie, w kolejnych dniach – 100 mg co 12 h doustnie), aztreonam (azactam) (1,0-2,0 g co 8-12 godzin), imipenem/cylstatyna (tienam) (500 mg co 6-8 godzin domięśniowo). 34. Etiologia, patogeneza, obraz kliniczny ostrego zapalenia przełyku Ostre zapalenie przełyku to zmiana zapalna błony śluzowej przełyku trwająca od kilku dni do 2-3 miesięcy. Etiologia i patogeneza. Czynniki etiologiczne: choroby zakaźne, urazy, oparzenia, zatrucia, reakcje alergiczne, błędy żywieniowe. Spośród czynników zakaźnych najbardziej charakterystyczne dla ostrego zapalenia przełyku są błonica, szkarlatyna, dur brzuszny i tyfus, grypa, paragrypa, infekcja adenowirusowa, świnka. Fizyczne i chemiczne czynniki uszkadzające są reprezentowane przez promieniowanie jonizujące, oparzenia chemiczne, gorące i bardzo zimne potrawy oraz przyprawy. obraz kliniczny. Nieżytowe zapalenie przełyku jest najczęstszą postacią ostrego zapalenia przełyku. Występuje na tle błędów w żywieniu: podczas jedzenia pikantnych, zimnych, gorących potraw, z niewielkimi obrażeniami, poparzeniami alkoholu. Klinicznie objawia się pieczeniem i bólem za mostkiem, zmuszając pacjentów do odmowy jedzenia przez kilka dni. Endoskopowo stwierdzono zapalenie przełyku I-II stopnia, prześwietlenie - hiperkinezja przełyku. Erozyjne zapalenie przełyku występuje w przypadku chorób zakaźnych i alergii. Objawy kliniczne są podobne do objawów nieżytowego zapalenia przełyku. Krwotoczne zapalenie przełyku jest rzadką kliniczną postacią nadżerkowego zapalenia przełyku. Etiologia jest taka sama jak w przypadku nadżerkowego zapalenia przełyku. Klinicznie typowe są zespół silnego bólu i krwawe wymioty. W klinice dominuje dysfagia i silny ból, nasilający się po jedzeniu, nudnościach, wymiotach. Z wymiocinami uwalniane są filmy fibrynowe, może wystąpić krwioplucie. Błonowe (złuszczające) zapalenie przełyku według etiologii jest chemiczne (oparzenia przełyku), zakaźne. W klinice ciężkiego błoniastego zapalenia przełyku przeważa zatrucie, dysfagia i zespół bólowy. Martwicze zapalenie przełyku jest rzadką postacią ostrego zapalenia przełyku. Jego rozwojowi sprzyja obniżona odporność w tak poważnych chorobach jak posocznica, dur brzuszny, kandydoza, schyłkowa niewydolność nerek. Klinika charakteryzuje się bolesną dysfagią, wymiotami, ogólnym osłabieniem, krwawieniem, częstym rozwojem zapalenia śródpiersia, zapalenia opłucnej, zapalenia płuc. Septyczne zapalenie przełyku jest rzadkim miejscowym lub rozlanym zapaleniem ścian przełyku o etiologii paciorkowcowej lub gdy błona śluzowa jest uszkodzona przez ciało obce, z oparzeniami, owrzodzeniami i może przejść z sąsiednich narządów. Czasami ostre zapalenie przełyku występuje jako powikłanie jakiejkolwiek postaci ostrego zapalenia przełyku, prowadzące do ropnej fuzji ścian przełyku. Obraz kliniczny charakteryzuje się silnym zatruciem, wysoką gorączką, bólem za mostkiem i karkiem, wymiotami. W badaniu występuje obrzęk szyi, ruchomość w tej części kręgosłupa jest ograniczona. Pozycja głowy jest wymuszona, pochylona na bok. Choroba często przechodzi w ropne zapalenie śródpiersia. 35. Leczenie i rokowanie ostrego zapalenia przełyku Leczenie. Zasady leczenia ostrego zapalenia przełyku: etiotropowe, patogenetyczne i objawowe. Leczenie etiotropowe - leczenie choroby podstawowej. W chorobach zakaźnych powikłanych ostrym zapaleniem przełyku stosuje się antybiotyki (pozajelitowo). Przy wyraźnych zmianach martwiczych i krwotocznych w przełyku zaleca się powstrzymanie się od jedzenia przez 2-3 tygodnie. W tym okresie wskazane jest żywienie pozajelitowe, dożylne podawanie hydrolizatów białkowych, mieszanin aminokwasów, intralipidów, witamin oraz terapia detoksykacyjna. Po zmniejszeniu stanu zapalnego przepisywane są pokarmy oszczędzające termicznie i chemicznie: ciepłe mleko, śmietana, zupy warzywne, płynne płatki zbożowe. Aby zmniejszyć miejscowe objawy stanu zapalnego - wewnątrz roztworów taniny 1%, collargol - 2%, novocaine - 1-2% przed posiłkami. Środki ściągające są przyjmowane w pozycji poziomej z nisko opuszczoną głową łóżka. W przypadku braku działania miejscowego podawania preparatów ściągających, nie-narkotyczne środki przeciwbólowe są przepisywane pozajelitowo. Aby zmniejszyć skutki dyskinezy przełyku, leki prokinetyczne (cerucal, raglan, cyzapryd) stosuje się doustnie przed posiłkami. W przypadku wielu erozji wskazane są preparaty bizmutu (denol, vikair), zastrzyki solcoseryl. W krwotocznym zapaleniu przełyku, powikłanym krwawieniem, stosuje się preparaty kwasu aminokapronowego, vikasol, dicynone. W przypadku masywnego krwawienia zalecana jest transfuzja krwi lub osocza. W przypadku ropnego, martwiczego zapalenia przełyku pacjent powinien być przez długi czas żywiony pozajelitowo, stosuje się masową terapię kilkoma antybiotykami, a ropień jest drenowany. Zwężenia przełyku są korygowane przez bougienage. W rzadkich przypadkach zakłada się gastrostomię. Prognoza. Rokowanie nieżytowego i nadżerkowego zapalenia przełyku jest korzystne. Możliwe jest samoistne zniknięcie objawów zapalenia przełyku pod warunkiem, że choroba podstawowa zostanie odpowiednio skorygowana. Rokowanie w przypadku rzekomobłoniastego, złuszczającego zapalenia przełyku jest poważne. We wszystkich przypadkach, z zastrzeżeniem wyzdrowienia z choroby podstawowej, zapalenie przełyku kończy się powstaniem zwężeń bliznowatych, które wymagają dalszej korekty. Pacjenci z ciężkimi postaciami zapalenia przełyku powikłanymi zwężeniami przełyku są niezdolni do pracy. Zapobieganie ostremu zapaleniu przełyku polega na odpowiedniej i terminowej diagnozie i leczeniu choroby podstawowej. 36. Etiologia, patogeneza, obraz kliniczny przewlekłego zapalenia przełyku Przewlekłe zapalenie przełyku to przewlekłe zapalenie błony śluzowej przełyku trwające do 6 miesięcy. Najczęstszym wariantem jest zapalenie przełyku (refluksowe zapalenie przełyku), które może być powikłane chorobą wrzodową przełyku. Etiologia i patogeneza. Główną przyczyną choroby jest ciągłe cofanie się treści żołądkowej do przełyku, czasem żółci i treści jelitowej, czyli zapalenie przełyku jest aseptycznym oparzeniem przełyku przez kwas żołądkowy. W patogenezie refluksowego zapalenia przełyku ważne są niedomykalność kwaśnej treści i naruszenie jej oczyszczania i opróżniania przełyku. Istnieje pięć kryteriów patogeniczności refluksu w genezie zapalenia przełyku: częstotliwość, objętość, niedomykalność, skład chemiczny, stan błony śluzowej przełyku i wrażliwość na czynnik chemiczny (zapalenie ścian zmniejsza wrażliwość), szybkość opróżniania (klirens) , który zależy głównie od aktywnej perystaltyki, alkalizującego działania śliny i śluzu. Występowaniu refluksowego zapalenia przełyku sprzyja przepuklina przełykowego ujścia przepony, wrzód dwunastnicy, zaburzenia po gastroresekcji, alergie. Predyspozycje alergiczne również mają znaczenie. W badaniu morfologicznym pacjentów z zapaleniem przełyku stwierdzono obrzęk, przekrwienie błony śluzowej, naciekanie błony podśluzowej nadprzeponowego odcinka przełyku. obraz kliniczny. Typowe objawy refluksowego zapalenia przełyku to pieczenie za mostkiem, zgaga, niedomykalność, którą nasila leżenie, dysfagia oraz pozytywny efekt przyjmowania leków zobojętniających. Po jedzeniu może wystąpić ból za mostkiem, przypominający dusznicę bolesną. Występowanie bólu w refluksowym zapaleniu przełyku wiąże się z podrażnieniem trawiennym ściany przełyku i jej skurczami podczas zarzucania kwaśnej treści żołądkowej, a także z naruszeniem wypadniętej błony śluzowej. Charakterystyczne cechy tego bólu: jego długi, palący charakter, lokalizacja w wyrostku mieczykowatym, napromieniowanie wzdłuż przełyku, rzadziej do lewej połowy klatki piersiowej, brak zauważalnego efektu przyjmowania leków zobojętniających, przeciwskurczowych, nasilonych w pozycji poziomej, zwłaszcza po jedzenie. Szczególną uwagę w diagnostyce klinicznej należy zwrócić na drobne objawy dysfagii, takie jak uczucie guzka za mostkiem, uczucie gorącego pokarmu przechodzącego przez przełyk. Oznaką stopniowo rozpoczynającego się zapalenia przełyku może być ślinotok i nawyk picia wody z jedzeniem. Badanie fizykalne pacjentów z refluksowym zapaleniem przełyku nie dostarcza informacji istotnych diagnostycznie. Powikłania refluksowego zapalenia przełyku obejmują krwawienie, owrzodzenie, zwężenia, skrócenie przełyku i nowotwór złośliwy. Przewlekłe refluksowe zapalenie przełyku może prowadzić do rozwoju osiowej przepukliny rozworu przełykowego. 37. Diagnoza, leczenie przewlekłego zapalenia przełyku Diagnostyka i diagnostyka różnicowa. Najcenniejszą metodą badawczą tej patologii jest endoskopia, podczas której odnotowuje się przekrwienie, obrzęk i pogrubienie fałdów błony śluzowej. Konieczne jest różnicowanie refluksowego zapalenia przełyku z chorobą wrzodową żołądka i dwunastnicy, chorobą wieńcową, przewlekłym zapaleniem pęcherzyka żółciowego i zapaleniem trzustki. Wiodącym objawem w diagnostyce różnicowej jest ból. Różnicowaniu z chorobą wrzodową pomaga brak późnych i „głodnych” bólów w zapaleniu przełyku, a także dane uzyskane z endoskopii przełyku i żołądka. Ból wieńcowy, w przeciwieństwie do zapalenia przełyku, charakteryzuje się powiązaniem ze stresem fizycznym i emocjonalnym, działaniem azotanów, objawami niedokrwienia na zapis EKG, w tym według ergometrii rowerowej. Dane ultrasonograficzne narządów jamy brzusznej pomagają wykluczyć patologię pęcherzyka żółciowego i trzustki jako przyczyny zespołu bólowego. Leczenie. Terapia refluksowego zapalenia przełyku obejmuje leczenie chorób, które je spowodowały, oraz wyznaczenie terapii przeciwrefluksowej. Pacjentom zaleca się unikanie podnoszenia ciężarów, schylania się. Podczas odpoczynku i snu konieczne jest przyjęcie prawidłowej pozycji (zagłówek podnosi się o 15-20 cm, pod kątem 30-50). Zaleca się normalizację masy ciała, jedzenie ułamkowe (ostatni posiłek - 3 godziny przed snem). Alkohol i pikantne potrawy są wyłączone z diety. Przypisz adsorbenty i leki alkalizujące, które mają działanie ochronne na błonę śluzową. Substancje te obejmują Venter, który podaje się doustnie w dawce 1 g (najlepiej w postaci zawiesiny) 30-40 minut przed posiłkiem 3 razy dziennie i 4 raz na czczo przed snem. Przebieg leczenia wynosi 8-10 tygodni. Podobny efekt mają Almagel, phosphalugel, maalox, gastal. Leki te stosuje się w okresie międzytrawiennym (1/2-2 godziny po posiłkach iw nocy) aż do całkowitej remisji. Phosphalugel i Maalox są przepisywane 1-2 opakowania 2-3 razy dziennie, gastal - 2-3 tabletki dziennie. Nie zaleca się stosowania sody herbacianej, mieszanki glinki Bourget, białej ze względu na niewystarczającą wydajność. Otulające i ściągające działanie ma azotan bizmutu 1 g 3-4 razy dziennie. Zaobserwowano wysoką aktywność przeciwrefluksową nowego środka zobojętniającego kwas, topalkan. Wody mineralne - "Borjomi", "Essentuki nr 4", "Jermuk", "Smirnovskaya" mają działanie alkalizujące. Aby zmniejszyć kwaśne wydzielanie żołądka, przepisuje się blokery receptora histaminowego H2 (cymetydyna, ranitydyna, famotydyna), inhibitory Ka-K-ATPazy (omeprazol), selektywny bloker receptorów M-cholinergicznych komórek okładzinowych i jego analog buskopan. Prognozowanie i zapobieganie. Prognozy na życie i pracę są korzystne. W skomplikowanym przebiegu o rokowaniu decyduje terminowość i jakość opieki medycznej. Pacjentom z ciężkim przebiegiem przypisuje się grupę niepełnosprawności. Pacjenci z przewlekłym refluksowym zapaleniem przełyku powinni znajdować się pod nadzorem gastroenterologa. Co najmniej 2 razy w roku wskazane są badania endoskopowe i morfologiczne ze względu na możliwość nowotworu złośliwego. 38. Wrzód trawienny przełyku Wrzód trawienny przełyku to ostra lub przewlekła choroba charakteryzująca się owrzodzeniem błony śluzowej dalszego odcinka przełyku pod wpływem aktywnego soku żołądkowego. Etiologia i patogeneza. Przewlekłe wrzody trawienne przełyku to powikłania refluksowego zapalenia przełyku i przepukliny rozworu przełykowego. Ich występowanie ułatwiają wewnętrzny krótki przełyk, ogniskowa metaplazja błony śluzowej, heterotopia błony śluzowej żołądka do przełyku, choroba refluksowa z niewydolnością serca, choroby towarzyszące częstym wymiotom (zespół po wagotomii, zespół pętli aferentnej, przewlekły alkoholizm). Obraz kliniczny. Objawy wrzodu trawiennego przełyku przypominają obraz kliniczny trawiennego zapalenia przełyku: uporczywa zgaga, nasilająca się po jedzeniu, podczas zginania ciała, w pozycji leżącej, niedomykalność, ból podczas połykania i utrudnione wydalanie stałego pokarmu. Objawy kliniczne perforacji są nie do odróżnienia od objawów ostrego penetrującego i niepenetrującego urazu mechanicznego przez ciała obce. Około 14% owrzodzeń przełyku przenika do otaczających tkanek. Diagnostyka i diagnostyka różnicowa. Na podstawie objawów klinicznych niezwykle trudno jest podejrzewać wrzód trawienny. Diagnoza jest weryfikowana w trakcie badań instrumentalnych i laboratoryjnych. Najbardziej pouczające badanie rentgenowskie i endoskopowe. Najbardziej wiarygodne informacje w weryfikacji choroby wrzodowej przełyku dostarcza endoskopia i biopsja wielokrotna z brzegów wrzodu. Podczas przesuwania endoskopu do wrzodu trawiennego ujawniają się objawy zapalenia przełyku w stadium I-IV, dysfunkcja motoryczna przełyku, obrzęk okołoogniskowy i przekrwienie błony śluzowej. Konieczne jest odróżnienie wrzodów trawiennych przełyku od owrzodzeń o określonym charakterze (z gruźlicą, kiłą). W takich sytuacjach znacząco pomagają specyficzne testy serologiczne, wyniki badań histologicznych i bakteriologicznych. Połączenie patologii przełyku z uszkodzeniem płuc i innych narządów powoduje, że konieczne jest celowe zbadanie pacjenta w odniesieniu do określonego procesu. Leczenie. Leczenie obejmuje wyznaczenie diety: zaleca się pokarm oszczędzający mechanicznie i chemicznie, który przyjmuje się w małych porcjach 5-6 razy dziennie. Aby zapobiec cofaniu się treści z żołądka do przełyku, pacjent powinien być ułożony w łóżku z podniesionym zagłówkiem. Leki przyjmuje się w pozycji leżącej. Przypisz monoterapię lekiem jednej z następujących grup farmakologicznych: przeciwwydzielnicze, w tym leki zobojętniające sok żołądkowy i adsorbenty, stymulanty funkcji motoryczno-ewakuacyjnej żołądka (prokinetyka), leki - symulatory śluzu. Terapię prowadzi się przez długi czas - 1,5-3 miesiące. Wskazania do leczenia operacyjnego - brak gojenia w ciągu 6-9 miesięcy, przebieg skomplikowany (perforacja, penetracja, zwężenie, krwawienie). Prognozowanie i zapobieganie. Prognozy na życie i pracę są korzystne. 39. Etiologia, patogeneza, obraz kliniczny przewlekłego zapalenia żołądka Przewlekłe zapalenie błony śluzowej żołądka jest chorobą, która klinicznie charakteryzuje się niestrawnością żołądka, a morfologicznie - zmianami zapalnymi i zwyrodnieniowymi błony śluzowej żołądka, zaburzeniami procesów odnowy komórek oraz wzrostem liczby komórek plazmatycznych i limfocytów we własnej błonie śluzowej. Etiologia i patogeneza. Na obecnym etapie rozwoju gastroenterologii ustalono, że pojawienie się przewlekłego zapalenia żołądka jest promowane przez ekspansję drobnoustrojów Helicobacter pylori (HP), która powoduje antralne zapalenie żołądka w 95% przypadków i zapalenie żołądka w 56% przypadków. Czynniki etiologiczne przewlekłego zapalenia błony śluzowej żołądka można z dużą pewnością przypisać czynnikom ryzyka (nieregularna niezbilansowana dieta, palenie tytoniu, spożycie alkoholu, nadmierne wydzielanie kwasu solnego i pepsyny). Wiodącą rolę w rozwoju choroby odgrywają również mechanizmy autoimmunologiczne, którym towarzyszy nagromadzenie przeciwciał przeciwko komórkom okładzinowym błony śluzowej żołądka, pogorszenie dziedziczności, a także stosowanie leków, które mają szkodliwy wpływ na błonę śluzową żołądka. Klasyfikacja. W 1990 roku na IX Międzynarodowym Kongresie Gastroenterologów w Australii przyjęto nową systematyzację przewlekłego zapalenia żołądka, zwaną systemem Sydney. Histologiczne podstawy klasyfikacji. 1. Etiologia: przewlekłe zapalenie żołądka związane z HP, autoimmunologiczne, idiopatyczne, ostre polekowe zapalenie żołądka. 2. Topografia: antral, dno, zapalenie żołądka. 3. Morfologia: formy ostre, przewlekłe, specjalne. Endoskopowe podstawy klasyfikacji: 1) zapalenie żołądka antrum żołądka; 2) zapalenie żołądka ciała żołądka; 3) zapalenie żołądka; 4) zmiany w błonie śluzowej żołądka: obrzęk, rumień, podatność błony śluzowej, wysięk, nadżerki płaskie, uniesione nadżerki, przerost fałdów, zanik fałdów, widoczność układu naczyniowego, krwotoki nadśluzówkowe. obraz kliniczny. Przewlekłe zapalenie żołądka jest jedną z najczęstszych chorób w klinice chorób wewnętrznych. Jego częstotliwość wśród mieszkańców kuli ziemskiej waha się od 28 do 75%. Przewlekłe zapalenie żołądka częściej objawia się objawami niestrawności żołądka i bólu w okolicy nadbrzusza. Rzadko przebiega bezobjawowo. Równie ważne miejsce w obrazie klinicznym przewlekłego zapalenia żołądka zajmuje zespół dyspeptyczny: nudności, odbijanie (kwaśne, gorzkie, zgniłe), zgaga, zaparcia lub biegunka, niestabilne stolce. W przypadku izolowanego antralnego zapalenia żołądka najważniejsze stają się dolegliwości zgagi i zaparć, wynikające z nadmiernego wydzielania kwasu solnego i pepsyny. 40. Diagnostyka i leczenie przewlekłego zapalenia żołądka Diagnostyka. Przewlekłe zapalenie żołądka płynie przez długi czas, z nasileniem objawów w czasie. Zaostrzenia są prowokowane przez zaburzenia żywieniowe. Fizyczny obraz przewlekłego zapalenia żołądka jest raczej słaby. U 80-90% pacjentów podczas zaostrzenia choroby obiektywne badanie określa jedynie miejscowy ból w okolicy nadbrzusza. Gdy przewlekłe zapalenie błony śluzowej żołądka łączy się z zapaleniem dwunastnicy, zapaleniem pęcherzyka żółciowego lub zapaleniem trzustki, można określić lokalizację bólu, który nie jest typowy dla zapalenia żołądka, ale charakterystyczny dla patologii innego narządu. Badanie rentgenowskie jest bardziej prawdopodobne, aby wykluczyć inne choroby żołądka (wrzody, nowotwory), pomóc w diagnozie choroby Menetriera niż potwierdzić rozpoznanie przewlekłego zapalenia żołądka. Ze względu na brak objawów klinicznych choroby, a także niespecyficzność badań laboratoryjnych, rozpoznanie przewlekłego zapalenia żołądka opiera się na wynikach badań endoskopowych i morfologicznych. Endoskopia ujawnia zmiany w nasileniu błony śluzowej żołądka o różnym nasileniu: obrzęk, rumień, wrażliwość błony śluzowej, wysięk, płaskie nadżerki, uniesione nadżerki, przerost lub zanik fałdów, widoczność układu naczyniowego, krwotoki podśluzówkowe. Objawy kliniczne charakterystyczne dla zapalenia żołądka obserwuje się również w innych chorobach przewodu pokarmowego, dlatego w procesie diagnozy konieczne jest badanie ultrasonograficzne jamy brzusznej, dokładne badanie endoskopowe i morfologiczne narządów trawiennych. Leczenie. Pacjenci z zapaleniem żołądka potrzebują ogólnych środków medycznych: regularnego zrównoważonego odżywiania, normalizacji reżimu pracy i odpoczynku, wyrównania stresujących sytuacji planu domowego i przemysłowego. Terapia lekowa jest wskazana tylko w przypadku objawów klinicznych przewlekłego zapalenia żołądka. Pacjenci z zapaleniem błony śluzowej żołądka związanym z HP leczeni są według programu leczenia choroby wrzodowej (patrz następny wykład). Osoby z autoimmunologicznym zapaleniem błony śluzowej żołądka potrzebują witaminy B12 (500 mcg raz dziennie podskórnie przez 1 dni, a następnie powtarzane cykle leczenia), kwasu foliowego (30 mg dziennie), kwasu askorbinowego (do 5 g dziennie). W razie potrzeby przeprowadza się terapię zastępczą preparatami enzymatycznymi (mezim-forte, festal, enzistal, creon, pancitrate, acidin-pepsyna). Zespół bólowy zwykle zatrzymuje się przez wyznaczenie leków zobojętniających (maalox, almagel, gastal) lub blokerów receptora H-histaminowego (ranitydyna, famotydyna) w średnich dawkach terapeutycznych. W przypadku specjalnych postaci zapalenia żołądka konieczne jest leczenie choroby podstawowej. Prognozowanie i zapobieganie. Prognozy na życie i pracę są korzystne. Zapobieganie zapaleniu żołądka ogranicza się do racjonalnego odżywiania, przestrzegania reżimu pracy i odpoczynku, ograniczenia przyjmowania NLPZ. 41. Etiologia wrzodu żołądka Wrzód trawienny (wrzód trawienny) jest przewlekłą, nawracającą chorobą, klinicznie objawiającą się funkcjonalną patologią strefy żołądkowo-dwunastniczej, a morfologicznie - naruszeniem integralności jej warstwy śluzowej i podśluzówkowej, a zatem wrzód zawsze goi się z tworzeniem blizna. Etiologia. Głównym czynnikiem etiologicznym wrzodu trawiennego jest ekspansja mikrobiologiczna HP na powierzchni nabłonka żołądka. Znaczenie agresji bakteryjnej w etiologii choroby badano od 1983 r., kiedy to J. Warren i B. Marshall donieśli o odkryciu dużej liczby bakterii S-spirali na powierzchni nabłonka jamy żołądka. Helicobacteria są w stanie egzystować w środowisku kwaśnym dzięki produkcji enzymu ureazy, który przekształca mocznik (z krwiobiegu) w amoniak i dwutlenek węgla. Produkty hydrolizy enzymatycznej neutralizują kwas solny i stwarzają warunki do zmiany pH środowiska wokół każdej komórki bakteryjnej, zapewniając tym samym dogodne warunki dla żywotnej aktywności mikroorganizmów. Nie mniej ważne w rozwoju wrzodów trawiennych są efekty neuropsychiczne, predyspozycje dziedziczne, czynniki zakaźne, błędy żywieniowe i przyjmowanie niektórych leków oraz złe nawyki. Czynniki dziedziczne są popularne wśród badaczy: bezwładność głównych procesów nerwowych, specyficzne dla grupy właściwości krwi, cechy immunologiczne i biochemiczne, zespół obciążenia dziedzicznego. W występowaniu choroby wrzodowej duże znaczenie miały zaburzenia odżywiania. Jednak badania kliniczne i eksperymentalne przeprowadzone w ciągu ostatnich dwóch dekad w większości przypadków nie wykazały szkodliwego wpływu produktów spożywczych na błonę śluzową żołądka i dwunastnicy. O wiodącej roli czynników żywieniowych świadczy również występowanie choroby wrzodowej żołądka wśród znaczących grup osób o odmiennych nawykach żywieniowych. Zaburzenia rytmu i regularności żywienia, długie przerwy między posiłkami, przedwczesne jedzenie są niezbędne do wystąpienia wrzodów trawiennych. Badacze wyrazili stosunkowo sprzeczne poglądy na temat roli alkoholu we wrzodzieniu. Wiadomo, że alkohol powoduje zmiany zanikowe w błonie śluzowej żołądka. Obserwacje te stoją w sprzeczności z ogólną koncepcją owrzodzenia. Aktywnie badana jest rola efektów leczniczych we wrzodzieniu. Opublikowane w piśmiennictwie wyniki badań oraz dane własne wskazują, że najsilniejsze właściwości wrzodziejące mają niesteroidowe leki przeciwzapalne i hormony glikokortykosteroidowe. 42. Diagnoza wrzodu żołądka Diagnostyka. W nieskomplikowanym przebiegu choroby wrzodowej nie ma zmian w ogólnym badaniu krwi, możliwe jest pewne zmniejszenie ESR, niewielka erytrocytoza. Wraz z komplikacjami pojawia się niedokrwistość w badaniach krwi, leukocytoza - gdy otrzewna jest zaangażowana w proces patologiczny. Nie ma zmian w ogólnej analizie moczu. Tradycyjną metodą badań w patologii żołądka jest określenie kwasowości treści żołądkowej. Możliwe są różne wskaźniki: podwyższone i normalne, w niektórych przypadkach nawet obniżone. Wrzód dwunastnicy występuje przy wysokiej kwasowości soku żołądkowego. W badaniu rentgenowskim wrzód trawienny jest „niszą” - magazynem zawiesiny baru. Gastroduodenoskopia z biopsją jest najbardziej wiarygodną metodą diagnozowania choroby wrzodowej. Pozwala ocenić charakter zmian w błonie śluzowej na krawędzi owrzodzenia, w strefie okołowrzodowej i gwarantuje trafność diagnozy na poziomie morfologicznym. Badania endoskopowe i morfologiczne wykazały, że większość owrzodzeń żołądka znajduje się w okolicy krzywizny mniejszej i antrum, znacznie rzadziej - na krzywiźnie większej oraz w okolicy kanału odźwiernika. 90% owrzodzeń dwunastnicy znajduje się w okolicy opuszkowej. W badaniu morfologicznym wycinka biopsyjnego pobranego z dna i brzegów owrzodzenia ujawniono pozostałości komórkowe w postaci nagromadzenia śluzu z domieszką gnijących leukocytów, erytrocytów i złuszczonych komórek nabłonka, pod którymi znajdują się włókna kolagenowe. 43. Leczenie wrzodów żołądka Leczenie. Racjonalna terapia wrzodów trawiennych powinna obejmować schemat, odpowiednie odżywianie, leczenie farmakologiczne, psychoterapię, zabiegi fizykalne i uzdrowiskowe. W okresie zaostrzenia choroby wrzodowej należy ściśle obserwować rozdrobnienie w żywieniu (od 4 do 6 razy dziennie przy niewielkiej ilości każdej porcji pokarmu przyjmowanej w określonych godzinach). Produkty spożywcze powinny mieć dobre właściwości buforujące i zawierać wystarczającą ilość białka (120-140 g). Psychoterapia jest niezbędna do zatrzymania lub zredukowania reakcji psychoneurotycznych wynikających z zespołu przewlekłego bólu i jego oczekiwania. Leki stosowane w leczeniu wrzodów trawiennych dzielą się na 5 grup: 1) leki wpływające na czynnik kwasowo-peptyczny (leki zobojętniające i histaminowe blokery H2, inne środki przeciwwydzielnicze); 2) leki poprawiające barierę śluzówkową żołądka; 3) leki zwiększające syntezę endogennych prostaglandyn; 4) środki przeciwbakteryjne i antyseptyczne; 5) leki normalizujące zaburzenia motoryczno-ewakuacyjne żołądka i dwunastnicy. Leki zobojętniające: 1) rozpuszczalny (wchłanialny) - wodorowęglan sody, węglan wapnia (kreda) i tlenek magnezu (magnezja palona); 2) nierozpuszczalne (niewchłanialne): trójkrzemian magnezu i wodorotlenek glinu. Kilka schematów terapii skojarzonej (dwu-, trzy-, czteroskładnikowej). Terapia dwuskładnikowa: amoksycylina 1000 mg 2 razy dziennie przez 2 tygodnie; omeprazol 40 mg dwa razy na dobę. Schemat trójskładnikowy obejmuje przygotowanie bizmutu koloidalnego 2 mg 120 razy dziennie; tetracyklina 4 mg 250 razy dziennie; metronidazol 4 mg 250 razy dziennie. Cykl terapii trwa 4 dni. Schemat czteroskładnikowy obejmuje omeprazol w dawce 20 mg 2 razy dziennie od 1. do 10. dnia; denol 120 mg 4 razy dziennie od 4 do 10 dnia; tetracyklina 500 mg 4 razy dziennie od 4 do 10 dnia; metronidazol 500 mg 3 razy dziennie od 4 do 10 dnia. Najbardziej skuteczny jest czteroskładnikowy schemat leczenia choroby wrzodowej żołądka i dwunastnicy. Po 6 tygodniach od jego wdrożenia wygojenie wady trawiennej obserwuje się u 93-96% pacjentów. Po bliznowaceniu wrzodu trawiennego żołądka i dwunastnicy tradycyjnie stosuje się dwa rodzaje leczenia. 1. Ciągłą terapię podtrzymującą prowadzi się lekami przeciwwydzielniczymi w połowie dziennej dawki przez okres do jednego roku. 2. Terapia „na żądanie” polega na stosowaniu jednego ze środków przeciwwydzielniczych w połowie dziennej dawki przez dwa tygodnie, gdy pojawią się objawy wrzodu trawiennego. 44. Przewlekłe zapalenie jelit. Etiologia, patogeneza, klasyfikacja Przewlekłe zapalenie jelit to choroba jelita cienkiego, charakteryzująca się naruszeniem jego funkcji (trawienie i wchłanianie) na tle zmian dystroficznych i dysregeneracyjnych, których kulminacją jest rozwój stanu zapalnego, zanik i stwardnienie błony śluzowej jelita cienkiego. Etiologia i patogeneza. Jest to choroba polietiologiczna, która może być wynikiem ostrego zapalenia jelita cienkiego lub pierwotnego przewlekłego procesu. W ostatnich latach duże znaczenie jako czynnik etiologiczny przewlekłego zapalenia jelit zyskały Yersinia, Helicobacteria, Proteus, Pseudomonas aeruginosa, rotawirusy, liczni przedstawiciele pierwotniaków i robaków pasożytniczych (giardia, ascaris, tasiemce, opistorchia, cryptosporidium). Duże znaczenie w występowaniu przewlekłego zapalenia jelit mają czynniki pokarmowe - przejadanie się, jedzenie suchej karmy, niezrównoważone, głównie węglowodanowe pokarmy, nadużywanie przypraw. Zapalenie jelit jest spowodowane promieniowaniem jonizującym, narażeniem na substancje toksyczne i leki. Wśród powszechnych mechanizmów patogenetycznych przewlekłych chorób jelita cienkiego występują zmiany w mikroflorze jelitowej na tle zmniejszenia odporności miejscowej i ogólnej. Zmiany stanu immunologicznego - zmniejszenie zawartości wydzielniczej lgA, wzrost poziomu lgE, zmniejszenie transformacji blastycznej limfocytów i zahamowanie migracji leukocytów - prowadzą do kolonizacji jelita cienkiego przez przedstawicieli mikroflory oportunistycznej i spadek normalnej flory beztlenowej. Morfologicznie przewlekłe zapalenie jelit objawia się zmianami zapalnymi i dysregeneracyjnymi błony śluzowej jelita cienkiego. Jeśli proces postępuje, obserwuje się jego atrofię i stwardnienie. Klasyfikacja (Zlatkina A.R., Frolkis A.V., 1985). 1. Etiologia: infekcje jelitowe, inwazje robaków pasożytniczych, czynniki pokarmowe, fizyczne i chemiczne, choroby żołądka, trzustki, dróg żółciowych. 2. Fazy choroby: zaostrzenie; umorzenie. 3. Stopień nasilenia: łagodny; umiarkowany; ciężki. 4. Przepływ: monotonny; nawracający; stale powtarzające się; utajony. 5. Charakter zmian morfologicznych: zespół bez atrofii; zapalenie jelita grubego z umiarkowaną częściową atrofią kosmków; zapalenie jelit z częściowym zanikiem kosmków; jednostka z całkowitym zanikiem kosmków. 6. Charakter zaburzeń czynnościowych: zaburzenia trawienia błon (niedobór disacharydazy), zaburzenia wchłaniania wody, elektrolitów, pierwiastków śladowych, witamin, białek, tłuszczów, węglowodanów. 7. Powikłania: zapalenie słoneczne, niespecyficzne mesadenitis. 45. Obraz kliniczny i rozpoznanie przewlekłego zapalenia jelit obraz kliniczny. Obraz kliniczny przewlekłego zapalenia jelit składa się z miejscowych i ogólnych zespołów jelitowych. Pierwszy wynika z naruszenia procesów trawienia ciemieniowego (błonowego) i jamy ustnej (maltrawienie). Pacjenci skarżą się na wzdęcia, bóle w okolicy pępkowej, wzdęcia w postaci czapki, głośne dudnienie, biegunkę, rzadziej zaparcia. Palpacja ujawnia ból w mezogastrium, a także po lewej stronie i nad pępkiem (pozytywny objaw Porges), plusk w okolicy kątnicy (objaw Obraztsova). Kał nabiera gliniastego wyglądu, charakterystyczna jest polyfecalia. Ogólny zespół jelitowy związany jest z zaburzeniami wchłaniania składników pokarmowych (złe wchłanianie), co skutkuje zaburzeniami wszystkich rodzajów metabolizmu, zmianami homeostazy. Charakteryzuje się wieloaspektowymi zaburzeniami metabolicznymi, przede wszystkim białkowymi, co objawia się postępującą utratą masy ciała. Zmiany w metabolizmie węglowodanów są mniej wyraźne, co objawia się wzdęciami, dudnieniem w jamie brzusznej oraz nasiloną biegunką podczas przyjmowania nabiału. W dużej mierze niedobór masy ciała u pacjentów wynika nie tylko z braku białka, ale także z braku równowagi lipidowej. Zmiany w metabolizmie lipidów są ściśle związane z zaburzeniami metabolicznymi witamin rozpuszczalnych w tłuszczach i minerałów (wapń, magnez, fosfor). Charakterystyczne objawy niedoboru wapnia to pozytywny objaw wałka mięśniowego, drgawki, nawracające „niezmotywowane” złamania kości, osteoporoza, osteomalacja. Diagnostyka i diagnostyka różnicowa. Ogólne badanie krwi ujawnia niedokrwistość mikro- i makrocytarną, wzrost ESR, aw ciężkich przypadkach - limfo- i eozynopenię. Jeśli choroba ma podłoże pasożytnicze, we krwi można zaobserwować limfocytozę i eozynofilię. W badaniu skatologicznym stwierdza się jelitową biegunkę tłuszczową spowodowaną kwasami tłuszczowymi i mydłami, twórca, amylorrhea. Zwiększa się zawartość enterokinazy i fosfatazy alkalicznej w kale. Dzienna masa kału znacznie wzrasta. Biochemiczne badanie krwi wykazuje hipoproteinemię, hipoalbuminemię, hipoglobulinemię, hipokalcemię, obniżony poziom magnezu, fosforu i innych pierwiastków śladowych, zaburzenia gospodarki elektrolitowej w postaci obniżonego poziomu sodu i potasu. Obraz morfologiczny łagodnej postaci przewlekłego zapalenia jelit charakteryzuje się pogrubieniem kosmków, ich deformacją, zmniejszeniem głębokości nacięć, zmniejszeniem napięcia mięśni gładkich, obrzękiem podnabłonkowym, zmianami zwyrodnieniowymi powierzchni nabłonka , ścieńczenie rąbka szczoteczkowego komórek, zmniejszenie liczby komórek kubkowych w okolicy kosmków, zwiększenie liczby krypt, naciekanie błony śluzowej warstwy własnej elementami limfoplazmatycznymi, zmniejszenie liczby komórek Panetha w okolicy dna krypt. 46. Leczenie, rokowanie przewlekłego zapalenia jelit Leczenie. Leczenie przewlekłego zapalenia jelit powinno być kompleksowe, obejmujące czynniki wpływające na czynniki etiologiczne, mechanizmy patogenetyczne oraz miejscowe i ogólne objawy choroby. Podstawą jest żywienie dietetyczne, które przyczynia się do obniżenia podwyższonego ciśnienia osmotycznego w jamie jelitowej, ogranicza wydzielanie oraz normalizuje pasaż treści jelitowej. Terapia lekowa powinna mieć charakter etiotropowy, patogenetyczny i objawowy. Leczenie etiotropowe: w przypadku dysbiozy stopnia II-IV przepisuje się leki przeciwbakteryjne: metronidazol (0,5 g 3 razy dziennie), klindamycynę (0,5 g 4 razy dziennie), cefaleksynę (0,5 g 2 razy dziennie) dzień), biseptol ( 0,48 g 2 razy dziennie), sulgina (1 g 3-4 razy dziennie), furazolidon (0,1 g 4 razy dziennie). Po zastosowaniu leków przeciwbakteryjnych przepisuje się eubiotyki - bifidumbakteryna lub bifikol 5 dawek 3 razy dziennie 30 minut przed posiłkiem, kolibakteryna lub laktobakteryna 3 dawki 3 razy dziennie przed posiłkami, hilak-forte 40 kropli 3 razy dziennie przed posiłkami. Leczenie preparatami bakteryjnymi prowadzi się przez długi czas: 3 kursy po 3 miesiące każdego roku. W przypadku dysbakteriozy gronkowcowej przepisywany jest bakteriofag antystafilokokowy (20 ml 3 razy dziennie przez 15-20 dni), w przypadku dysbakteriozy proteus - bakteriofag coliproteus doustnie, 20 ml 3 razy dziennie, przebieg leczenia wynosi 2-3 tygodnie. W celu usprawnienia procesu trawienia zalecane są enzymy: pankreatyna, panzinorm forte, festal, trawienie, pankurmen, mezim forte, trienzym, których dawki dobierane są indywidualnie (od 1 tabletki 3 razy dziennie do 3-4 tabletek 4 razy dziennie ) i które są przepisywane bezpośrednio przed lub w trakcie posiłków przez 2-3 miesiące. W razie potrzeby enzymatyczną terapię zastępczą kontynuuje się przez dłuższy czas. Aby skorygować zaburzenia wodno-elektrolitowe, dożylne iniekcje pananginy 20-30 ml, glukonian wapnia 10% 10-20 ml w 200-400 ml roztworu izotonicznego lub roztworu glukozy, roztwory polijonowe „Disol”, „Trisol”, „Quartasol” są wskazane. Roztwory elektrolitów podaje się dożylnie przez 10-20 dni pod kontrolą stanu kwasowo-zasadowego i poziomu elektrolitów we krwi. Prognozowanie i zapobieganie. Prognozy dotyczące życia i zdolności do pracy w większości przypadków są korzystne. Niekorzystnymi prognostycznie objawami są stale nawracający przebieg choroby, ostra znaczna utrata masy ciała, niedokrwistość, zespół zaburzeń endokrynologicznych (obniżone libido, bolesne miesiączkowanie, niepłodność). Zapobieganie przewlekłemu zapaleniu jelit polega na szybkim leczeniu ostrych infekcji jelitowych i współistniejących chorób strefy żołądka i dwunastnicy, zgodnie z dietą, w profilaktycznym podawaniu preparatów bakteryjnych podczas prześwietlenia i radioterapii. 47. Etiologia, patogeneza, obraz kliniczny choroby Leśniowskiego-Crohna Choroba Leśniowskiego-Crohna jest przewlekłą chorobą jelit z objawami ogólnoustrojowymi; którego podstawą morfologiczną jest ziarniniakowe autoimmunologiczne zapalenie przewodu pokarmowego. Etiologia i patogeneza. Etiologia i patogeneza choroby nie są dobrze poznane. Najbardziej popularne są zakaźne i immunologiczne koncepcje początku choroby. W ostatnich latach pojawiły się doniesienia o etiologicznej roli drobnoustrojów z rodzaju Yersinia. Trudno jednak ustalić, czy te czynniki drobnoustrojowe są patogenami czy komensalami. Jednocześnie istotną rolę w patogenezie choroby odgrywają zmiany w mikroflorze jelitowej. Zazwyczaj zmniejszenie liczby bakterii typu bifidum z jednoczesnym wzrostem liczby enterobakterii z objawami patogenności. W rozwoju choroby rolę odgrywają mechanizmy autoimmunologiczne. W chorobie Leśniowskiego-Crohna pojawiają się autoprzeciwciała (lgC, lgM) przeciwko tkankom jelitowym. Klasyfikacja. Klasyfikacja (F. I. Komarov, A. I. Kazanov, 1992). 1. Kurs: ostry; chroniczny. 2. Charakterystyka procesu: zmiana w jelicie cienkim; uszkodzenie w okolicy krętniczo-kątniczej; uszkodzenie w okrężnicy. 3. Powikłania: zwężenie jelita; toksyczne rozszerzenie okrężnicy; przetoki; amyloidoza; kamica nerkowa, kamica żółciowa; Niedokrwistość z niedoboru witaminy B12. obraz kliniczny. Obraz kliniczny choroby Leśniowskiego-Crohna charakteryzuje się znacznym zróżnicowaniem, które determinowane jest lokalizacją i rozległością procesu patologicznego w jelicie, postacią choroby oraz dodatkowymi powikłaniami. Obiektywne badanie zwraca uwagę na bladość skóry, która koreluje z nasileniem niedokrwistości, obrzękiem nóg z powodu upośledzenia wchłaniania i metabolizmu białek. Podczas badania dotykowego brzucha obserwuje się wzdęcia i dudnienie. W badaniu przedmiotowym pacjenta stwierdza się bladość skóry, stan podgorączkowy, niedobór masy ciała, pętle skurczowe jelit, ból w okolicy pępkowej, w prawym biodrowym odcinku. W chorobie Leśniowskiego-Crohna obserwuje się pozajelitowe objawy choroby: aftowe zapalenie jamy ustnej, ropowicę i przetoki jamy ustnej, zapalenie stawów, przypominające reumatoidalne zapalenie stawów w klinice, z charakterystycznymi objawami symetrycznych zmian drobnych stawów, sztywność rano. Typowe zmiany w oczach: zapalenie tęczówki, zapalenie tęczówki i ciała rzęskowego, makulopatia. Na skórze może pojawić się rumień guzowaty i ropne zapalenie zgorzelinowe. Biegunka charakteryzuje się wzrostem częstości stolca do 10 razy dziennie lub więcej, materii wielokałowej. Objętość stolca zależy od anatomicznej lokalizacji procesu. U wszystkich pacjentów obserwuje się utratę masy ciała. 48. Diagnoza choroby Leśniowskiego-Crohna Diagnostyka i diagnostyka różnicowa. W klinicznym badaniu krwi podczas zaostrzenia wykrywa się leukocytozę, niedokrwistość i wzrost ESR. Zmiany w ogólnej analizie moczu pojawiają się w ciężkiej postaci, charakteryzującej się dodatkiem amyloidozy nerek (białkomocz). Biochemiczne badanie krwi ujawnia hipoproteinemię, hipoalbuminemię, wzrost α-globulin, zmniejszenie zawartości żelaza, witaminy B12, kwasu foliowego, cynku, magnezu i potasu. Dane z badania skatologicznego pozwalają pośrednio ocenić poziom zmiany. W koprogramie z lokalizacją procesu w jelicie cienkim stwierdza się materię wielokałową, stolce tłuszczowe, twórcę; w okrężnicy - domieszka śluzu, leukocytów, erytrocytów. Diagnostyka rentgenowska pozwala ustalić lokalizację i rozpowszechnienie procesu patologicznego w jelicie. Obszary zmienionego jelita przeplatają się z obszarami jelita niezmienionego. Zmienione pętle stają się sztywne, obraz jest mozaikowy z niewielkimi defektami wypełnienia oraz z przenikaniem kontrastu poza ścianę jelita w postaci kieszonek. Jelito w dotkniętym obszarze nabiera charakteru drobno frędzlowego, z utworzeniem pseudouchyłków. Zdolność skurczowa ściany jelita jest zmniejszona lub całkowicie utracona, ewakuacja baru spowalnia. Obserwuje się nierównomierne zwężenie światła jelita, w wyniku czego staje się ono tak wąskie, że przyjmuje formę koronki. Powyżej strefy zwężenia jelito rozszerza się. Diagnoza endoskopowa ma decydujące znaczenie w weryfikacji diagnozy. W przypadku choroby Leśniowskiego-Crohna najbardziej charakterystyczna jest zmiana w antrum żołądka i początkowej części dwunastnicy. Endoskopowo możliwe jest wykrycie kolistego zwężenia antrum, przypominającego zwężenie guza. Początkowy okres choroby Leśniowskiego-Crohna charakteryzuje się słabymi danymi endoskopowymi: matową błoną śluzową, na której widoczne są nadżerki typu aft, otoczone białawymi granulkami. Wzór naczyniowy jest nieobecny lub wygładzony. W świetle jelita i na jego ścianach określa się ropny śluz. W remisji klinicznej opisane zmiany mogą całkowicie zniknąć. W miarę postępu choroby błona śluzowa staje się nierównomiernie pogrubiona, ma białawy kolor i widoczne są duże powierzchowne lub głębokie owrzodzenia bruzd. Światło jelita zwęża się, co utrudnia prowadzenie kolonoskopu. Kolonoskopia umożliwia wykonanie celowanej biopsji błony śluzowej w dowolnej części okrężnicy oraz w końcowym odcinku jelita krętego. W chorobie Leśniowskiego-Crohna proces patologiczny zaczyna się w warstwie podśluzówkowej, dlatego biopsję należy wykonać w taki sposób, aby część warstwy podśluzówkowej dostała się do materiału biopsyjnego. W związku z powyższym w 54% przypadków nie wykryto morfologicznego podłoża choroby. 49. Leczenie choroby Leśniowskiego-Crohna Leczenie. Zalecana jest dieta oszczędzająca mechanicznie i chemicznie z dużą zawartością białka, witamin, mikroelementów, z wyjątkiem mleka w przypadku jego nietolerancji i ograniczenia grubego włókna roślinnego. Pokazano zastosowanie płynnych hydrolizatów dojelitowych. Salazopreparaty i kortykosteroidy stanowią podstawę farmakoterapii patogenetycznej. Dzienna dawka leków wynosi 3-6 g. Wraz z lokalizacją procesu patologicznego w jelicie grubym aktywność sulfasalazyny przewyższa aktywność prednizolonu. W przypadku braku efektu stosowania sulfasalazyny, ze zmianami głównie w jelicie cienkim i wyraźnymi objawami zapalenia immunologicznego, a także w obecności ogólnoustrojowych objawów choroby, wskazane jest stosowanie kortykosteroidów. Efekt ich stosowania odnotowuje się w ciągu pierwszych 8 tygodni od rozpoczęcia leczenia. Prednizolon jest przepisywany według następującego schematu: w szczycie zaostrzenia 60 mg na dobę, następnie dawkę stopniowo zmniejsza się i do 6-10 tygodnia dostosowuje się do dawki podtrzymującej 5-10 mg na dobę. Po osiągnięciu remisji klinicznej lek jest stopniowo anulowany. Jeśli remisja nie zostanie osiągnięta, leczenie prednizolonem jest kontynuowane w warunkach ambulatoryjnych do 52 tygodnia. W ciężkim przebiegu choroby, w przypadku powikłań pod postacią śpiączki obecnych przetok odbytniczo-pochwowych, skórno-jelitowych, jelitowo-jelitowych, wskazane jest podanie 6-merkaptopuryny doustnie w dawce 0,05 g 2-3 razy dziennie przez 10 dni kursy w odstępie 3 dni do remisji klinicznej. Następnie przestawiają się na przyjmowanie dawek podtrzymujących leku w ciągu roku. Dawka 6-merkaptopuryny w tym przypadku wynosi 75 mg na dobę. Efekt leczenia lekami immunosupresyjnymi można określić nie wcześniej niż po 3-4 miesiącach. Metronidazol znalazł szerokie zastosowanie w leczeniu choroby Leśniowskiego-Crohna, której głównymi wskazaniami są przetoki i szczeliny okołoodbytowe, brak działania leków salazalowych i glikokortykoidów, a także nawroty choroby po protektomii. Lek jest przepisywany w dawce 500-1000 mg na dzień. Czas trwania ciągłego kursu nie powinien przekraczać 4 tygodni. Leczenie objawowe choroby Leśniowskiego-Crohna ogranicza się do przepisywania krótkich kursów (2-3 dni) leków przeciwbiegunkowych (imodium, loperamid). Dawki dobierane są indywidualnie w zależności od efektu klinicznego. Leków przeciwbiegunkowych nie należy przepisywać przez dłuższy czas (ponad 5 dni). Ze względu na występowanie zespołu złego wchłaniania w chorobie Leśniowskiego-Crohna, stosuje się preparaty enzymatyczne niezawierające kwasów żółciowych (pankreatyna, mezim-forte, solisim, somilaza) w dawce od 2 do 6 tabletek do każdego posiłku. Według wskazań niedokrwistość i hipoalbuminemię koryguje się przepisując suplementy żelaza (pozajelitowo) i podając alwezynę, hydrolizery białek, aminopeptyd, aminokrowinę. Multiwitaminy są przepisywane w tabletkach, a niezbędne produkty w kapsułkach. Leczenie dysbiozy odbywa się według ogólnych zasad. 50. Klasyfikacja niespecyficznego wrzodziejącego zapalenia jelita grubego Niespecyficzne wrzodziejące zapalenie jelita grubego jest chorobą zapalną, która atakuje błonę śluzową okrężnicy ze zmianami wrzodziejąco-destrukcyjnymi, która ma przewlekły, nawracający przebieg, któremu często towarzyszy rozwój powikłań zagrażających życiu. Klasyfikacja (Yu. V. Baltaitis i in., 1986). Charakterystyka kliniczna. 1. Forma kliniczna: 1) ostry; 2) przewlekłe. 2. Aktualne: 1) szybko postępujący; 2) ciągłe nawroty; 3) nawracające; 4) utajony. 3. Stopień aktywności: 1) zaostrzenie; 2) zaostrzenie zanikania; 3) umorzenie. 4. Dotkliwość: 1) światło; 2) umiarkowany; 3) ciężki. Charakterystyka anatomiczna. 1. Charakterystyka makroskopowa: 1) zapalenie odbytnicy: 2) zapalenie odbytnicy; 3) zmiana częściowa; 4) całkowita porażka. 2. Charakterystyka mikroskopowa: 1) przewaga procesów niszcząco-zapalnych; 2) redukcja procesów zapalnych z elementami naprawczymi; 3) konsekwencje procesu zapalnego Powikłania. 1. Lokalne: 1) krwawienie z jelit; 2) perforacja okrężnicy; 3) zwężenie okrężnicy; 4) pseudopolipowatość; 5) wtórne zakażenie jelitowe; 6) zanik błony śluzowej; 7) toksyczne rozszerzenie okrężnicy; 8) nowotwór złośliwy. 2. Ogólne: 1) czynnościowa hipokortyka; 2) sepsa; 3) objawy ogólnoustrojowe - zapalenie stawów, zapalenie stawów krzyżowo-biodrowych, zmiany skórne, zapalenie tęczówki, amyloidoza, zapalenie żył, stwardniające zapalenie dróg żółciowych, dystrofia wątroby. 51. Obraz kliniczny wrzodziejącego zapalenia jelita grubego obraz kliniczny. Klinika wrzodziejącego zapalenia jelita grubego jest polimorficzna i zależy od ciężkości przebiegu i nasilenia procesu. Przebieg procesu zapalnego, uważanego częściej za przewlekły, w niektórych przypadkach przybiera ostry charakter. Zakres zmiany okrężnicy może się również różnić. Wrzodziejące zapalenie jelita grubego charakteryzuje się 3 głównymi objawami: uwolnieniem szkarłatnej krwi podczas wypróżnień, zaburzeniami czynności jelit i bólem brzucha. Dysfunkcja jelit objawia się dolegliwościami powtarzających się niestabilnych stolców, co jest wynikiem rozległego uszkodzenia błony śluzowej oraz zmniejszenia wchłaniania wody i soli. Najczęściej biegunka występuje z ciężkim wrzodziejącym zapaleniem jelita grubego. Jednak biegunka nie jest wiarygodnym wskaźnikiem nasilenia procesu. Znaczenie ma nasilenie biegunki w połączeniu z obecnością czerwonej krwi w stolcu. U znacznej liczby pacjentów z wrzodziejącym zapaleniem jelita grubego na powierzchni powstałego kału okresowo znajdują się krew i śluz, co często błędnie uważa się za przejaw hemoroidów. Łagodny przebieg nieswoistego wrzodziejącego zapalenia jelita grubego charakteryzuje się zadowalającym stanem pacjentów. Ból brzucha jest umiarkowany i krótkotrwały. Krzesło jest dekorowane, przyspieszone, do 2-3 razy dziennie. W kale znajdują się krew i śluz. Proces zlokalizowany jest w odbytnicy i esicy. Przebieg kliniczny jest nawracający. Efekt leczenia salazopreparatami jest zadowalający. Nawroty występują nie więcej niż 2 razy w roku. Remisje mogą trwać długo (ponad 2-3 lata). Umiarkowany przebieg choroby rozpoznaje się, gdy pacjent ma biegunkę. Fotel jest częsty (do 6-8 razy dziennie), w każdej porcji widoczna domieszka krwi i śluzu. Bóle skurczowe brzucha są bardziej intensywne. Występuje przerywana gorączka ze wzrostem temperatury ciała do 38 C, intensywne ogólne osłabienie. Mogą również wystąpić pozajelitowe objawy choroby (zapalenie stawów, zapalenie błony naczyniowej oka, rumień guzowaty). Kurs jest stale nawracający, efekt salazopreparatów jest niestabilny, podczas zaostrzeń przepisywane są hormony. Ciężka postać choroby charakteryzuje się ostrym początkiem. Całkowite uszkodzenie jelita grubego szybko rozwija się wraz z rozprzestrzenianiem się procesu patologicznego w głąb ściany jelita. Stan pacjenta gwałtownie się pogarsza. Klinika charakteryzuje się nagłym początkiem, wysoką gorączką, obfitymi biegunkami do 24 razy na dobę, obfitymi krwawieniami jelitowymi oraz szybkim wzrostem odwodnienia. Pojawia się tachykardia, obniża się ciśnienie krwi, wzrastają pozajelitowe objawy niespecyficznego wrzodziejącego zapalenia jelita grubego. Leczenie zachowawcze nie zawsze jest skuteczne i często konieczna jest pilna operacja. 52. Rozpoznanie nieswoistego wrzodziejącego zapalenia jelita grubego Diagnostyka i diagnostyka różnicowa. W klinicznych badaniach krwi z łagodną postacią choroby nie zmienia się niewielka leukocytoza neutrofilowa, wzrost ESR i liczba czerwonych krwinek. Wraz ze wzrostem ciężkości przebiegu i wzrostem czasu trwania zaostrzenia pojawia się niedokrwistość o mieszanej genezie (niedobór witaminy B12 i niedobór żelaza), a ESR wzrasta. W analizie biochemicznej krwi w postaciach umiarkowanych i ciężkich obserwuje się dysproteinemię, hipoalbuminemię, hipergammaglobulinemię, zaburzenia równowagi elektrolitowej i stan kwasowo-zasadowy. W ogólnej analizie moczu zmiany pojawiają się tylko wtedy, gdy powikłania występują w postaci zespołu nerczycowego na tle amyloidozy, gdy obserwuje się charakterystyczne zmiany w badaniach moczu - białkomocz, "martwy" osad moczu, występuje również wzrost krwi oraz poziom kreatyniny, mocznika. Główną rolę w diagnostyce odgrywa badanie endoskopowe z celowaną biopsją, ponieważ w nieswoistym wrzodziejącym zapaleniu jelita grubego głównie dotyczy to błony śluzowej jelita grubego. Odbytnica jest zawsze zaangażowana w proces patologiczny, tj. zmiany erozyjne i wrzodziejące są wykrywane podczas endoskopii bezpośrednio za zwieraczem odbytu podczas sigmoidoskopii. We wrzodziejącym zapaleniu jelita grubego nie zawsze jest możliwe pokonanie zgięcia odbytniczo-sigmoidalnego z powodu silnego skurczu. Próbie trzymania rurki proktoskopu towarzyszy silny ból. W tej sytuacji proktoskop należy wprowadzić na głębokość nie większą niż 12-15 cm. Obraz endoskopowy zależy od postaci choroby. Przy łagodnej postaci widoczne są obrzęknięte, matowe błony śluzowe, gęste białawe naloty śluzu na ściankach jelita, lekkie krwawienie kontaktowe. Wzór naczyniowy warstwy podśluzówkowej nie jest określany wizualnie. W umiarkowanym przebiegu choroby ujawniają się przekrwienie i obrzęk błony śluzowej, silne krwawienia kontaktowe, krwotoki, nadżerki i owrzodzenia o nieregularnym kształcie, grube naloty śluzu na ściankach jelita. W ciężkim przebiegu choroby błona śluzowa okrężnicy ulega znacznemu zniszczeniu. Stwierdzono ziarnistą, krwawiącą powierzchnię wewnętrzną, rozległe obszary owrzodzenia ze złogami włóknikowatymi, pseudopolipy o różnych rozmiarach i kształtach, ropę i krew w świetle jelita. Przeciwwskazaniami do kolonoskopii i sigmoidoskopii są ciężkie postacie wrzodziejącego zapalenia jelita grubego w ostrym stadium choroby. W przypadku epidemii infekcji jelitowych diagnozę można łatwo ustalić. Ale nawet w przypadku sporadycznej zachorowalności w ostrych infekcjach jelitowych zespół zapalenia jelita grubego przebiega bez nawrotów, podczas gdy wrzodziejące zapalenie jelita grubego ma nawracający przebieg. Najdokładniejsze metody identyfikacji ostrej infekcji jelitowej obejmują bakteriologiczne i serologiczne. 53. Leczenie nieswoistego wrzodziejącego zapalenia jelita grubego Leczenie. Brak jednego czynnika etiologicznego oraz złożoność patogenezy nieswoistego wrzodziejącego zapalenia jelita grubego utrudniają leczenie tej choroby. Stosowane są leki przeciwzapalne i przeciwbakteryjne: salazopirydazyna, sulfasalazyna, salazodimetoksyna, salofalk. Przyjęta sulfasalazyna, przy udziale mikroflory jelitowej, rozkłada się na kwas 5-aminosalicylowy i sulfapirydynę. Niewchłonięta sulfapirydyna hamuje wzrost mikroflory beztlenowej w jelicie, w tym Clostridia i bakterioidy. A dzięki kwasowi 5-aminosalicylowemu lek nie tylko powoduje zmiany w mikroflorze jelitowej, ale także moduluje odpowiedzi immunologiczne, blokuje mediatory procesu zapalnego. Lek jest przepisywany w dawce 2-6 g dziennie przez cały okres aktywnego zapalenia. Gdy zespół zapalenia okrężnicy ustępuje, dawka sulfasalazyny jest stopniowo zmniejszana, doprowadzając ją do dawki podtrzymującej (średnio 1-1,5 tabletki dziennie). W ciężkim zespole biegunkowym u osób z łagodnym i umiarkowanym przebiegiem choroby wskazane jest wyznaczenie sandostatyny, która hamuje syntezę hormonów żołądkowo-jelitowych i amin biogennych (wazoaktywny peptyd jelitowy, gastryna, serotonina), których produkcja jest gwałtownie zwiększona w wrzodziejące zapalenie jelita grubego i choroba Leśniowskiego-Crohna. A także lek zmniejsza wydzielanie i poprawia wchłanianie w jelicie, hamuje trzewny przepływ krwi i zmniejsza ruchliwość. Przy stosowaniu sandostatyny (w ciągu 7 dni w dawce 0,1 mg 2 razy, podskórnie) zmniejsza się biegunka, parcie praktycznie znika, a wydalanie krwi z kałem zmniejsza się. W ciężkiej postaci niespecyficznego wrzodziejącego zapalenia jelita grubego leczenie prowadzi się na tle żywienia pozajelitowego. Zawartość białka w tych preparatach powinna wynosić około 1,5-2,0 g/kg masy ciała. Kortykosteroidy, które są podawane pozajelitowo, są patogenetycznym leczeniem ciężkiej postaci choroby: w pierwszym dniu prednizon podaje się dożylnie w odstępach 12 godzin (90-120 mg lub więcej), w ciągu następnych 5 dni - domięśniowo, stopniowo zmniejszając dawkę. Z pozytywnym efektem przechodzą na leki doustne (prednizolon 40 mg dziennie). W umiarkowanej postaci przebiegu niespecyficznego wrzodu wrzodowego wymagana jest ścisła dieta z ograniczeniem błonnika, produktów mlecznych i wysokiej zawartości białka. Prednizolon jest przepisywany doustnie w początkowej dawce 20-40 mg na dobę. Leczenie można uzupełnić sulfasalazyną i jej analogami, które przyjmuje się doustnie lub podaje do odbytnicy w mikroklisterach i czopkach. Początkowa dawka sulfasalazyny wynosi 1 g dziennie, następnie zwiększa się ją do 4-6 g. Jako pomocniczą metodę leczenia można stosować wywary z ziół o działaniu przeciwzapalnym i hemostatycznym (korzeń czarniaka, liść pokrzywy, porosty, szyszki olchy szarej, korzeń lukrecji), ziołolecznictwo często pozwala zmniejszyć dawkę salazopreparatów, przedłużyć umorzenie. 54. Obraz kliniczny ostrego gromerulonephritis Ostre kłębuszkowe zapalenie nerek (AGN) to ostra rozlana choroba nerek o charakterze zakaźno-alergicznym, zlokalizowana w kłębuszkach nerkowych. AGN może być chorobą niezależną (pierwotną) lub wtórną jako część innej choroby, komplikując obraz kliniczny i diagnozę tej ostatniej. AGN zwykle dotyka mężczyzn młodych i w średnim wieku. obraz kliniczny. Obraz kliniczny choroby składa się z następujących zespołów. zespół moczowy. 1. Proteinuria ze względu na przechodzenie cząsteczek białka przez przestrzenie ściany naczyń włosowatych kłębuszków nerkowych, powstałe podczas osadzania się na nich kompleksów immunologicznych. Proteinuria ma charakter selektywny, w którym przez „filtr kłębuszkowy” przechodzą głównie albuminy. 2. Krwiomocz z powodu zaangażowania w patologiczny proces mezangium włośniczkowego i tkanki śródmiąższowej. Erytrocyty przenikają przez najmniejsze szczeliny w błonie podstawnej, zmieniając swój kształt. 3. Cylindruria - wydalanie z moczem cylindrycznych komórek kanalików. Podczas procesów dystroficznych w kanalikach rozpadających się komórek nabłonka nerek powstają ziarniste cylindry składające się z gęstej ziarnistej masy; woskowe cylindry mają ostre kontury i jednorodną strukturę; szkliste odlewy to formacje białkowe. Zespół nadciśnieniowy obserwuje się z powodu: 1) retencja sodu i wody; 2) aktywacja układu renina-angiotensyna-aldosteron i współczulno-nadnerczowa; 3) zmniejszenie funkcji układu depresyjnego nerek. Zespół obrzęku wiąże się z następującymi czynnikami: 1) spadek filtracji kłębuszkowej z powodu ich porażki; 2) zmniejszenie ładunku filtracyjnego sodu i wzrost jego reabsorpcji; 3) retencja wody spowodowana zatrzymaniem sodu w organizmie; 4) wzrost BCC; 5) wtórny hiperaldosteronizm; 6) wzrost wydzielania ADH i wzrost wrażliwości na nie dystalnego nefronu, co prowadzi do zatrzymania płynów; 7) wzrost przepuszczalności ścian naczyń włosowatych i uwalnianie osocza do tkanek; 8) spadek ciśnienia onkotycznego osocza z masywnym białkomoczem. 55. Diagnoza ostrego gromerulonephritis Diagnostyka. W 100% przypadków w badaniu moczu zdiagnozowano białkomocz o różnym nasileniu, cylindrurię i, co najważniejsze dla diagnozy, krwiomocz o różnym nasileniu - od mikrohematurii (do 10 erytrocytów na pole widzenia) po makrohematurię (choć dość rzadką). Jeśli jednak podejrzewa się AGN, konieczne jest przeprowadzenie serii powtórnych badań moczu lub wykonanie testu Nechiporenko (oznaczenie liczby utworzonych elementów w 1 μl), ponieważ erytrocyty mogą nie zostać wykryte w pojedynczej porcji moczu. Badanie krwi ujawnia wskaźniki ostrej fazy (wzrost zawartości fibrynogenu i a2-globuliny, białka C-reaktywnego, przyspieszenie ESR), liczba leukocytów zmienia się nieznacznie, umiarkowana niedokrwistość. W nieskomplikowanym przebiegu AGN zawartość substancji azotowych (kreatyniny, indican, mocznika) we krwi nie zmienia się. W początkowej fazie choroby obserwuje się zmianę w teście Reberga - spadek filtracji kłębuszkowej i wzrost reabsorpcji kanalikowej, która normalizuje się wraz z powrotem do zdrowia. Badanie rentgenowskie u pacjentów z ciężkim nadciśnieniem tętniczym może wykazać umiarkowany wzrost lewej komory, która przybiera takie same rozmiary, jak pacjent wraca do zdrowia. Istnieją 3 kliniczne warianty AGN. 1. Wariant monosymptomatyczny: drobne dolegliwości, brak obrzęku i nadciśnienia tętniczego, występuje tylko zespół moczowy; najczęstszy wariant przebiegu choroby (86% przypadków). 2. Wariant nerczycowy: wyraźny obrzęk, skąpomocz, możliwe jest zwiększenie ciśnienia krwi do stosunkowo niskich wartości, wykrywa się go u 8% pacjentów. 3. Wersja rozszerzona: nadciśnienie tętnicze, osiągające wysokie wartości (180/100 mm Hg), umiarkowanie nasilony obrzęk, niewydolność krążenia występuje w 6% przypadków. 56. Leczenie ostrego gromerulonephritis Leczenie. Leczenie AGN jest złożone i obejmuje następujące czynności. 1. Tryb. W przypadku podejrzenia AGN lub natychmiast po ustaleniu diagnozy pacjent powinien być natychmiast hospitalizowany. Ścisły leżenie w łóżku należy obserwować przez około 2-4 tygodnie, aż do ustąpienia obrzęku i normalizacji ciśnienia krwi. Przebywanie w łóżku zapewnia równomierne rozgrzanie organizmu, co prowadzi do zmniejszenia skurczu naczyń (a tym samym do obniżenia ciśnienia krwi) oraz do wzrostu filtracji kłębuszkowej i diurezy. Po wypisaniu ze szpitala wskazane jest leczenie domowe przez okres do 4 miesięcy od dnia wystąpienia choroby, co stanowi najlepszą prewencję przejścia AGN do stadium przewlekłego. 2. Dieta. W zależności od nasilenia objawów klinicznych bardzo ważne jest ograniczenie płynów i chlorku sodu. Przy postaci rozszerzonej i nerczycowej zaleca się całkowity post przez 1-2 dni z przyjmowaniem płynów w ilości równej diurezie. W 2-3 dniu pokazano spożycie żywności bogatej w sole potasu (owsianka ryżowa, ziemniaki). Całkowita ilość wypijanej wody dziennie powinna być równa objętości moczu przeznaczonej na dzień poprzedni plus 300-500 ml. Po 3-4 dniach pacjent przechodzi na dietę z ograniczeniem białka (do 60 g dziennie), a całkowita ilość soli nie przekracza 3-5 g / dzień. Taka dieta jest zalecana do ustąpienia wszelkich objawów pozanerkowych i gwałtownej poprawy osadu moczowego. 3. Farmakoterapia obejmuje przede wszystkim terapię przeciwbakteryjną, która jednak powinna być prowadzona tylko wtedy, gdy zakaźny charakter AGN jest wiarygodnie ustalony (patogen został wyizolowany i minęły nie więcej niż 3 tygodnie od początku choroba). Zwykle przepisywana penicylina lub jej półsyntetyczne analogi w konwencjonalnych dawkach. Obecność wyraźnych ognisk przewlekłej infekcji (zapalenie migdałków, zapalenie zatok itp.) jest również bezpośrednim wskazaniem do antybiotykoterapii. Diuretyki w leczeniu AGN są wskazane tylko przy zatrzymaniu płynów, podwyższonym ciśnieniu krwi i pojawieniu się niewydolności serca. Najskuteczniejszy furosemid (40-80 mg), stosowany do czasu eliminacji obrzęków i nadciśnienia. Nie ma potrzeby długoterminowego przepisywania tych leków, wystarczą 3-4 dawki. W przypadku braku obrzęku, ale utrzymującego się nadciśnienia lub niedostatecznego działania przeciwnadciśnieniowego saluretyków, leki przeciwnadciśnieniowe (klofelina, dopegyt) są przepisywane z czasem podawania zależnym od utrzymywania się nadciśnienia tętniczego. W przypadku długotrwałego białkomoczu indometacynę lub woltaren przepisuje się w dawce 75-150 mg na dobę (przy braku nadciśnienia i skąpomoczu). Rokowanie jest korzystne, jednak przy długotrwałych formach istnieje możliwość, że proces stanie się przewlekły. Zapobieganie AGN sprowadza się do skutecznego leczenia infekcji ogniskowej, racjonalnego stwardnienia. Aby w porę wykryć początek choroby po szczepieniu, przeniesiony SARS u wszystkich pacjentów, konieczne jest zbadanie moczu.
▪ Prawo konstytucyjne (państwowe) Federacji Rosyjskiej. Kołyska
Maszyna do przerzedzania kwiatów w ogrodach
02.05.2024 Zaawansowany mikroskop na podczerwień
02.05.2024 Pułapka powietrzna na owady
01.05.2024
▪ GIS jest przydatny dla polityków ▪ Krzem zachowuje przewodność przy bardzo niskich poziomach naładowania ▪ Fulguryci opowiadają o starożytnym klimacie ▪ Platforma MediaTek LinkIt Smart 7688
▪ sekcja witryny Rzeczy szpiegowskie. Wybór artykułów ▪ artykuł Cała Rosja spoczywa na Iwanowach. Popularne wyrażenie ▪ artykuł Gdzie i kiedy wyemitowano pieniądze zabezpieczone opium? Szczegółowa odpowiedź ▪ artykuł Kierownik laboratorium fotograficznego. Opis pracy ▪ artykuł Rozciągnięty węzeł. Sekret ostrości
Strona główna | biblioteka | Artykuły | Mapa stony | Recenzje witryn www.diagram.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese





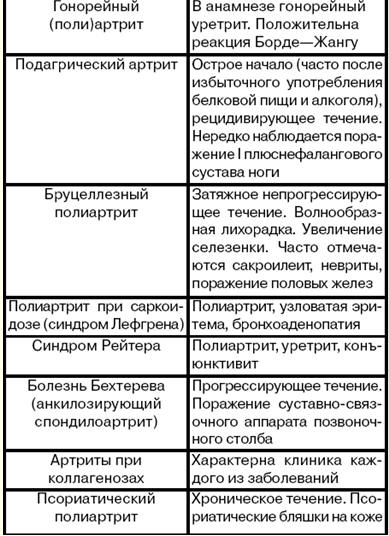
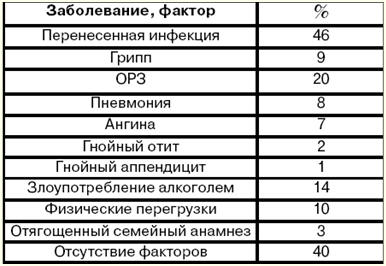
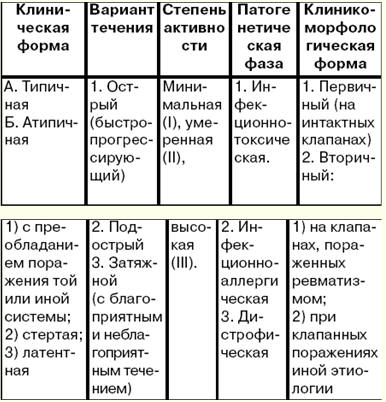
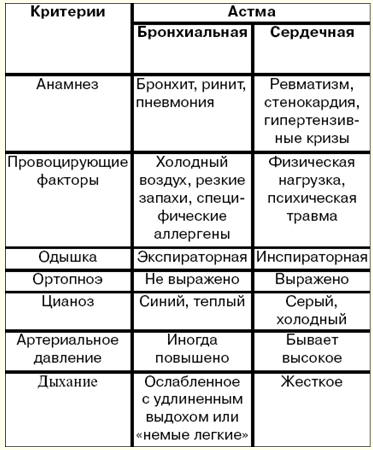

 Zobacz inne artykuły Sekcja
Zobacz inne artykuły Sekcja 